
Аминокислоты

Аминокислоты — органические амфотерные соединения, в состав которых входят карбоксильные группы – СООН и аминогруппы - NH 2 .
Аминокислоты можно рассматривать как карбоновые кислоты, в молекулах которых атом водорода в радикале замещен аминогруппой.

Строение
Общая формула (NH 2 ) m R(COOH) n, где m и n чаще всего равны 1 или 2. таким образом, аминокислоты сое6динения со смешанными функциями
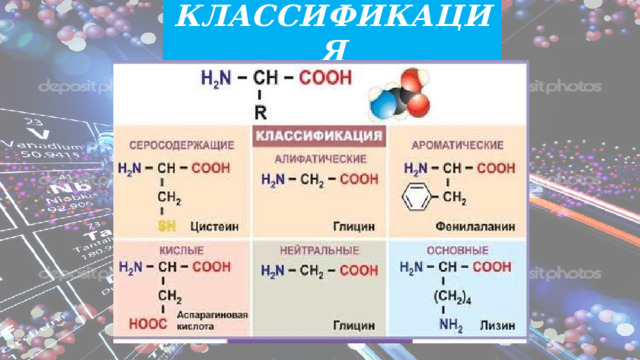
КЛАССИФИКАЦИЯ

Аминокислоты классифицируют по структурным признакам.
В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на α-, β-, γ-, δ-, ε- и т. д.

По числу функциональных групп
- моноаминомонокарбоновые кислоты;
- диаминомонокарбоновые кислоты
- моноаминодикарбоновые кислоты

Аминокислоты делят на:
Их около 150, они были обнаружены в живых организмах, около 20 из них входят в состав белков. Половина этих аминокислот – незаменимые (не синтезируются в организме человека), они поступают с пищей.
Получают кислотным гидролизом белков, либо из карбоновых кислот, воздействуя на них галогенном и, далее, аммиаком.

Аминокислоты организма
аминокислоты
Заменимые
Незаменимые
Синтезируются в организме человека
Не синтезируются в организме человека

Номенклатура
- Систематическая
- Рациональная
- Тривиальное

Номенклатура
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе.

Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Пример:

По рациональной номенклатуре положение аминогруппы указывается буквами греческого алфавита, начиная со второго атома углерода от - СООН: α, β, γ, δ, ε и т.д. Например:
α – аминопропионовая кислота

Изомерия
- Изомерия углеродного скелета;
- Изомерия положения функциональных групп;
- Межклассовая изомерия с нитросоединениями;
- Оптическая изомерия;
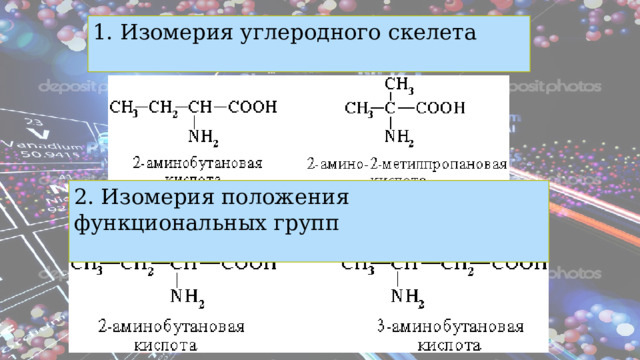
1. Изомерия углеродного скелета
2. Изомерия положения функциональных групп
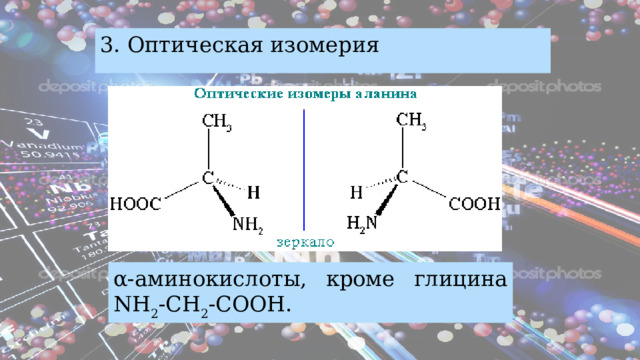
3. Оптическая изомерия
α-аминокислоты, кроме глицина NН 2 -CH 2 -COOH.

4. Межклассовая с нитросоединениями
(С ≥2 ), например; С 3 H 7 NO 2
1-нитропропан
2-аминопропановая кислота

Физические свойства
Аминокислоты
- бесцветные;
- кристаллические;
- хорошо растворимы в воде, но нерастворимы в эфире;
- в зависимости от R могут быть сладкими, горькими или безвкусными;
- обладают оптической активностью;
- плавятся с разложением при температуре выше 200º.

Химические свойства
- Наличие амино- и карбоксильной групп определяет двойственность химических свойств аминокислот.
- Амфотерность ( от греч. amphуteros – «и тот и другой») – способность некоторых веществ в зависимости от условий проявлять либо кислотные, либо основные свойства; амфотерные вещества иногда называют амфолитами.

Химические свойства
– СООН
– NH
- со щелочами
- с металлами
- со спиртами
ВЗАИМОДЕЙСТВИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП
- с сильными кислотами
- с галогено-водородами
- Образование внутренних солей
- Образование молекул белков
Аминокислота + Cu(OH) 2 синий раствор

ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты амфотерные органические соединения, для них характерны кислотно-основные свойства.
I. Общие свойства
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе:
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп.

2. Поликонденсация → образуются полипептиды (белки):
При взаимодействии двух α-аминокислот образуется дипептид .

3. Разложение → Амин + Углекислый газ:
NH 2 -CH 2 -COOH → NH 2 -CH 3 + CO 2 ↑

II. Свойства карбоксильной группы (кислотность)
1. С основаниями → образуются соли :
NH 2 -CH 2 -COO H + Na OH →
→ NH 2 -CH 2 -COONa + H 2 O
NH 2 -CH 2 -COONa - натриевая соль 2-аминоуксусной кислоты
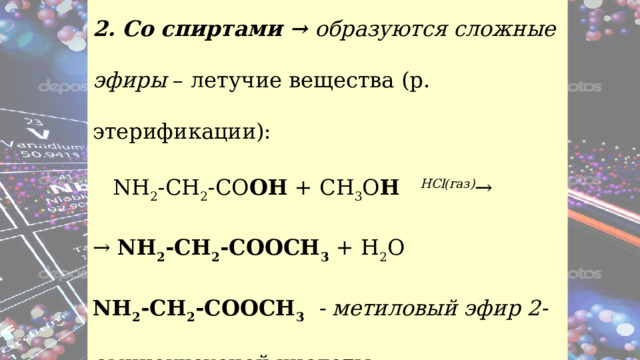
2. Со спиртами → образуются сложные эфиры – летучие вещества (р. этерификации):
NH 2 -CH 2 -CO OH + CH 3 O H HCl(газ) →
→ NH 2 -CH 2 -COOCH 3 + H 2 O
NH 2 -CH 2 -COOCH 3 - метиловый эфир 2- аминоуксусной кислоты

3. С аммиаком → образуются амиды:
NH 2 -CH(R)-CO OH + H -NH 2 →
→ NH 2 -CH(R)-CONH 2 + H 2 O

4. Практическое значение имеет внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона):
![III. Свойства аминогруппы (основность) 1. С сильными кислотами → соли: HOOC-CH 2 -NH 2 + HCl → → [HOOC-CH 2 -NH 3 ]Cl или HOOC-CH 2 NH 2 *HCl](https://fsd.multiurok.ru/html/2022/04/27/s_6269662281a32/img26.jpg)
III. Свойства аминогруппы (основность)
1. С сильными кислотами → соли:
HOOC-CH 2 -NH 2 + HCl →
→ [HOOC-CH 2 -NH 3 ]Cl
или HOOC-CH 2 NH 2 *HCl

2. С азотистой кислотой (подобно первичным аминам):
NH 2 -CH(R)-COOH + HNO 2 →
→ HO-CH(R)-COOH + N 2 ↑+ H 2 O
гидроксокислота
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка)
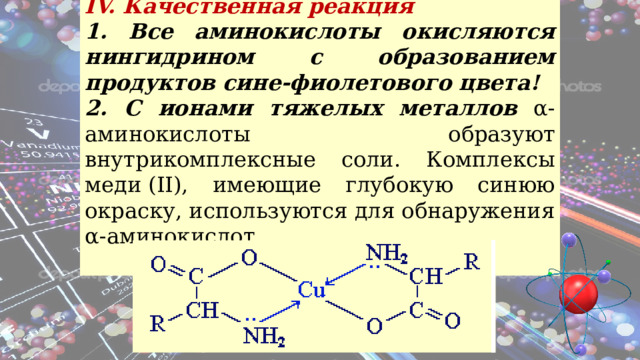
IV. Качественная реакция
1. Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета!
2. С ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.

Получение аминокислот
- Гидролиз белков под влиянием ферментов, кислот или щелочей.
- Действие аммиака на хлорзамещенные органические кислоты: CH 3 – CH(Cl) – COOH + NH 3 → CH 3 – CH(NH 2 ) – COOH + NH 4 Cl
- Действие цианистого аммония на оксосоединения (реакция Н.Д.Зелинского)
IV. Присоединение аммиака к непредельным кислотам
CH 2 = CH – COOH + 2NH 3 → H 2 N –CH 2 – CH 2 – COONH 4
V. Микробиологический синтез
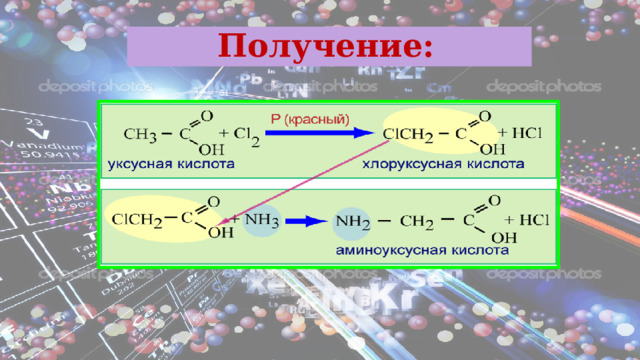
Получение:
1 . Гидролиз белков . Белок – полимер под действием воды распадается на мономеры - аминокислоты
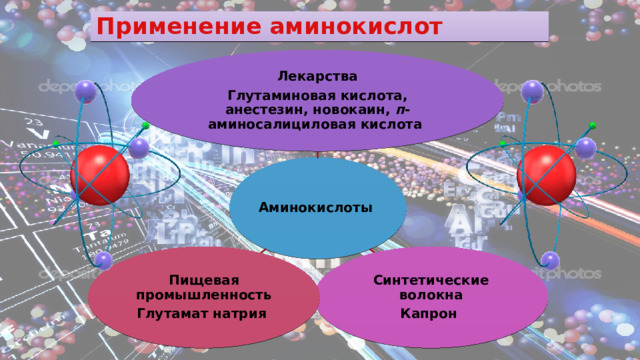
Применение аминокислот
Лекарства
Глутаминовая кислота, анестезин, новокаин, п -аминосалициловая кислота
Аминокислоты
Синтетические волокна
Пищевая промышленность
Капрон
Глутамат натрия

ПРИМЕНЕНИЕ
1) аминокислоты широко распространены в природе;
2) молекулы аминокислот – это те кирпичики, из которых построены все растительные и животные белки; аминокислоты, необходимые для построения белков организма, человек и животные получают в составе белков пищи;
3) аминокислоты прописываются при сильном истощении, после тяжелых операций;
4) их используют для питания больных;
5) аминокислоты необходимы в качестве лечебного средства при некоторых болезнях (например, глутаминовая кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты применяются в сельском хозяйстве для подкормки животных, что положительно влияет на их рост;
7) имеют техническое значение: аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна – капрон и энант.

































![III. Свойства аминогруппы (основность) 1. С сильными кислотами → соли: HOOC-CH 2 -NH 2 + HCl → → [HOOC-CH 2 -NH 3 ]Cl или HOOC-CH 2 NH 2 *HCl](https://fsd.multiurok.ru/html/2022/04/27/s_6269662281a32/img26.jpg)

























