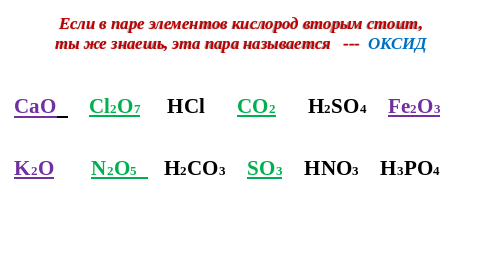
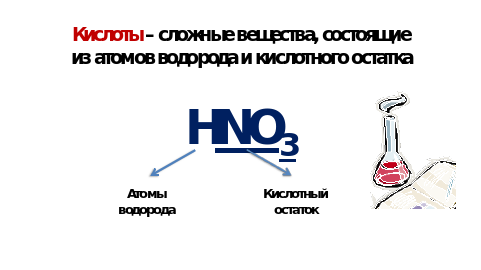
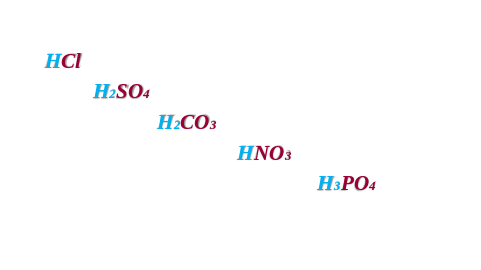| Мотивация. Эпиграф урока: «Ум заключается не только в знании, но и в умении прилагать знание на деле». Аристотель Предлагает учащимся вспомнить какие классы неорганических веществ им известны --Отгадайте загадку: Если в паре элементов кислород вторым стоит, ты же знаешь, эта пара называется …(ОКСИД) --На какие группы можно разделить оксиды? На экране задание (работа в парах): Из предложенных формул выберите оксиды и распределите их по группам: CaO, CI2O7, HCI, CO2, H2SO4 , Fe2O3, K2O, N2O5,H2CO3 , SO3, HNO3, H3PO4 Подводит учащихся к формулированию понятия кислоты. --Почему вы назвали не все вещества? Выпишите их формулы в тетрадь. Что между ними общего? Попробуем догадаться, как они называются. (Приложение 1.) На экране мы видим яблоки, лимоны, муравья, бутылочку с уксусом, щавель, крапиву. На столах –дольки мандаринов и яблок. --Что объединяет все это? Еще одна загадка: Кислый вкус они имеют, лакмус в них всегда краснеет, и опасны для работы эти жгучие … (КИСЛОТЫ) Формулирует тему и цель урока. |
Отвечают на вопросы, работают в парах - из предложенных формул выбирают оксиды.
Выписывают оставшиеся формулы, анализируют их состав, находят общие признаки. (наличие водорода). Обсуждают изображения на экране, пробуют фрукты, определяют вкус (кислый) и высказывают предположения о названии веществ, имеющих такие признаки
По загадке определяют перечень вопросов, на которые нужно найти ответы. Предлагают пути достижения поставленной цели урока, определяют ход деятельности на уроке. Записывают тему в тетрадь.
| ЛР-2 ПУД-2 ПУД-3 ПУД-4 РУД-1 РУД-4 КУД-2 КУД-3 |
| 1.Изучение нового материала. Состав кислот. --Предлагает учащимся дать определение понятию кислота исходя из формул
2.Классификация кислот. Названия кислот Используя текст учебника с.102,104 найдите признаки, по которым классифицируют кислоты, составьте схему, приведите примеры. Ознакомьтесь с названиями кислот
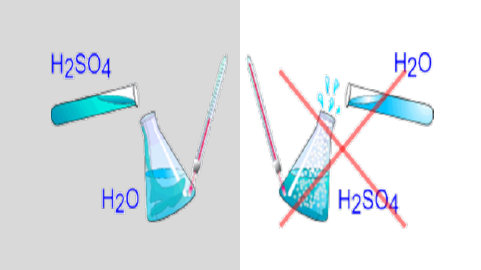
3. Изменение окраски индикаторов в кислой среде. Предлагает еще раз вернуться к последней загадке: --О каких еще признаках кислот в ней упоминается? Объясняет, что такое индикаторы, их виды и как с их помощью можно распознать кислоты. --Мотивирует к проведению исследования. Предлагает провести эксперимент. Проводит инструктаж по ТБ при работе с кислотами. При обращении с кислотами необходимо соблюдать правила безопасной работы: 1.Для приготовления растворов серной, азотной и других кислот необходимо их приливать к воде тонкой струей при непрерывном перемешивании, а не наоборот. Приливать воду в кислоту запрещается! 2.Разлитые кислоты необходимо немедленно засыпать песком, нейтрализовать, и только после этого проводить уборку. 3.При попадании на кожу или одежду кислоты, надо смыть ее большим количеством воды, а затем обработать 3-5% раствором питьевой соды или разбавленным раствором аммиака.
Организует обсуждение результатов эксперимента
Объясняет, почему кислоты называют жгучими и почему они могут вызвать ожоги. Понятие концентрации. Предлагает ознакомиться с текстом учебника: с. 104-106 | Проводят сравнение. Формулируют понятие кислоты. Записывают в тетрадь. Кислоты - это сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка.
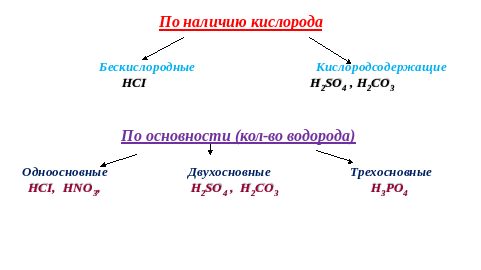
Индивидуально работают с учебником. В тетради учащихся должна появиться схема: По наличию кислорода  
Бескислородные Кислородсодержащие HCI, HNO3, H2SO4 , H2CO3 По основности (кол-во водорода)   
Одноосновные Двухосновные Трехосновные HCI, HNO3, H2SO4 , H2CO3 H3PO4
Возникает вопрос: что такое лакмус? И почему кислоты опасные? Ведь они входят в состав всеми любимых фруктов?!
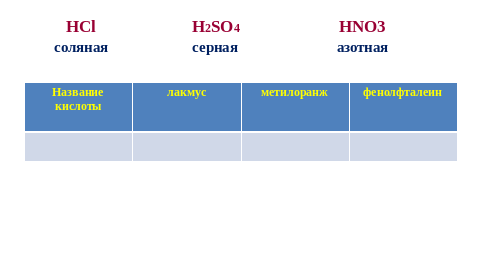
Работают в группах по инструктивным картам. Каждая группа изучает действие разных кислот на индикаторы: 1 группа – соляная кислота 2 группа – серная кислота 3 группа – азотная кислота. Данные заносят в таблицу: | Название кислоты | Лакмус | Метилоранж | Фенолфталеин | |
|
|
|
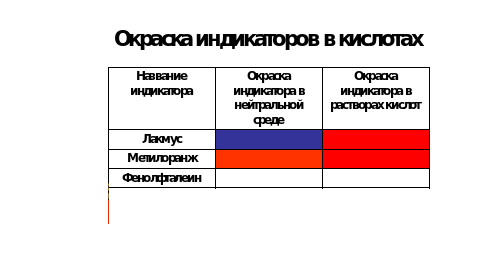
| Делают вывод: 1.Независимо от вида кислоты, индикаторы изменяют свой цвет одинаково, а это означает, что все кислоты обладают сходными свойствами. 2. Для определения кислот можно использовать лакмус или метиловый оранжевый.
Обсуждают меры предосторожности при работе с кислотами. Запомнить: при разбавлении кислот водой кислоту лить в воду!!! Объясняют почему.
| ЛР-2 ПУД-1 ПУД-2 ПУД-5 ПУД-6 КУД-2 КУД-3 РУД-4 ПР-1 ПР-2
|
| - Мы завершили наше исследование. Назовите тему, цель и задачи нашего исследования. - Достигли ли мы поставленной цели? - Посовещайтесь в группах, сделайте общий вывод по теме нашего исследования. - У кого остались вопросы?
Проверьте себя. Задания на экране 1.«Верны ли утверждения?». Если вы согласны с утверждением ставьте «+», если нет - «–». +1. Кислоты – это сложные вещества, состоящие из H и кислотного остатка. −2.Кислота, формула которой H2SO4 – это одноосновная кислородосодержащая кислота. −3.В кислой среде фенолфталеин меняет окраску на красный. +4.Эти кислоты: H2S H2CO3 H2SiO3 -двухосновные +5. Среди веществ, формулы которых СО2,HCl,СuCl2 HNO3, H3PO4 - три кислоты 2.Дать описание азотной кислоты по плану в учебнике: с. 107. Самопроверка. Слайд - Проверим. Оценим выполнение работы. |
Совещаются и делают вывод
Осуществляют самопроверку заданий. Оценивают результаты своей работы. | ЛР-1 ПУД-4 КУД-2 КУД-3 РУД-3 РУД-4 ПР-3 |