Урок химии в 8 классе
Урок №________
Дата:__________
Тема урока: «Состав солей и их названия. Классификация солей»
Цель урока: сформировать понятие о солях и их классификации, физических свойствах; закрепить понятие валентность.
Задачи урока
Образовательные: познакомить с классом неорганических веществ «Соли»; рассмотреть состав и название солей; научить составлять формулы солей.
Воспитательные: показать значимость солей; совершенствовать навыки групповой и индивидуальной работы.
Развивающие: развивать умение анализировать и обобщать данные, классифицировать вещества, составлять химические формулы и читать их.
Оборудование: презентация, учебник «Химия» 8 класс Г.Е.Рудзитис, пробирки, образцы солей, стеклянные палочки.
Реактивы: хлорид натрия, карбонат кальция (мел), медный купорос, хлорид натрия, вода.
Ход урока
| «Знания! Великое дело!
Что же составляет величие
Человека, как не знания!» |
| А.С.Пушкин |
1. Организационный момент.
2. Актуализация опорных знаний.
Сегодня мы отправимся с вами в путешествие в новый город, который находится в государстве под названием «Неорганические вещества». Давайте вспомним, какие государства находятся на карте данного государства и уже посещены нами? (слайд 2).
Прежде, чем мы отправимся в путешествие, нам необходимо пройти таможенный контроль и ответить на несколько вопросов (слайд 3).
Какие вещества называются оксидами?
Как классифицируют оксиды?
Какие вещества называются кислотами?
Как определить валентность кислотного остатка?
На какие группы делят кислоты?
Какие вещества относят к классу оснований?
Как классифицируют основания?
(слайд 4) Задание: Необходимо выписать вещества соответствующего класса, дать им названия и классифицировать:
CO, Fe(OH)3, H2SO4, CaO, NaOH, CuSO4, HCl, CO2, HNO3, Cu(OH)2, KOH, Al2O3, Fe2(SO4)3, H2CO3, NaCl
1 ряд – оксиды,
2 ряд – кислоты,
3 ряд – основания.
Проверяется выполнение. Отмечаются формулы веществ, которые не были отнесены ни к одному из классов.
3. Изучение нового материала
А теперь мы отправляемся в путь. Но название города, в который мы отправляемся, вы должны определить по моему небольшому рассказу, который повествует об одном из жителей этого города. Без этого вещества не могут жить ни люди, ни звери. Взрослому человеку для поддержания жизнедеятельности необходимо получать 8-10 г. этого вещества. Оно содержится в слюне, наличие его в крови обеспечивает необходимое осмотическое давление. Считают, например, что массовая гибель войска Наполеона, особенно раненных солдат, при отступлении была вызвана недостатком этого вещества. Некоторые народы Африки платили когда-то за это вещество золотым песком. Римские легионеры часов Цезаря получали часть платы этим веществом. Т.е. оно заменяло во многих государствах деньги. И до сих пор, для многих народов – это символ гостеприимства.
О каком веществе идет речь? (дети высказывают версии).
Ученые подсчитали, что все жители нашей планеты в год используют приблизительно 17 млн. тонн хлорида натрия. Для перевозки такой массы соли понадобится состав длиной приблизительно 5000 км.
Действительно речь идет об обычной поваренной соли – хлориде натрия.
К какому классу неорганических веществ относится данное вещество? (Солей)
Тема урока «Состав солей и их названия. Классификация солей» (записывают в тетрадь) (слайд 5).
Определим цели урока (обучающиеся формулируют цели).
Мы с вами оказались в городе под названием «Соли». Название «Соль» происходит от латинского слова «sol» - «солнце». Оседание соли под действием солнечных лучей в древние времена объясняли как рождение этого вещества под влиянием солнечной энергии. «Соль» буквально означает «солнечное вещество». Раньше так называли только хлорид натрия, а теперь целый класс веществ.
В путешествии нам будут помогать маршрутные карты (приложение 1).
А теперь вернемся к веществам, которые не были отнесены ни к одному из изученных ранее классов веществ:
слайд 6: CuSO4, Fe2(SO4)3, NaCl
Это все жители нового города. Что у них общего?
Беседа подводится к выводу определения класса «Соли».
Соли – сложные вещества, состоящие из атомов металла и кислотного остатка.
Определение фиксируется в маршрутном листе.
В городе есть кланы (семейства) солей. Каждое семейство отличает индивидуальность:
- нормальные (средние);
- кислые;
-основные;
-двойные;
-смешанные;
-комплексные.
Сегодня мы с вами познакомимся с тремя семействами: Нормальные, Кислые, Основные.
Слайд 8:
Посмотрите на представителей каждого из семейств. Сделайте вывод о том, чем же отличаются они друг от друга:
Нормальные - CuSO4, Fe2(SO4)3, NaCl
Кислые - BaHPO4, NaHSO4, Ba(H2PO4)2
Основные - Ca(OH)Cl, Pb(OH)NO3, Аl(OH)SO4
Что общего?
Чем отличаются?
Поиграем в «крестики-нолики» (слайд 9):
Выигрышный путь составляет соответствующая группа солей:
| HNO3 | NaOH | Na2CO3 |
| CuCl2 | Al2(CO3)3 | Na3PO4 |
| Cu(OH)2 | Fe(NO3)2 | Ba(OH)2 |
а) нормальные (средние) соли
| KHCO3 | Al2(CO3)3 | H2SO3 |
| KNO3 | CaHPO4 | H2CO3 |
| Ca(OH)2 | Mg(OH)Cl | NaHSO4 |
б) кислые соли
| H2SO4 | NaCl | Zn(OH)Br |
| AgNO3 | Fe(OH)SO4 | Ca(OH)2 |
| Ca(OH)Cl | CuCl2 | Na2CO3 |
в) основные соли
У каждого жителя планету есть имя. У жителей города «Соли» также есть имена. Как же их назвать?!
Названия солей строятся следующим образом:
(валентность металла),
если переменная!!!
Название кислотного остатка
Название металла в р.п.
+ +
Учитель приводит по два примера – название соли, относящиеся к разным группам солей (средний, кислые, основные)
(работа в парах) У вас на столах есть поле №1 (Приложение 2). Поиграем в лото. Ваша задача закрыть за 3 минуты как можно больше клеточек, написав на «фишках» названия соответствующих солей. Для работы используем таблицы «Кислоты и их соли», выданные ранее или информацию со слайда. Проверяют по слайду №11.
Обратное действие – у нас есть название соли, необходимо составить формулу соли (учитель показывает два примера). Поле №2 (приложение 3). Работают 3 минуты. Проверяют по слайду №12.
Нужно сказать, что для многих солей используются не только международные, а и традиционные названия:
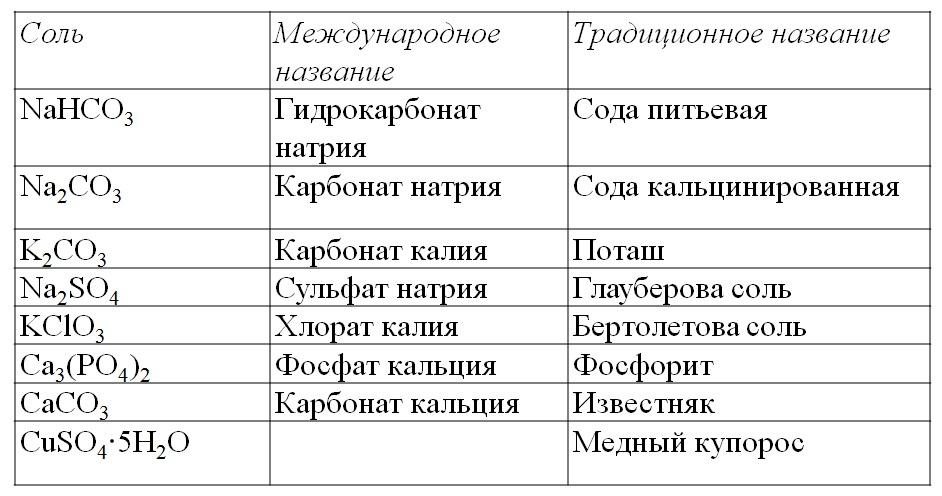
Учитель рассказывает о некоторых представителях, обращает внимание на последнюю соль (кристаллогидрат).
Ну а теперь попробуем раскрыть тайну внешнего вида жителей города. У вас на столах находятся подписанные пробирки с образцами солей. Внимательно рассмотрите выданные вам образцы. Обратите внимание на агрегатное состояние, цвет и запах каждого вещества. Исследуйте их растворимость в воде. Заполните соответствующую таблицу:
| Название соли | Состав (формула) | Физические свойства |
| Агрегатное состояние | Цвет | Запах | Растворимость в воде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4. Закрепление изученного.
Ребята, пока мы знакомились с солями, кто-то пробрался в город.
Игра «Третий – лишний» (слайд 11):
CaCl2, AgNO3, HCl
CuO, K2S, FePO4
MgCl2, Mg, CuSO4
NaNO3, ZnSO4, H3PO4
Наше путешествие на сегодня закончено и пусть всегда в исследовании вам сопутствует успех.
5. Рефлексия и подведение итогов.
- Что нового узнали на уроке?
- Что было интересного?
- Что было сложным?
-
6. Выставление отметок.
7. Домашнее задание §_____, упражнения _______
(на оценку «3» любые 3 задания
на оценку «4», «5» - 4 задания)
Приложение 1
Маршрутный лист ___________________________________
(Ф.И. учащегося)
Дата:_____________________
Тема урока:_______________________________________________________________
__________________________________________________________________________
Задание: Выписать вещества соответствующего класса, дать им названия и классифицировать:
CO, Fe(OH)3, H2SO4, CaO, NaOH, CuSO4, HCl, CO2, HNO3, Cu(OH)2, KOH, Al2O3, Fe2(SO4)3, H2CO3, NaCl
1 ряд – оксиды, 2 ряд – кислоты, 3 ряд – основания.
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
n m
Ме m (К/О)n
СОЛИ - _______________________________________________________________________________
_______________________________________________________________________________________
Классификация солей:

Задание: «Крестики-нолики». Выигрышный путь составляет соответствующая группа солей:
| HNO3 | NaOH | Na2CO3 | | CuCl2 | Al2(CO3)3 | Na3PO4 | | Cu(OH)2 | Fe(NO3)2 | Ba(OH)2 | KHCO3 | Al2(CO3)3 | H2SO3 |
| KNO3 | CaHPO4 | H2CO3 |
| Ca(OH)2 | Mg(OH)Cl | NaHSO4 |
а) нормальные (средние) соли б) кислые соли
| H2SO4 | NaCl | Zn(OH)Br |
| AgNO3 | Fe(OH)SO4 | Ca(OH)2 |
| Ca(OH)Cl | CuCl2 | Na2CO3 |
в) основные соли
Названия для средней соли -
название кислотного остатка + название металла + указываем валентность для металла с
переменной валентностью
Na2SO4- _________________________________________________________________,
CuSO4- __________________________________________________________________.
Карбонат кальция -______________, хлорид железа (III) - _____________________

Физические свойства солей
Задание: изучите физические свойства солей и заполните таблицу
| Название соли | Состав (формула) | Физические свойства |
| Агрегатное состояние | Цвет | Запах | Растворимость в воде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вывод:_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задание: Игра «Третий – лишний»:
CaCl2, AgNO3, HCl
CuO, K2S, FePO4
MgCl2, Mg, CuSO4
NaNO3, ZnSO4, H3PO4
Домашнее задание:__________________________________________________________
Приложение 2
| AgNO3 | CuSO4 | Na2CO3 |
| FeCl3 | KBr | AlPO4 |
| Cr2(SO4)3 | Ba(NO2)2 | NaCl |
Приложение 3
| сульфат меди (II) | карбонат натрия | нитрат алюминия |
| хлорид железа (II) | бромид кальция | ортофосфат кальция |
| сульфит бария | сульфид магния | сульфат железа (III) |

























