Просмотр содержимого документа
«Типы химических реакций»

Типы химических реакций
Презентация к уроку химии в 8 классе
Подготовил учитель химии высшей категории Коровин С.И.
п. Чёбаково 2012 г.

Выполните задание:
Из перечисленных ниже явлений выберите химические явления. Обоснуйте свои ответы.
- Образование капель росы на листьях растений ночью
- Растворение сахара в воде
- Горение газа в газовой плите
- Получение зелёной краски смешиванием синей и жёлтой
- Шипение пищевой соды при добавлении к ней уксуса
- Образование накипи на стенках чайника

Всё многообразие химических реакций учёные для удобства их изучения классифицируют на различные типы. Существует множество классификаций. Мы сегодня познакомимся с классификацией химических реакций по
количеству и качеству исходных веществ и продуктов реакции
1. Реакции соединения
Химические реакции, при которых два или более веществ взаимодействуют между собой, при этом образуется одно более сложное вещество называются реакциями соединения
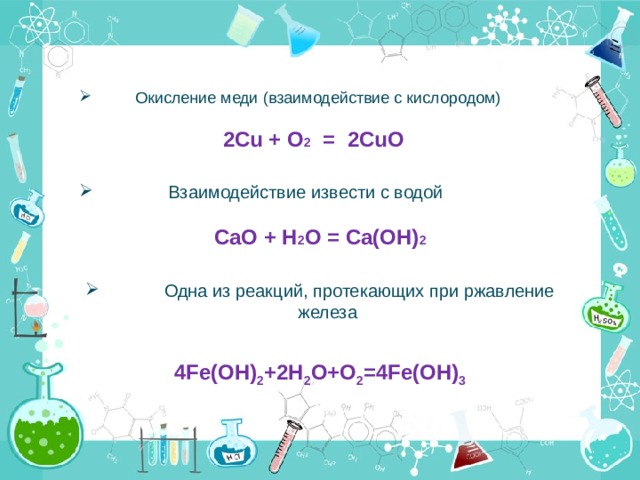
- Окисление меди (взаимодействие с кислородом)
2Cu + O 2 = 2CuO
- Взаимодействие извести с водой
CaO + H 2 O = Ca(OH) 2
- Одна из реакций, протекающих при ржавление железа
4Fe(OH) 2 +2H 2 O+O 2 =4Fe(OH) 3

2. Реакции разложения
Химические реакции, при которых одно сложное вещество разлагается на два или несколько более простых веществ называются реакциями разложения
- Разложение воды под действием электрического тока
2H 2 O = 2H 2 + O 2 -Q
- Разложение известняка при нагревании
CaCO 3 = CaO + CO 2 - Q
- Разложение хлорида аммония
NH 4 Cl = NH 3 + HCl -Q

3. Реакции замещения
Химические реакции между просым и сложным веществами при которых атомы, образующие простое вещество замещают некоторые атомы молекул сложного вещества называются реакциями замещения
- Серебрение медной проволоки
Cu + 2AgNO 3 = Ag + Cu(NO 3 ) 2
- Взаимодействие цинка с соляной кислотой
Zn + 2HCl = ZnCl 2 + H 2
- Восстановление меди из её оксида
CuO + H 2 = Cu + H 2 O

4. Реакции обмена
Химические реакции между двумя сложными веществами при которых молекулы этих веществ обмениваются своими составными частями называются реакциями обмена
- Взаимодействие мела (известняк) с соляной кислотой
CaCO 3 + 2HCl = CaCl 2 + H 2 CO 3
- Взаимодействие пищевой соды с уксусной кислотой
NaHCO 3 + CH 3 COOH = CH 3 COONa + H 2 CO 3
- Образование осадка гидроксида меди (II)
CuSO 4 + 2NaOH = Na 2 SO 4 + Cu(OH) 2 ↓
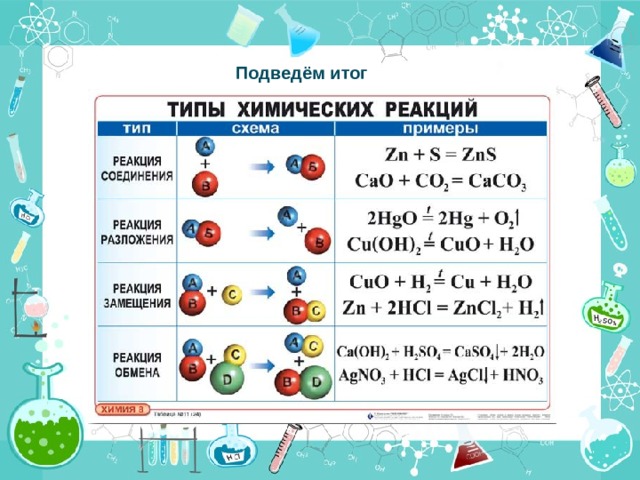
Подведём итог

Спасибо за активную работу на уроке

При подготовке презентации были использованы рисунки с сайта: http://alhimikov.net/gallery/


































