
Теория химического строения органических веществ А.М.Бутлерова

Содержание
- Исторические предпосылки создания теории строения вещества
- Основные положения теории строения органических соединений А.М.Бутлерова, ее значение для развития органической химии
- Валентные состояния атомов углерода в органических веществах
- Пространственное расположение углеродных цепей и колец
- Изомерия. Виды изомерии. Язык современной химии
- Общие закономерности реакций органической химии. Гомолитический и гетеролитический разрыв ковалентных связей
- Основные типы органических реакций

Исторические предпосылки создания теории строения вещества
Фридрих Вёлер (Германия) синтезировал мочевину (1828 г).
Это было первое в истории человечества получение органического вещества «in vitro», то есть «в стекле».
Только после этого органические вещества стали пытаться получать лабораторным синтезом и добивались успехов.
Выход

Марселен Бертло (Франция) синтезировал муравьиную кислоту (1862), жироподобные вещества (1854), этиловый спирт (1854);
Выход

Уильям Генри Перкин (Англия) впервые синтезировал синтетические красители (1868)
Выход

Александр Михайлович Бутлеров (Россия) — синтез сахароподобных веществ (1861).
Таким образом, шло накопление экспериментального материала; это происходило очень быстро, но бессистемно. Ученые не могли объяснить суть проводимых реакций, причины тех или иных свойств веществ, не было единых стандартов в написании формул...
Выход

Теория строения органических соединений не только помогла систематизировать уже полученную информацию, но и дала возможность вести целенаправленные исследования в будущем.
1853 г - Эдвард Франкленд заложил основы теории валентности.
1857 г - Август Кекуле и Адольф Кольбе установили четырехвалентность атомов углерода в органических молекулах, а также предположил наличие в их основе углеродных цепей.
1860 г - в городе Карлсруэ (Германия) на съезде химиков были определены и разграничены понятия «атом», «молекула», «простое вещество», «сложное вещество» и т. д.
Выход

Основные положения Теории строения органических соединений
19 сентября 1861 г Шпейер
- Атомы в молекулах соединяются согласно их валентности

веществ зависят не только
от их качественного и
количественного состава, но
и от того, в каком порядке
соединены атомы в молекулах,
т.е. от химического строения

- Атомы в молекулах взаимно влияют друг на друга

- Свойства органических
- Свойства органических
- Свойства органических
- Свойства органических
- Свойства органических
веществ зависят от их
строения. Зная строение
вещества, можно
определить его свойства
- веществ зависят от их строения. Зная строение вещества, можно определить его свойства
- веществ зависят от их строения. Зная строение вещества, можно определить его свойства
- веществ зависят от их строения. Зная строение вещества, можно определить его свойства
- веществ зависят от их строения. Зная строение вещества, можно определить его свойства
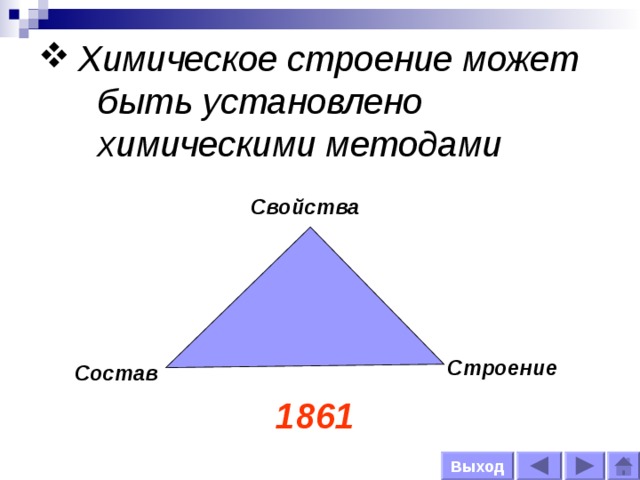
- Химическое строение может быть установлено химическими методами
Свойства
Строение
Состав
1861
Выход

Основные положения Теории строения органических соединений
19 сентября 1861 г Шпейер
- Атомы в молекулах соединяются согласно их валентности
- Свойства органических веществ зависят не только от их качественного и количественного состава, но и от того, в каком порядке соединены атомы в молекулах, т.е. от химического строения
- Атомы в молекулах взаимно влияют друг на друга
- Свойства органических веществ зависят от их строения. Зная строение вещества, можно определить его свойства
Выход
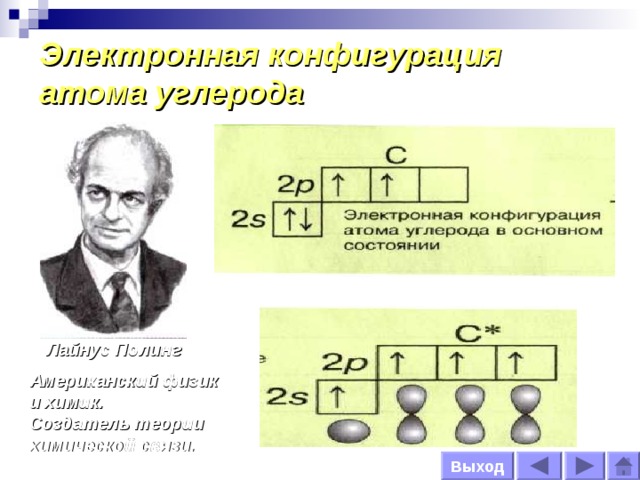
Электронная конфигурация атома углерода
Лайнус Полинг
Американский физик
и химик.
Создатель теории химической связи.
Выход
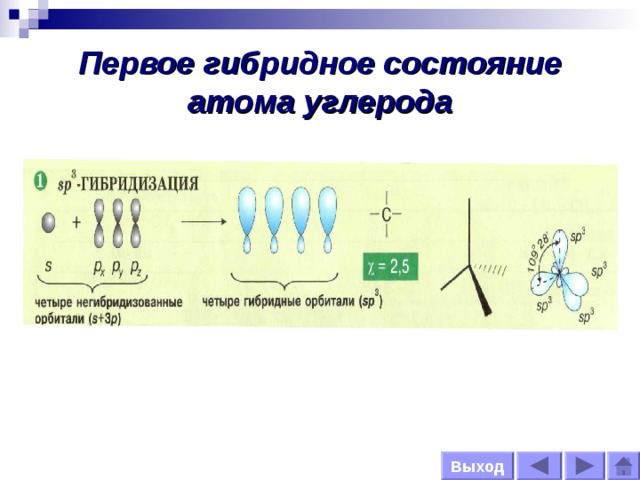
Первое гибридное состояние атома углерода
Выход
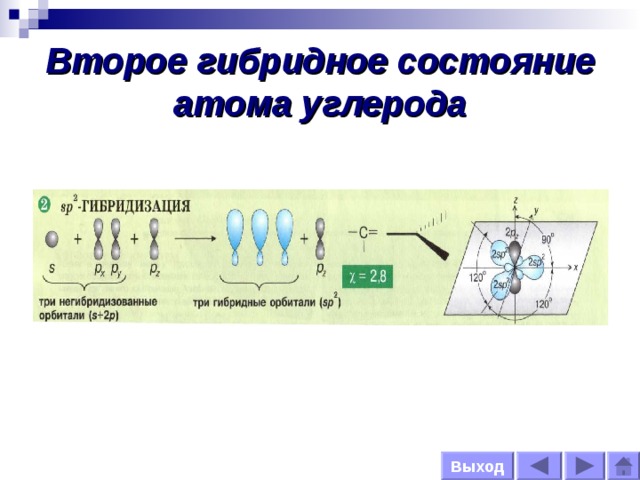
Второе гибридное состояние атома углерода
Выход
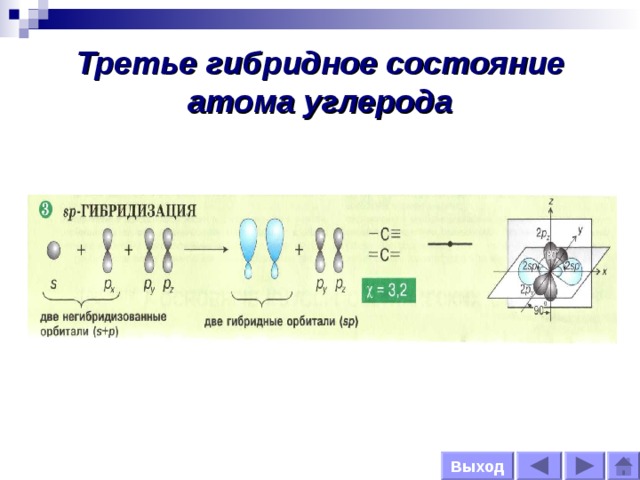
Третье гибридное состояние атома углерода
Выход
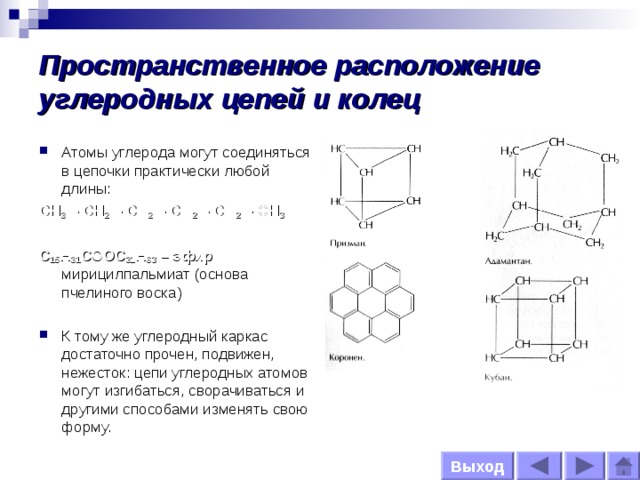
Пространственное расположение углеродных цепей и колец
- Атомы углерода могут соединяться в цепочки практически любой длины:
СН 3 – СН 2 – СН 2 – СН 2 – СН 2 – СН 3
С 15 Н 31 СООС 31 Н 63 – эфир мирицилпальмиат (основа пчелиного воска)
- К тому же углеродный каркас достаточно прочен, подвижен, нежесток: цепи углеродных атомов могут изгибаться, сворачиваться и другими способами изменять свою форму.
Выход

Изомерия – это явление существования изомеров. Изомеры – это вещества, которые имеют одинаковый состав, но разное строение молекул и различные свойства.
- Изомеры имеют одинаковую эмпирическую формулу и разные структурные формулы.
- С увеличением числа атомов углерода в молекуле число изомеров резко возрастает; например: С 4 Н 10 – 2 изомера, С 10 Н 22 – 75 изомеров.
Выход

Типы изомерии
Выход

Виды структурной изомерии
С Н 3 – С Н 2 – С Н 2 – С Н 3 С 4 Н 10 С Н 3 – С Н – С Н 3
С Н 3
- Изомерия положения кратной связи
СН 3 – СН = СН – СН 3 С 4 Н 8 СН 2 = СН – СН 2 – СН 3
- Изомерия положения функциональной
группы
СН 3 – СН 2 – СН 2 – ОН СН 3 – СН – СН 3
ОН
С 3 Н 7 ОН
Выход
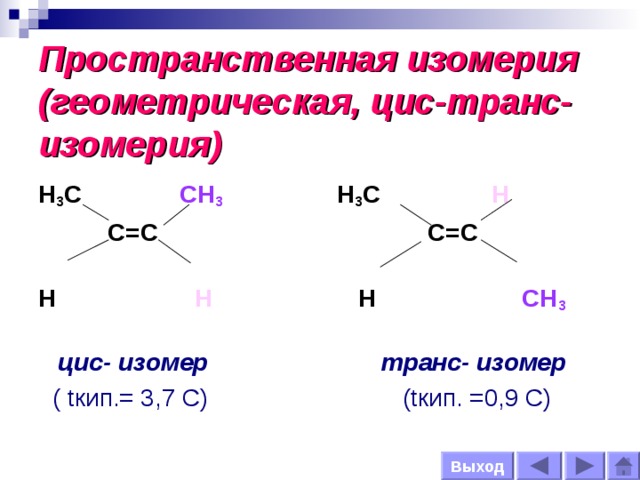
Пространственная изомерия (геометрическая, цис-транс-изомерия)
Н 3 С СН 3 Н 3 С Н
С=С С=С
Н Н Н СН 3
цис- изомер транс- изомер
( tкип.= 3,7 С) (tкип. =0,9 С)
Выход
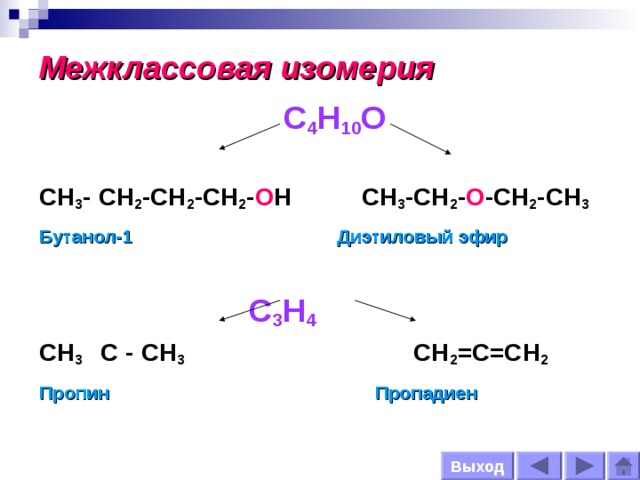
Межклассовая изомерия
С 4 Н 10 О
СН 3 - СН 2 -СН 2 -СН 2 - О Н СН 3 -СН 2 - О -СН 2 -СН 3
Бутанол-1 Диэтиловый эфир
С 3 Н 4
СН 3 С - СН 3 СН 2 =С=СН 2
Пропин Пропадиен
Выход

Язык современной химии
Номенклатура – это система названий.
Существует несколько номенклатур. Наиболее распространена номенклатура выработанная Международным союзом теоретической и прикладной химии – сокращенно IUPAC .
Правила составления названия веществ:
- Выбрать самую длинную цепь углеродных атомов;
- Пронумеровать атомы в главной цепи так, чтобы сумма цифр в названии была наименьшей;
- Заместители (боковые цепи) перечислить в алфавитном порядке.
Выход

Назвать вещество:
CH 3 CH 2 – CH 3
1 2 3 4 5 6 7
CH 3 - CH - CH - CH 2 - CH - CH 2 – CH 3
CH 3
- Главная цепь - гептан (так как 7 атомов углерода в основной цепи);
- Боковые ответвления – радикалы ( метил –СН 3 при втором и третьем атоме углерода, этил – С 2 Н 5 при пятом атоме углерода);
- Получаем название вещества:
2,3 – диметил – 5 - этил гептан
Выход
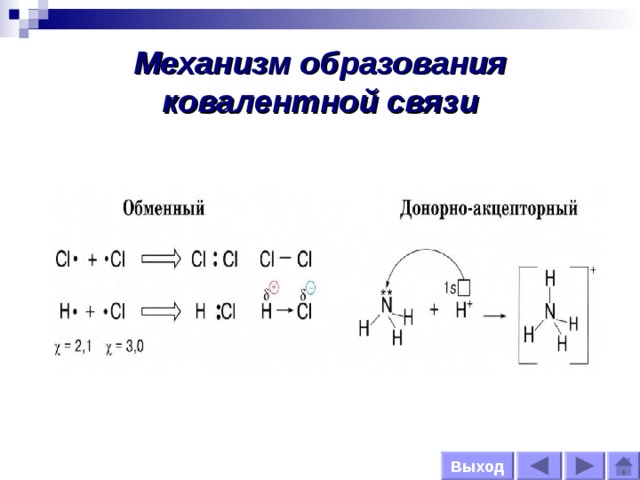
Механизм образования ковалентной связи
Выход

Механизм разрыва (диссоциации) ковалентной связи
Выход
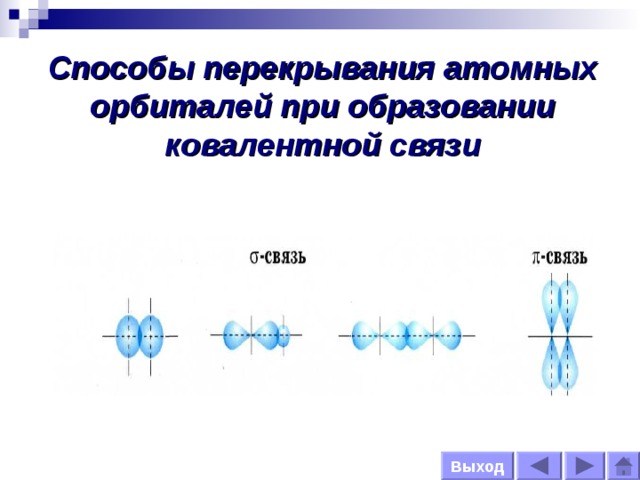
Способы перекрывания атомных орбиталей при образовании ковалентной связи
Выход

Основные типы органических реакций
Реакции замещения
Выход
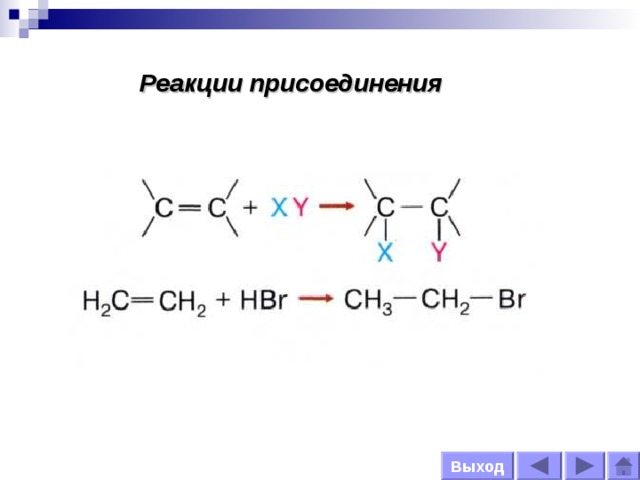
Реакции присоединения
Выход
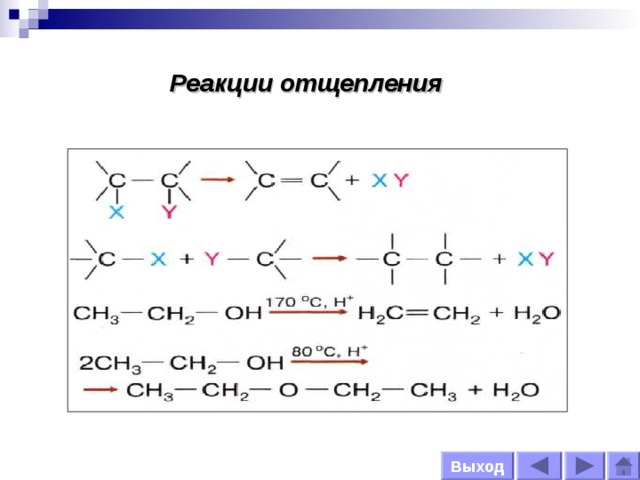
Реакции отщепления
Выход

- Презентация составлена для поддержки курса лекций по теме «Теория химического строения органических веществ А.М.Бутлерова»
- Составитель: Просвирякова О.Л., учитель химии Городокской средней школы
Выход
























































