
ОКСИДЫ: КЛАССИФИКАЦИЯ, СВОЙСТВА
Презентация к уроку химии
для 8 класса
Учитель химии МБОУ СШ № 16
г. Новый Уренгой
Батырова Раиля Бадртдиновна

Цели урока
- Сформировать представления об оксидах, их составе и классификации.
- Выяснить различия и сходства между кислотными и основными оксидами.
- Выяснить основные свойства оксидов.
- Закрепить умения по составлению уравнений химических реакций.

СОСТАВЬТЕ МОЛЕКУЛЯРНЫЕ И ИОННЫЕ УРАВНЕНИЯ
I вариант
II вариант
1. соляная к-та + алюминий →
2. серная к-та + гидроксид железа(III) →
3. гидроксид натрия + хлорид магния →
2. фосфорная к-та + гидроксид натрия →
3. гидрокид бария + сульфат натрия →

Распорядилась так природа,
Что окислитель-кислород
Давным - давно и год за годом
Легко оксиды создает.
А что относится к оксидам?
Обыкновенная вода.
Оксидов очень много видов:
Речной песок, слюда, руда.
В оксидах разберись однажды
В самом составе вещества:
Есть кислород в оксиде каждом,
А элементов только два.

ОКСИДЫ –
это сложные вещества, состоящие из двух химических элементов, один из которых – кислород в степени окисления - 2
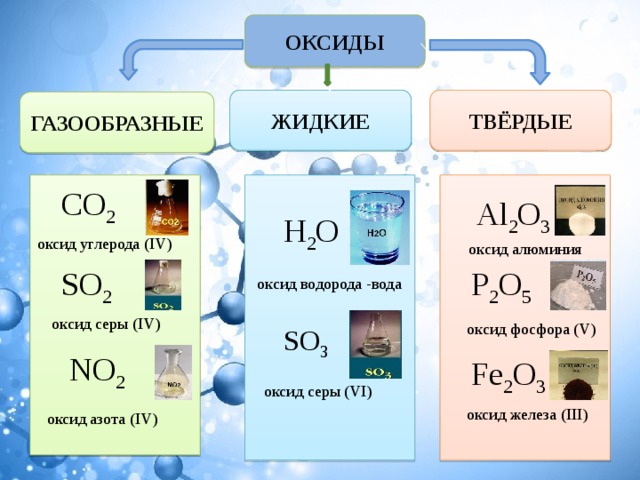
ОКСИДЫ
ЖИДКИЕ
ТВЁРДЫЕ
ГАЗООБРАЗНЫЕ
CO 2
Al 2 O 3
H 2 O
оксид углерода (IV)
оксид алюминия
SO 2
P 2 O 5
оксид водорода -вода
оксид серы (IV)
оксид фосфора (V)
SO 3
NO 2
Fe 2 O 3
оксид серы (VI)
оксид железа (III)
оксид азота (IV)
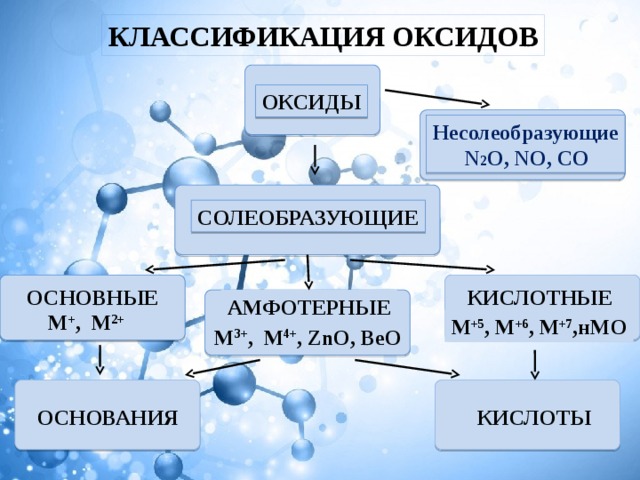
КЛАССИФИКАЦИЯ ОКСИДОВ
ОКСИДЫ
Несолеобразующие
N 2 O, NO, CO
СОЛЕОБРАЗУЮЩИЕ
КИСЛОТНЫЕ
ОСНОВНЫЕ
АМФОТЕРНЫЕ
М + , М 2+
М +5 , М +6 , M +7 ,нМО
М 3+ , М 4+ , ZnO, BeO
ОСНОВАНИЯ
КИСЛОТЫ
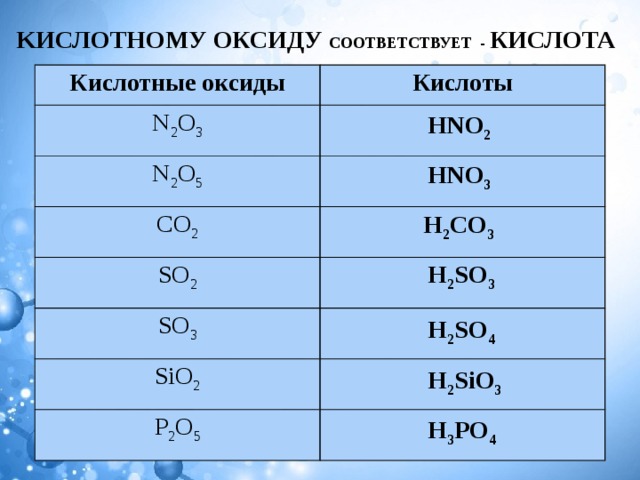
KИСЛОТНОМУ ОКСИДУ СООТВЕТСТВУЕТ - КИСЛОТА
Кислотные оксиды
Кислоты
N 2 O 3
N 2 O 5
СO 2
SO 2
SO 3
SiO 2
P 2 O 5
HNО 2
HNО 3
H 2 СO 3
H 2 SO 3
H 2 SO 4
H 2 SiO 3
H 3 PO 4

ОКСИДЫ – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород в степени окисления - 2
ОСНОВНЫЕ ОКСИДЫ
- это оксиды, которым соответствуют основания .
К основным оксидам относятся
оксиды металлов
IA и IIA групп
(Na 2 O, CaO)
и оксиды металлов
побочных подгрупп
со степенью окисления +1,+2
(Ag 2 O, FeO)
(кроме: ZnO и BeO)

ОКСИДЫ – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород в степени окисления - 2
КИСЛОТНЫЕ ОКСИДЫ
- это оксиды, которым соответствуют кислоты .
К кислотным оксидам относятся
оксиды неметаллов
(SO 2 , CO 2 , P 2 O 5 , Cl 2 O 7 ,)
и оксиды металлов
побочных подгрупп
со степенью окисления
+5,+6, +7
(CrO 3 , Mn 2 O 7 )

ОКСИДЫ – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород в степени окисления - 2
АМФОТЕРНЫЕ
ОКСИДЫ
-это оксиды, которым соответствуют гидроксиды , проявляющие свойства как оснований , так и кислот .
Амфотерные оксиды образуют металлы со степенью окисления
+2, +3, +4
ZnO, BeO,
Al 2 O 3 , Fe 2 O 3 ,
MnO 2

ОКСИДЫ – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород в степени окисления - 2
НЕСОЛЕОБРАЗУЮЩИЕ
ОКСИДЫ
– это оксиды
безразличные к кислотам и основаниям.
К ним относятся
оксиды неметаллов
со степенью окисления +1,+2
N 2 O – оксид азота (I),
NO - оксид азота (II),
CO - оксид углерода (II)

ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
ОСНОВНЫЕ ОКСИДЫ
КИСЛОТНЫЕ ОКСИДЫ
ВЗАИМОДЕЙСТВИЕ С ВОДОЙ
МеО + Н 2 О→ МеОН (щелочь)
неМеО + Н 2 О→ НАс (кислота)
Na 2 O + H 2 O = 2NaOH
Р 2 O 5 + 3H 2 O = 2H 3 РO 4
ОСНОВНОЙ ОКСИД + КИСЛОТНЫЙ ОКСИД = СОЛЬ
МеО + неМеО→ соль
CaO + СO 2 = CaСO 3
ОКСНОВНЫЙ ОКСИД+ КИСЛОТА
КИСЛОТНЫЙ ОКСИД +ЩЕЛОЧЬ
→ СОЛЬ +H 2 O
→ СОЛЬ +H 2 O
МеО + кислота→ соль + Н 2 О
неМеО+ щелочь→ соль + Н 2 О
3Na 2 O + 2H 3 PO 4 = 2Na 3 PO 4 + 3H 2 O
SO 3 +2NaOH→ Na 2 SO 4 + Н 2 О
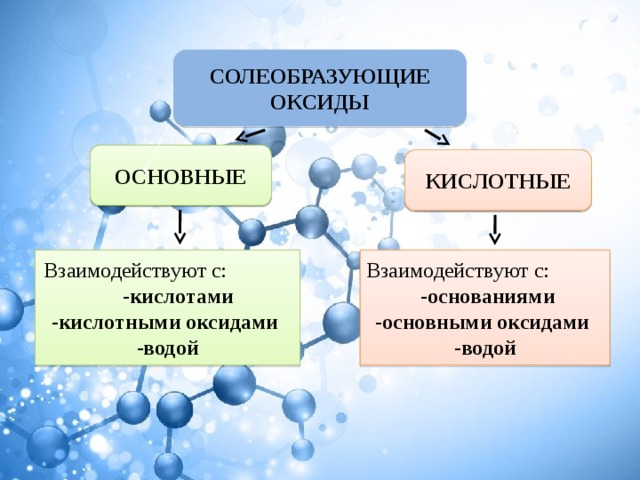
СОЛЕОБРАЗУЮЩИЕ ОКСИДЫ
ОСНОВНЫЕ
КИСЛОТНЫЕ
Взаимодействуют с:
Взаимодействуют с: - кислотами
- основаниями
-кислотными оксидами
-основными оксидами
-водой
-водой

Из перечня формул выпишите отдельно формулы основных , амфотерных и кислотных оксидов и дайте им названия
SO 3 , MnO 2 , Na 2 O, N 2 O 5 , CaO,
CrO 3 , Ag 2 O, Al 2 O 3 , Mn 2 O 7 ,
ZnO, FeO, Cu 2 O, Fe 2 O 3
ОСНОВНЫЙ
АМФОТЕРНЫЙ
КИСЛОТНЫЙ

Запишите уравнения характерных реакций для следующих оксидов:
I вариант
II вариант
SO 2
СаO






































