Zn + H2SO4 = ZnSO4 + H2
2H 2 + O 2 = 2 H 2 O
8 класс
«Типы химических реакций»
Бозаджи Н.М.,
преподаватель химии,
высшая дид .категория

В результате изучения темы ,
вы будете способны:
- Характеризовать признаки хим.реакций и условия необходимые для осуществления химической реакции.
- Давать определения понятиям: химическая реакция, химическое уравнение, реакция соединения, реакция разложения.
- Применят ь Закон сохранения массы веществ при выведении коэффициентов в уравнении хим.реакции.
- Определять типы хим.реакций.
- Осуществлять рефлексию учебной деятельности

Задание № 1
Экспресс- опрос
- Химия- это наука…
- Химическое уравнение - это …
- Химические реакции - это …
- Каковы признаки химических реакций?

Задание № 2
ГОРЕНИЕ СВЕЧИ
- Признак химической реакции:
выделение
тепла и света

Реакция между раствором хлорида кальция и раствором щелочи.
- Признак химической реакции:
выпадение
белого
осадка.

Действие индикаторов на растворы кислоты, щелочи и воды.
- Признак химической реакции:
изменение окраски индикатора.

Реакция между раствором хлорида железа (III) и раствором щелочи.
- Признак химической реакции:
выпадение
бурого
осадка.

ГОРЕНИЕ СТАЛЬНОЙ ПРОВОЛОКИ В КИСЛОРОДЕ
- Признак химической реакции:
выделение
тепла и света

РЕАКЦИЯ МЕДИ С АЗОТНОЙ КИСЛОТОЙ
- Признак химической реакции:
выделение бурого газа

Задание № 3
Перечислите условия , необходимые для осуществления химической реакции:
- Соприкосновение веществ
- Перемешивание веществ
- Определенная температура
Предложите действие. Сделайте это четко, ясно и кратко. Вы должны хорошо представлять, как аудитория выполнит это действие. Если вы этого не можете представить, аудитория тем более не может этого сделать. Будьте уверенным, предлагая действие.

Химические реакции - это реакции, в результате которых изменяется состав веществ , т.е. из одних веществ образуются другие, новые вещества.
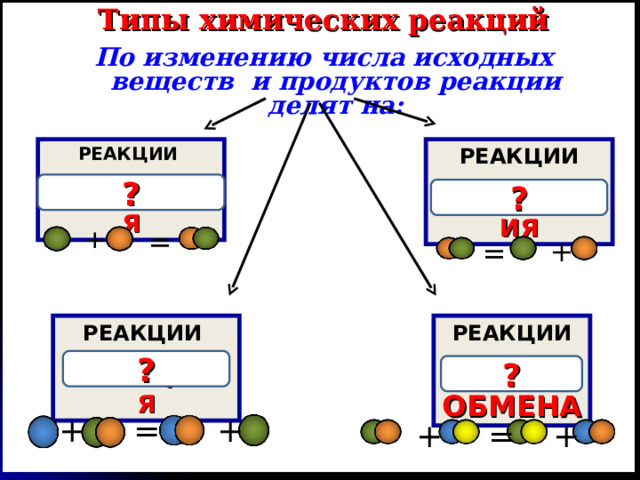
Типы химических реакций
По изменению числа исходных веществ и продуктов реакции делят на:
РЕАКЦИИ
РЕАКЦИИ
РАЗЛОЖЕНИЯ
СОЕДИНЕНИЯ
?
?
+
=
+
=
РЕАКЦИИ
ОБМЕНА
РЕАКЦИИ
ЗАМЕЩЕНИЯ
?
?
+
=
+
=
+
+

Типы химических реакций :
Соединения
Разложения
Замещения
Обмена
12

Задание № 4
Реакция соединения
??? А +B AB
+
=
Реакция соединения - это реакция, при которой из двух или нескольких простых или сложных веществ образуется одно более сложное вещество.

Горение алюминия
https://www.youtube.com/watch?v=nsskGWABldY

Составим уравнение реакции:
-2
+3
Al + O 2 Al O
2
3
4
3
2
Таблица растворимости
CaO + СO 2 CaСO 3
14


Выберите уравнения реакций соединения:
Задание № 5
1) CaCO 3 = CaO + CO 2
2) CuSO 4 + Fe = Cu + FeSO 4
3) 2H 2 + O 2 = 2H 2 O
4) H 2 SO 4 + 2KOH = K 2 SO 4 + 2H 2 O
5) BaO + SO 2 = BaSO 3

Задание № 6
Реакция разложения
??? А B A + B
+
=
Реакция разложения - это реакция, при которой из одного сложного вещества образуется два или несколько простых или сложных веществ.

Разложение оксида ртути ( II)
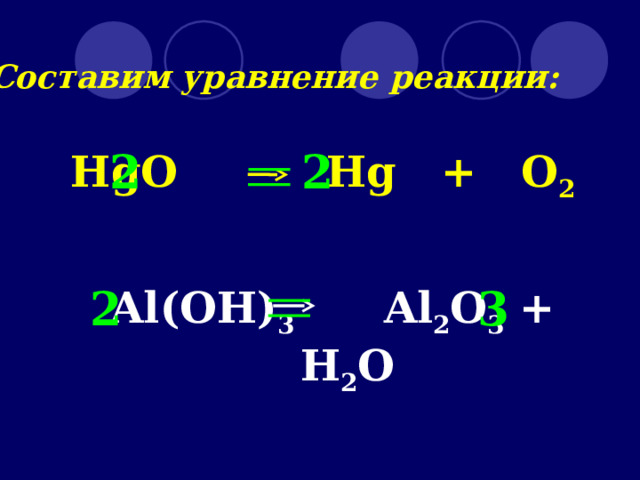
Составим уравнение реакции:
2
2
HgO Hg + O 2
3
2
Al(OH) 3 Al 2 O 3 + H 2 O

Выберите уравнения реакций разложения:
Задание № 7
1) CaO + CO 2 = CaCO 3
2) 2H 2 O = 2H 2 + O 2 ↑
3) Fe + S = FeS
4) CuO + H 2 = Cu + H 2 O
5) Cu(OH) 2 = CuO + H 2 O

Ребята, берегите зрение!
Ребята, берегите зрение!

Задание №8
Игра «ТРЕТИЙ ЛИШНИЙ-1»
1. 2NaCl = 2Na + Cl 2
2. CaO + CO 2 = CaCO 3
3. C + O 2 =CO 2
Ответ:
2NaCl = 2Na + Cl 2

Задание № 9
Игра «ТРЕТИЙ ЛИШНИЙ-2»
1. 2Ag 2 O = 4Ag + O 2
2. 2NO + O 2 = 2NO 2
3. CaCO 3 = CaO + CO 2
Ответ:
2NO + O 2 = 2NO 2

Задание № 10
Самостоятельная работа

Задание № 1
Уравняйте уравнения и определите тип реакции в следующих уравнениях реакций:
1 вариант 2 вариант
1 . Cu + O 2 → CuO ; 1. HgO → Hg + O 2
2. Na+Cl 2 → NaCl 2. Ва + O 2 → BaO
3. Ag 2 O → Ag + O 2 ; 3. H 2 O → H 2 + O 2

Ответ на задание № 1
Уравняйте уравнения и определите тип реакции в следующих уравнениях реакций:
1 вариант 2 вариант
1 . 2 Cu + O 2 = 2 CuO ; 1. 2 HgO = 2 Hg + O 2
2. 2 Na+Cl 2 = 2 NaCl 2. 2 Ва + O 2 = 2 BaO
3. 2 Ag 2 O = 4 Ag + O 2 ; 3. 2 H 2 O = 4 H 2 +O 2

Задание № 2
Химический диктант
2 .1. Докончи определение (устно)
- Реакция соединения- это реакция, при которой…
- Реакция разложения это реакция, при которой…

Химический диктант
2.2 Укажи верно или не верно утверждение
1…из одного сложного вещества образуются два/несколько простых или сложных веществ
2…в молекулах меняются индексы
3…в уравнениях реакций все коэффициенты складываются
4… из нескольких веществ образуются одно сложное вещество
5…из нескольких веществ образуется одно вещество
6…в уравнениях реакций необходимос расставлять коэффициенты
В
Н
Н
В
Н
В

Задание № 11 ( на дом)
Царь зовет к себе Стрельца - удалого молодца
И дает ему поручение государственного значения:
«Чтоб я стал очень богат, нужен мне сульфид алюминия
Ночь даю тебе подумать, утром буду ждать доклад!
Не смогешь – кого винить? Должен я тебя казнить.
Запиши себе названье, чтоб со страху не забыть».
Напишите уравнение реакции получения сульфида алюминия.
Укажите тип реакции.

Что вам сегодня понравилось на уроке?

Домашнее задание
- § 2.4.1-2;
- конспект, PPT
- упр.3стр.25
- упр.работа в группе а)г)з)*стр.25

























































