Просмотр содержимого документа
«Рабочий лист для урока "Вода. Вода в жизни человека"»
Рабочий лист
Фамилия:___________________ Имя:___________________
Тема:________________________________________________________________________
Строение молекулы воды.
Имеет ______________ строение: входящие в её состав атомы образуют __________________ треугольник, в основании которого находятся_______атома водорода, а в вершине______________атом кислорода.
Угол между связями Н-О-Н равен ___________.
В целом молекула Н2О является полярной молекулой, т.е.____________.

М воды =_____________________г/моль.
Соединение молекул воды в более сложные агрегаты за счёт образования водородной химической связи называется_________________________.
Химическая связь между атомами____________________одной молекулы т атомами наиболее электроотрицательных элементов (_________________________________), имеющих неподелённые элетронные пары, другой молекулы называется________________________________________.
Физические свойства воды.
| Агрегатные состояния | 1) 2) 3) |
| Температура кипения и плавления |
|
| Температура, при которой у воды максимальная плотность |
|
| Низкие или высокие значения теплоты плавления и парообразования |
|
| Высокая или низкая удельная теплоёмкость |
|
| Высокое или низкое поверхностное натяжение |
|
| Вязкость |
|
| Гидрофильные вещества |
|
| Гидрофобные вещества |
|
Диссоциация KMnO4 =
Химические свойства воды.
Фотосинтез: 6CO2 + ___________=C6H12O6 + ___________
Взаимодействие с ____________и ___________ оксидами: CaO + H2O =_______
Взаимодействие с активными металлами: 2Na + 2H2O = _______+ H2
Вода разлагает некоторые органические и неорганические вещества:
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
Реакция разложения воды при нагревании до 2000 C:
2H2O 2H2 + __________
Вода вступает в реакцию с некоторыми солями, образуя кристаллогидраты:
CuSO4 + __________ = CuSO4•5H2O
Круговороты воды в природе:________________________________.
Стр.154 учебник
Значение воды для организма человека: ____________________________________________________________________________________________________________________________________________________________________________________________________________________.
Причины загрязнения воды:
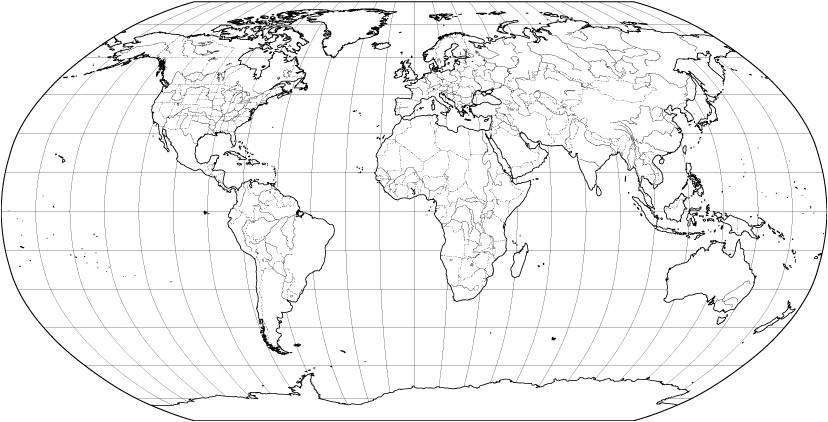
Нанесите на контурную карту названия наиболее загрязнённых вод Мирового океана
Водоочистка
| 1 | Этап состоит в предварительной очистке поступающих на очистные сооружения сточных вод |
| 2 | Этап состоит в переработке органических загрязнителей микроорганизмами |
| 3 | Этап состоит в осаждении оставшихся минеральных примесей солями железа и алюминия |
| 4 | Этап состоит в хлорировании или озонировании воды |
| 5 | Процесс обогащения воды кислородом воздуха |
6) Кластер:

1 вариант
1. Укажите соединение, котором водород имеет степень окисления +1.
NaH
BaH2
H2O
H2
2. Является реакцией горения:
1) СuО + Н2 = Сu + Н2О; 2) Zn + 2HCl = ZnCl2 + H2;
3) Zn + S = ZnS; 4) 4Р + 5О2 = 2Р2О5
3. Вещества, хорошо растворимые в воде, называют:
1) гидрофильными; 2) гидропроводными;
3) гидрофобными; 4) текучими.
4. Расставьте коэффициенты, назовите окислитель и восстановитель:
Mg + H2O = Mg(OH)2 + H2
5. Вычислите массовую долю водорода в воде (в %)
2 вариант
Укажите соединение, в котором водород имеет степень окисления
– 1
HCl
CaH2
NH3
H2
2. Как распознать кислород среди других газов?
1) по окраске; 2) по помутнению известковой воды;
3) по вспыхиванию тлеющей лучинки; 4) по запаху
3.Химическая связь в молекуле воды:
1) ионная 2) ковалентная полярная
3) ковалентная неполярная 4) водородная
4. Расставьте коэффициенты, назовите окислитель и восстановитель:
F2 +H2O = HF+ O2
5.Вычислите массовую долю кислорода в воде (в %)
ОЦЕНКА:
– Какую работу мы сегодня выполняли?
– Чему научились?
– Кто или что вам помогало справиться?
– Кто доволен сегодня своей работой?
| | Все понял | Частично понял | Ничего не понял |
| 1. Строение молекулы воды | | | |
| 2. Водородная связь | | | |
| 3. Физические свойства воды | | | |
| 4. Химические свойства воды | | | |
| 5. Круговорот воды |
|
|
|
| 6. Загрязнение и очистка воды |
|
|
|
| 7. Доволен ли ты своей работой? | | | |

























