
С какими из перечисленных веществ реагирует
соляная кислота:
Ba(OH) 2 , AgNO 3 , NaCl, Hg, Na 2 O, Fe, ZnO, CO 2 ?

Основания,
их классификация и
свойства
СТРАНИЦЫ
Определительная
Классификационная
Способы получения
Химическая (о свойствах)
Техника безопасности
Экспериментальная
Закрепительная

Определительная
Термин «основание» ввел французский химик Г.Руэль в 1744 г.
Основания – это сложные вещества, состоящие из ионов металлов
и связанных с ними гидроксид-ионов
Основания – это электролиты, которые при диссоциации образуют катионы
металлов и анионы гидроксогрупп
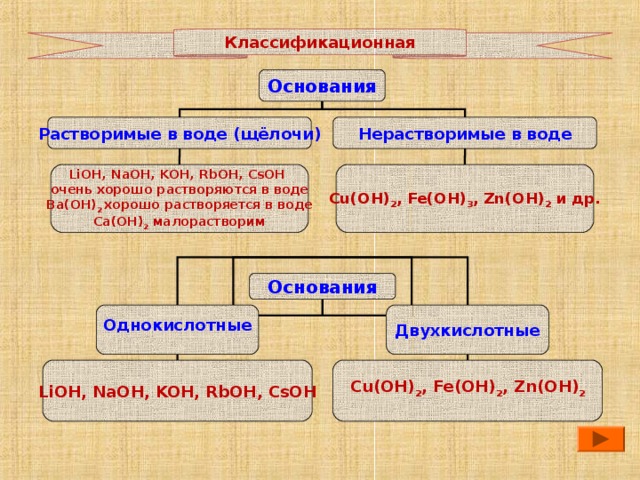
Классификационная
Основания
Нерастворимые в воде
Растворимые в воде (щёлочи)
Cu(OH) 2 , Fe(OH) 3 , Zn(OH) 2 и др.
LiOH, NaOH, KOH, RbOH, CsOH
очень хорошо растворяются в воде
Ba(OH) 2 хорошо растворяется в воде
Са(ОН) 2 малорастворим
Основания
Двухкислотные
Однокислотные
LiOH, NaOH, KOH, RbOH, CsOH
Cu(OH) 2 , Fe(OH) 2 , Zn(OH) 2
5

NaOH
Закрепительная
Zn(OH) 2
Fe(OH) 2
Гидроксид цинка( II)
Fe(OH) 3
Гидроксид натрия
Гидроксид железа ( II)
Гидроксид железа ( III)
5
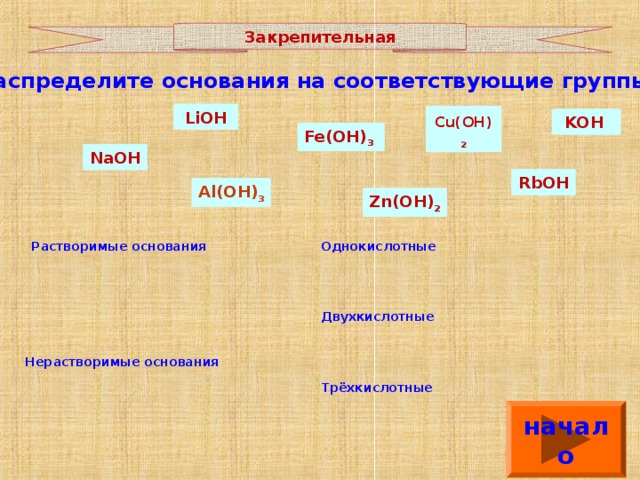
Закрепительная
Распределите основания на соответствующие группы:
LiOH
LiOH
Cu(OH) 2
KOH
KOH
Cu(OH) 2
Fe(OH) 3
Fe(OH) 3
NaOH
NaOH
RbOH
RbOH
А l(OH) 3
А l(OH) 3
Zn(OH) 2
Zn(OH) 2
Однокислотные
Растворимые основания
Двухкислотные
Нерастворимые основания
Трёхкислотные
начало
5
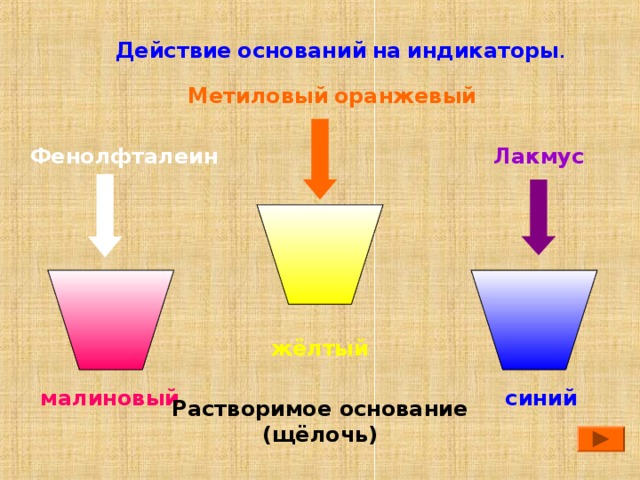
Действие оснований на индикаторы .
Метиловый оранжевый
Лакмус
Фенолфталеин
жёлтый
малиновый
синий
Растворимое основание
(щёлочь)
5

Техника безопасности
Растворы щелочей разъедают
кожу, ткани, бумагу.
При ожогах щелочью необходимо промыть место
ожога обильно водой
и нейтрализовать 2% раствором борной кислоты .
Твердые щёлочи гигроскопичны, они поглощают
воду
из воздуха, поэтому их хранят в таре –
сделанной из пластмассы .
Растворы щелочей можно распознать, используя
индикаторы .
5
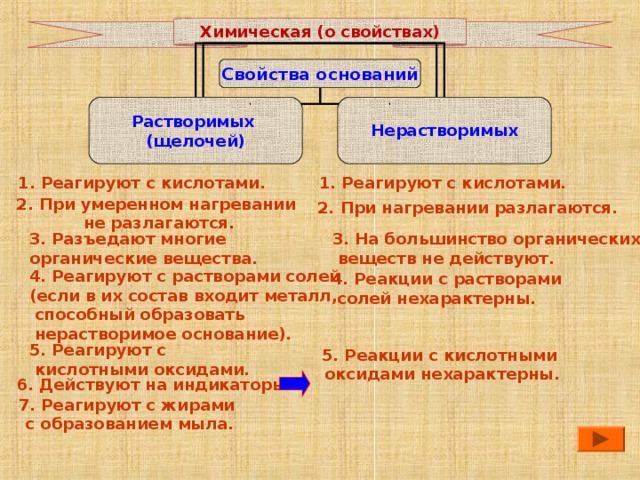
Химическая (о свойствах)
Свойства оснований
Нерастворимых
Растворимых
(щелочей)
1. Реагируют с кислотами.
1. Реагируют с кислотами.
2. При умеренном нагревании
не разлагаются .
2. При нагревании разлагаются.
3. Разъедают многие
органические вещества.
3. На большинство органических
веществ не действуют.
4. Реагируют с растворами солей
(если в их состав входит металл,
способный образовать
нерастворимое основание).
4. Реакции с растворами
солей нехарактерны.
5. Реагируют с
кислотными оксидами.
5. Реакции с кислотными
оксидами нехарактерны.
6. Действуют на индикаторы
7. Реагируют с жирами
с образованием мыла.
10

- Лабораторный опыт «Типичные реакции оснований» План деятельности: - Изучение инструкции -Поиск информации в учебнике -Проведение опыта -Наблюдение за ходом эксперимента -Обобщение и выводы по эксперименту -Оформление в тетради результатов эксперимента
10

Экспериментальная
Осуществите следующие превращения
Вариант 1
CuO → CuCl 2 → Cu(OH) 2 → CuO
Вариант 2
Fe → FeCl 2 → Fe(OH) 2 → FeO
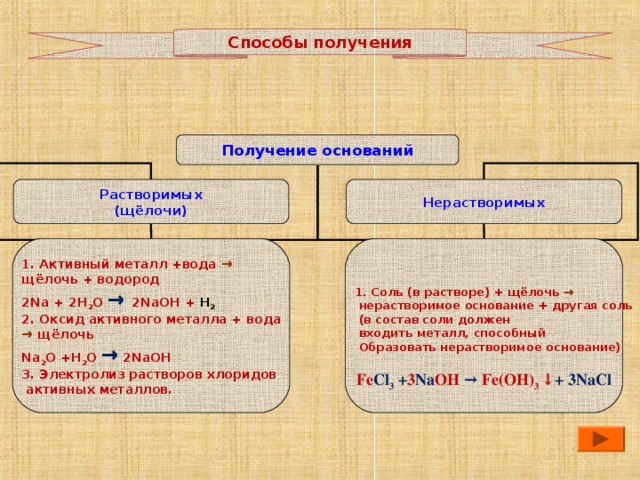
Способы получения
Получение оснований
Нерастворимых
Растворимых
(щёлочи)
1. Активный металл +вода →
щёлочь + водород
2Na + 2H 2 O → 2NaOH + H 2
2. Оксид активного металла + вода
1. Соль (в растворе) + щёлочь →
нерастворимое основание + другая соль
(в состав соли должен
входить металл, способный
Образовать нерастворимое основание)
→ щёлочь
Na 2 O +H 2 O → 2NaOH
3. Электролиз растворов хлоридов
активных металлов.
Fe Cl 3 + 3 Na OH → Fe(OH) 3 ↓ + 3NaCl
13

- Лабораторный опыт План деятельности: - Изучение инструкции -Поиск информации в учебнике -Проведение опыта -Наблюдение за ходом эксперимента -Обобщение и выводы по эксперименту -Оформление в тетради результатов эксперимента
13






































