Просмотр содержимого документа
«Презентация по теме "Основания"»

Классификация и свойства оснований

Какие вещества называются основаниями?

Классификация оснований
Основания
по растворимости в воде
по степени электролитической диссоциации
по числу гидроксогрупп
(кислотность)
нерастворимые в воде
растворимые в воде
(щелочи)
слабые
сильные
двухкислотные
однокислотные
Al(OH) 3
нерастворимые основания, водный раствор аммиака
КOH
NaOH
щелочи
Zn(OH) 2
NaOH
Сu(OH) 2
Mg(OH) 2
Ca(OH) 2

Название оснований
Гидроксид
+
Название металла в родительном падеже
+
Степень окисления римскими цифрами

Дайте названия гидроксидам
Fe(OH) 2
Ca(OH) 2
Al(OH) 3
Fe(OH) 3

Все щелочи называют едкими т.к. они разрушают бумагу, ткань и древесину.

Гидроксид калия разрушает ткань
Гидроксид калия разрушает ткань
Химические свойства оснований
А) растворимых оснований

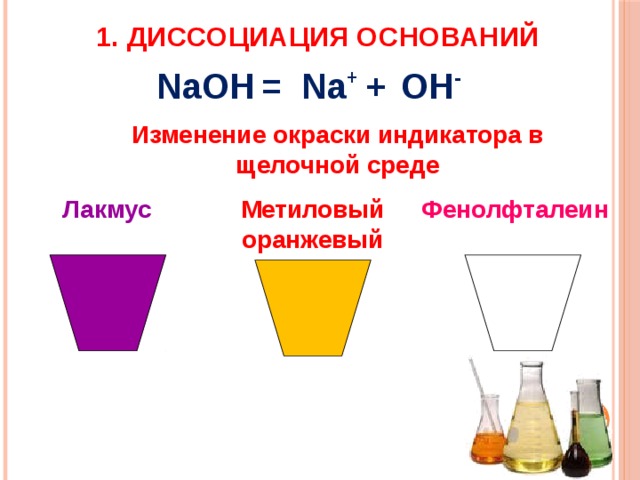
1. Диссоциация оснований
NaOH
=
OH -
Na +
+
Изменение окраски индикатора в щелочной среде
Лакмус
Метиловый оранжевый
Фенолфталеин
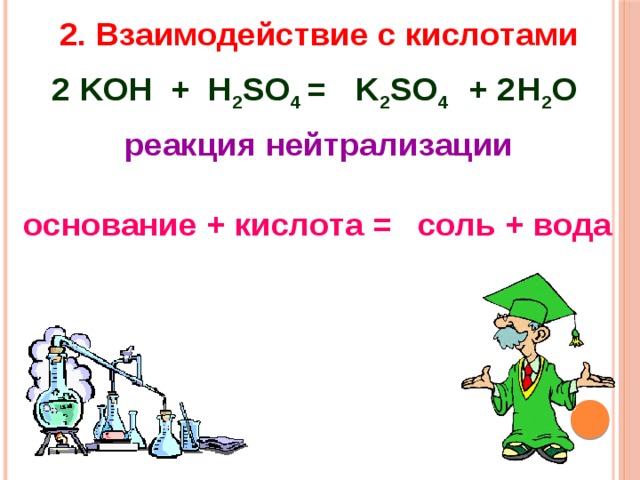
2. Взаимодействие с кислотами
KOH + H 2 SO 4 =
K 2 SO 4 + H 2 O
2
2
реакция нейтрализации
основание + кислота =
соль + вода
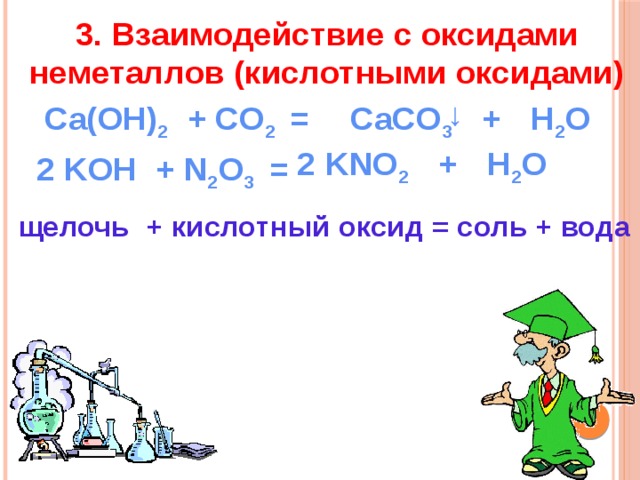
3. Взаимодействие с оксидами неметаллов (кислотными оксидами)
↓
Ca(OH) 2 + CO 2 =
CaCO 3 + H 2 O
KNO 2 + H 2 O
2
KOH + N 2 O 3 =
2
щелочь + кислотный оксид = соль + вода

4. Взаимодействие с солями
↓
KOH + CuCl 2 =
KCl + Cu(OH) 2
2
2
протекает в том случае, если образуется ↑, ↓
щелочь + соль =
новое основание + новая соль

Химические свойства нерастворимых оснований
Cu(OH) 2 + HCl =
CuCl 2 + H 2 O
2
2
основание + кислота = соль + вода
1. Взаимодействие с кислотами

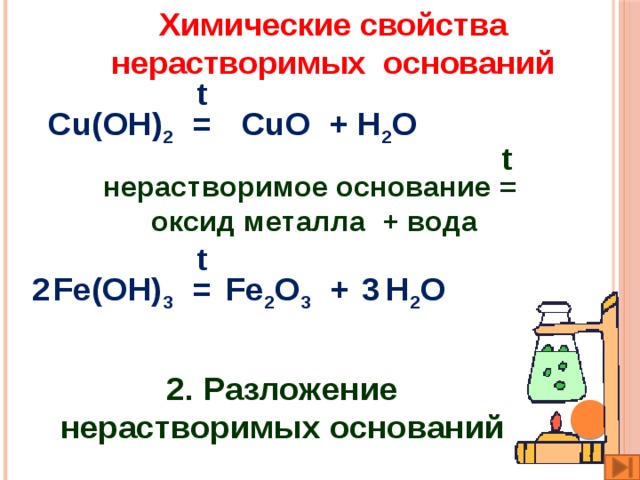
Химические свойства нерастворимых оснований
t
Cu(OH) 2 =
CuO + H 2 O
t
нерастворимое основание =
оксид металла + вода
t
Fe(OH) 3 =
Fe 2 O 3 + H 2 O
2
3
2. Разложение нерастворимых оснований

Применение оснований
Аккумуляторы
Очистка нефти
Химическая промышленность
ОСНОВАНИЯ
Текстильная промышленность
Сельское хозяйство
Строительство
Производство мыла

Домашнее задание












































