Просмотр содержимого документа
«Презентация урока по химии "Основания"»

Урок химии 8 класс

Девиз урока:
«Лучший способ изучить что-либо - это открыть самому»

Задание распределить вещества по группам: 1) простые вещества, 2) кислотные оксиды, 3) основные оксиды. Назвать оксиды
- NaOH
- Al
- CO 2
- O 3
- Fe(OH) 3
- SO 3
- MgO
- Ba(OH) 2
- K 2 O
- KOH
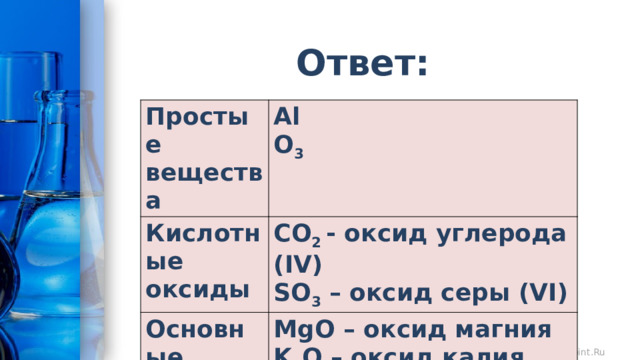
Ответ:
Простые вещества
Al
Кислотные оксиды
O 3
CO 2 - оксид углерода (IV)
Основные оксиды
SO 3 – оксид серы (VI)
MgO – оксид магния
K 2 O – оксид калия
Вопрос : К какому классу соединений можно отнести оставшиеся вещества из списка? Что их объединяет?
- NaOH
- Fe(OH) 3
- Ba(OH) 2
- KOH

Демонстрация эксперимента

Тема урока:
ОСНОВАНИЯ

Цели и задачи урока : (формулируются учащимися)
- Дать определение понятию «основания».
- Познакомиться с составом, классификацией и образцами оснований.
- Изучить их физические свойства.
- Научиться составлять формулы оснований,
называть их.
- Исследовать действие индикаторов на основания.

Основания – это сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксогрупп. Число гидроксогрупп определяется валентностью металла.
Общая формула оснований:
Me(OH) n
- Me – знак элемента металла
- OH – гидроксильная группа ( валентность равна I )
- n – число гидроксильных групп = валентности металла
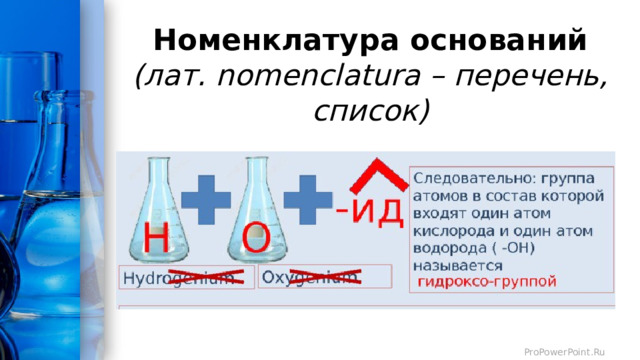
Номенклатура оснований (лат. nomenclatura – перечень, список)

Модельный ответ задания по карточке № 1
- Ca(OH) 2 – гидроксид кальция
- Fe(OH) 3 – гидроксид железа (III)
- NaOH – гидроксид натрия
- Гидроксид лития – LiOH
- Гидроксид меди (II) – Cu(OH) 2
- Гидроксид бария – Ba(OH) 2

Задание : установите соответствие между формулой основания и его названием
Mg(OH) 2
Гидроксид меди (I)
CuOH
Гидроксид магния
KOH
Гидроксид калия

Физкультминутка

Техника безопасности при работе с NaOH и KOH
- При контакте слизистых поверхностей с едкой щёлочью необходимо промыть поражённый участок струей воды , а при попадании на кожу после промывания, обработать 1-2 % раствором уксусной кислоты .
- При работе с щелочами рекомендуется использовать
защитные средства :
- резиновые перчатки,
- для защиты тела —халат.

Работа в группах
- 2 группа работает по инструктивной карточкой № 3 Лабораторный опыт «Изменение окраски индикаторов в растворах оснований»
- 1 группа работает по инструктивной карточке № 2 Лабораторный опыт «Физические свойства оснований»
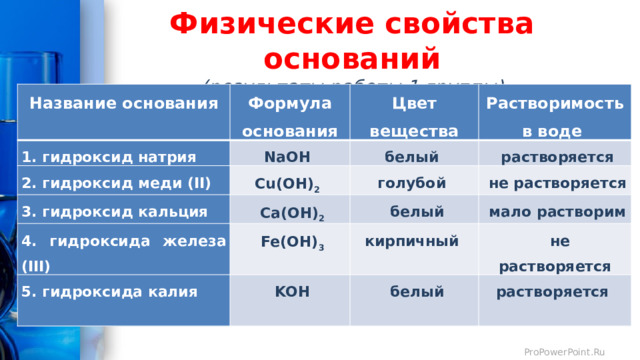
Физические свойства оснований (результаты работы 1 группы)
Название основания
Формула основания
1. гидроксид натрия
NaOH
Цвет вещества
2. гидроксид меди (II)
Растворимость
белый
3. гидроксид кальция
Cu(OH) 2
Ca(OH) 2
растворяется
в воде
голубой
4. гидроксида железа (III)
5. гидроксида калия
Fe(OH) 3
не растворяется
белый
мало растворим
KOH
кирпичный
не растворяется
белый
растворяется
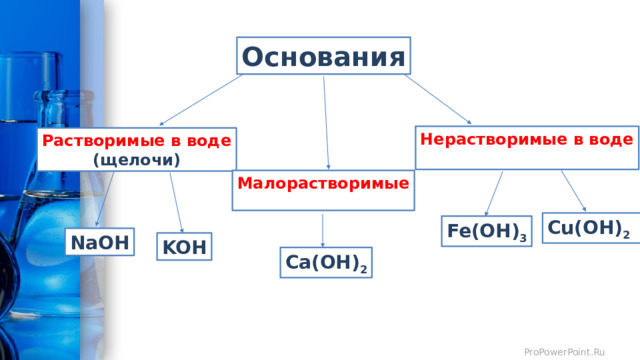
Основания
Нерастворимые в воде
Растворимые в воде
(щелочи)
Малорастворимые
Cu(OH) 2
Fe(OH) 3
NaOH
KOH
Ca(OH) 2
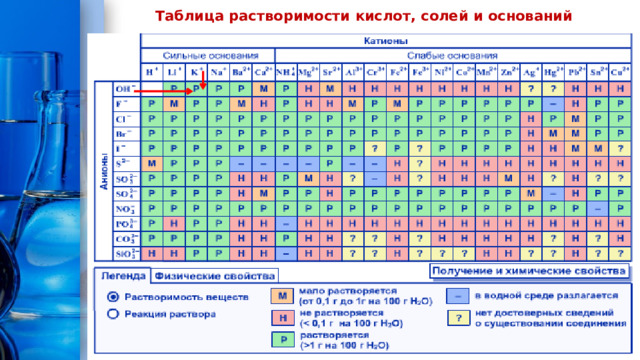
Таблица растворимости кислот, солей и оснований

 7 Нейтральная среда рН =7 … В щелочах у фенолфталеина Настанет не жизнь, а сплошная малина! Ярче цвета всех малин наш фенолфталеин! " width="640"
7 Нейтральная среда рН =7 … В щелочах у фенолфталеина Настанет не жизнь, а сплошная малина! Ярче цвета всех малин наш фенолфталеин! " width="640"
Действие индикаторов на основания (результаты работы 2 группы)
Индикатор
Цвет индикатора в воде
1. Метиловый оранжевый
Цвет индикатора в щелочи
Оранжевый
2. Фенолфталеин
3. Лакмус
Желтый
Бесцветный
Малиновый
Фиолетовый
Синий
Кислая среда - рН
Щелочная среда - рН 7
Нейтральная среда рН =7
… В щелочах у фенолфталеина Настанет не жизнь, а сплошная малина!
Ярче цвета всех малин наш фенолфталеин!
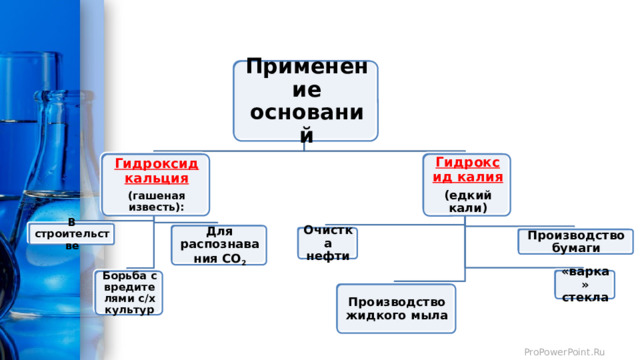
Применение оснований
Гидроксид кальция
Гидроксид калия
(едкий кали)
(гашеная известь):
В строительстве
Для распознавания CO 2
Очистка нефти
Производство бумаги
«варка» стекла
Борьба с вредителями с/х культур
Производство жидкого мыла
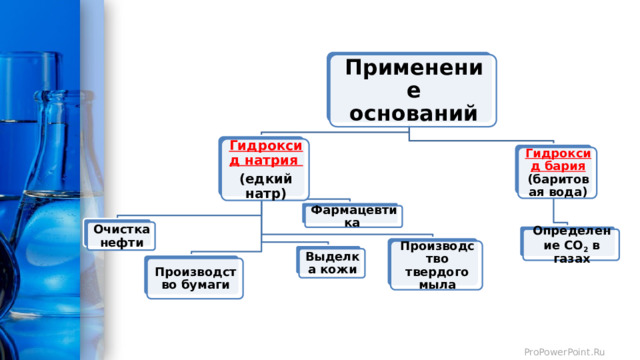
Применение оснований
Гидроксид натрия
(едкий натр)
Гидроксид бария (баритовая вода)
Фармацевтика
Очистка нефти
Определение CO 2 в газах
Производство твердого мыла
Выделка кожи
Производство бумаги

ЗАКРЕПЛЕНИЕ «Третий лишний»
- Гидроксид, основание, оксид
- NaOH, Ba(OH) 2 , Cu(OH) 2
- LiOH, Zn(OH) 2 , Mg(OH) 2
- Фенолфталеин, индикатор, гидроксид.
- Н 2 SO 4 , Сa(OH) 2 , HCl

Ответы
- Оксид.
- Cu(OH) 2 т.к. это нерастворимое основание, а остальные соединения – щелочи.
- LiOH т.к. это щелочь, а все остальные – нерастворимые основания.
- Гидроксид.
- Сa(OH) 2 т.к. только это вещество является основанием.
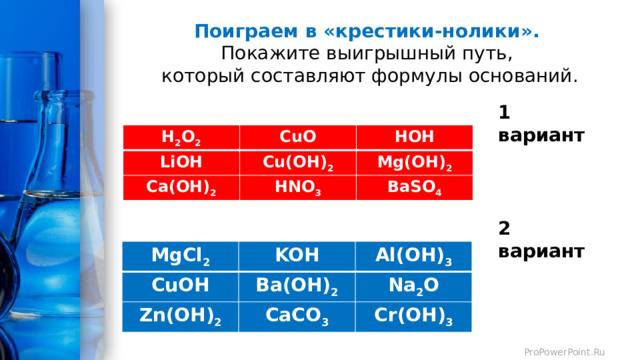
Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оснований.
1 вариант
H 2 O 2
CuO
LiOH
HOH
Cu(OH) 2
Ca(OH) 2
HNO 3
Mg(OH) 2
BaSO 4
2 вариант
MgCl 2
CuOH
KOH
Al(OH) 3
Ba(OH) 2
Zn(OH) 2
Na 2 O
CaCO 3
Cr(OH) 3

Вывод:
- Сегодня на уроке мы познакомились с новым классом неорганических веществ. Каким?
- Основания в своем составе имеют группу. Какую и как она называется?
- Чему равна валентность этой группы?
- Как классифицируют основания?
- С помощью какого индикатора мы можем доказать наличие щелочи в пробирке?

Самооценка работы на уроке:
- 9 – 10 баллов – «5»
- 7 – 8 баллов – «4»
- 5 – 6 баллов – «3»

Домашнее задание:


























 7 Нейтральная среда рН =7 … В щелочах у фенолфталеина Настанет не жизнь, а сплошная малина! Ярче цвета всех малин наш фенолфталеин! " width="640"
7 Нейтральная среда рН =7 … В щелочах у фенолфталеина Настанет не жизнь, а сплошная малина! Ярче цвета всех малин наш фенолфталеин! " width="640"


























