
Гидролиз
солей
«Три пути ведут к знанию: путь размышления – это путь самый благородный; путь подражания – это путь самый легкий и
путь опыта – это путь самый горький»
Конфуций
СОДЕРЖАНИЕ
Алгоритм составления уравнений гидролиза
Определение
Типы солей,участвующих в гидролизе
Примеры солей,участвующих в гидролизе
Обратите внимание!
Применение гидролиза
Вопросы для самоконтроля
процесс разложения соли водой
взаимодействие ионов соли с составными частями молекул воды
ГИДРОЛИЗ
в основном это процесс обратимый, но бывает необратимый, тогда в итоге - образование слабого электролита

Новые понятия
Гидролиз – реакция обмена между растворимыми солями и водой
Сильные кислоты – кислоты, являющиеся сильными электролитами (H 2 SO 4 , HCl, HNO 3 , HBr, HI, HClO 4 и другие)
Слабые кислота – кислоты, являющиеся слабыми электролитами (H 2 CO 3 , H 2 SO 3 , H 2 S, H 2 SiO 3 , H 3 PO 4 и др)
Сильные основания – сильные электролиты - щелочи (NaOH, KOH, Ca(OH) 2 и другие)
Слабые основания – нерастворимые основания, слабые электролиты (Cu(OH) 2 , Al(OH) 3 и другие)

Классификация солей
участвующих в гидролизе:
Соль образована
сильным основанием и слабой кислотой
Соль образована
слабым основанием и сильной кислотой
Соль образована
слабым основанием и слабой кислотой
Соль образована
сильным основанием и сильной кислотой
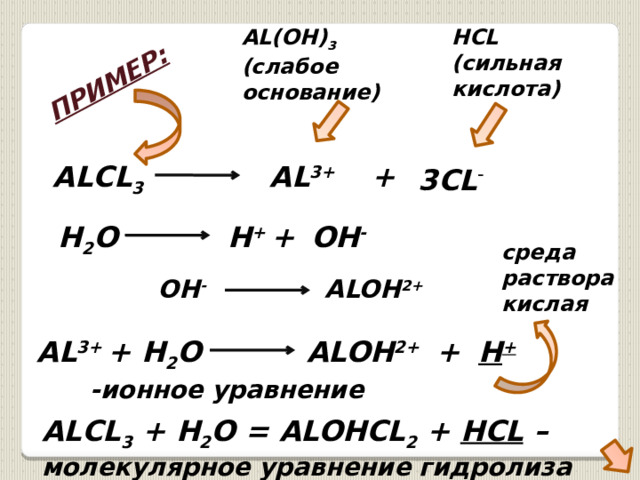
ПРИМЕР:
AL(OH) 3
HCL
(сильная кислота)
(слабое основание)
ALCL 3
3CL -
+
AL 3+
H 2 O
H + OH -
+
среда
раствора
кислая
ALOH 2+
OH -
AL 3+ + H 2 O
H +
ALOH 2+
+
-ионное уравнение
ALCL 3 + H 2 O = ALOHCL 2 + HCL – молекулярное уравнение гидролиза

О Б Р А Т И Т Е
В Н И М А Н И Е:
!
!
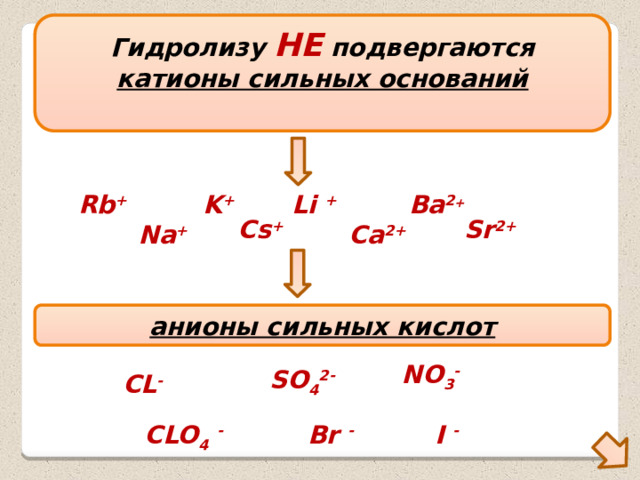
Гидролизу НЕ подвергаются
катионы сильных оснований
K +
Rb +
Li +
Ba 2 +
Sr 2+
Cs +
Ca 2+
Na +
анионы сильных кислот
NO 3 -
SO 4 2-
CL -
CLO 4 -
Br -
I -
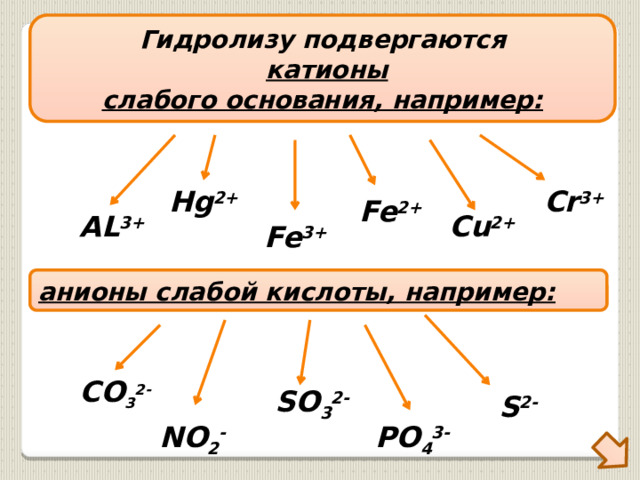
Гидролизу подвергаются
катионы
слабого основания, например:
Cr 3+
Hg 2+
Fe 2+
Cu 2+
AL 3+
Fe 3+
анионы слабой кислоты, например:
CO 3 2-
SO 3 2-
S 2-
NO 2 -
PO 4 3-

Классификация солей
Задание1.
Разделите предложенные формулы солей на четыре типа, объясните свой выбор:
BaCl 2 , ZnSO 4 , CuCl 2 , Na 2 SO 4 , Al(NO 3 ) 3 , MnCl 2 , Cr 2 (SO 4 ) 3 , K 2 SiO 3 , LiNO 3 , Co(NO 2 ) 2 ,MgSO 3

Алгоритм составления
уравнений гидролиза
Проверить растворимость соли.
Определить состав соли, т.е. указать, каким по силе основанием и какой по силе кислотой образована данная соль
Записать диссоциацию соли и подчеркнуть ион слабого электролита
Записать уравнение взаимодействия иона слабого электролита с водой
Определить среду раствора соли
Записать молекулярное уравнение
П Р И М Е Р Ы
С О Л Е Й,
П О Д В Е Р Г А Ю Щ И Х С Я
Г И Д Р О Л И З У
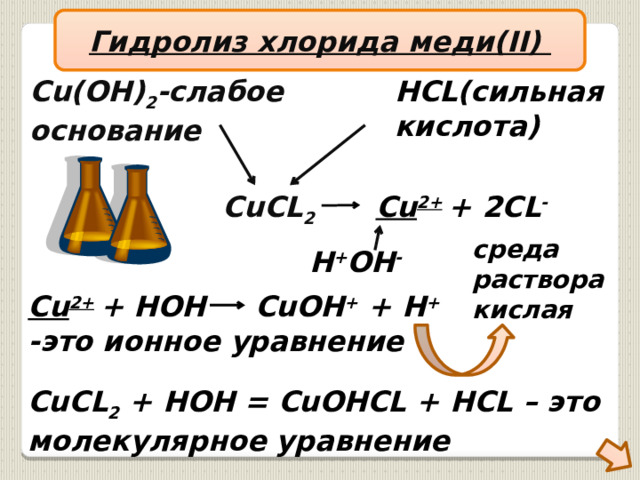
Гидролиз хлорида меди(II)
Cu(OH) 2 -слабое
HCL(сильная
основание
кислота)
CuCL 2
Cu 2+ + 2CL -
среда
раствора
кислая
H + OH -
Cu 2+ + HOH CuOH + + H +
-это ионное уравнение
CuCL 2 + HOH = CuOHCL + HCL – это
молекулярное уравнение
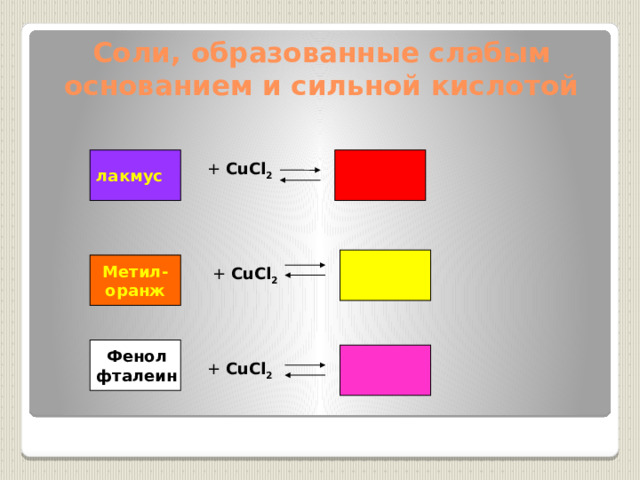
Соли, образованные слабым основанием и сильной кислотой
лакмус
+ CuCl 2
Метил-
оранж
+ CuCl 2
Фенол
фталеин
+ CuCl 2
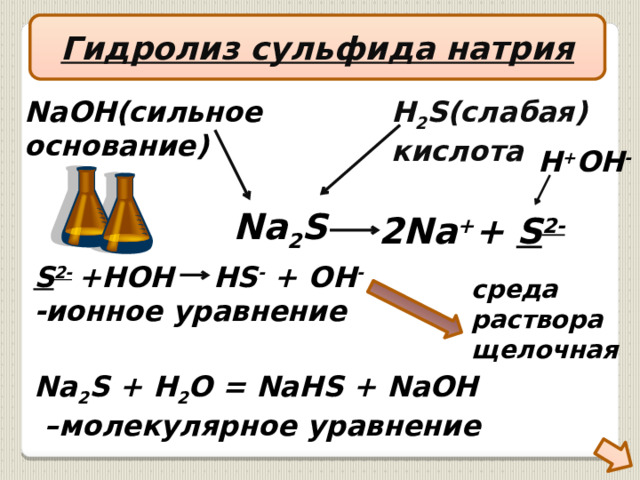
Гидролиз сульфида натрия
NaOH(сильное
H 2 S(слабая)
основание)
кислота
H + OH -
Na 2 S
2Na + + S 2-
S 2- +HOH HS - + OH -
-ионное уравнение
среда
раствора
щелочная
Na 2 S + H 2 O = NaHS + NaOH
– молекулярное уравнение
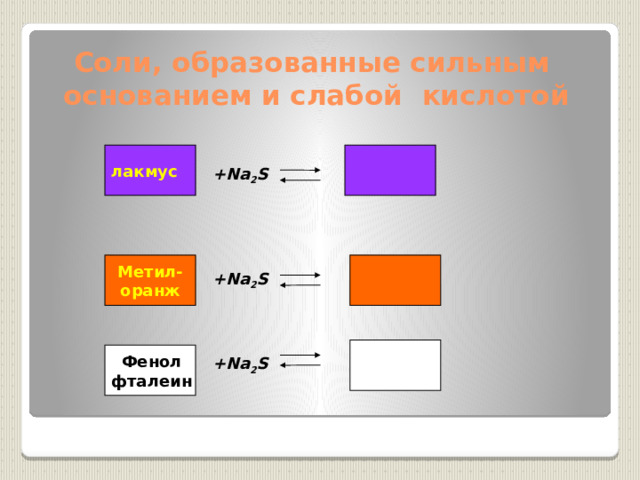
Соли, образованные сильным основанием и слабой кислотой
лакмус
+Na 2 S
Метил-
оранж
+Na 2 S
Фенол
фталеин
+Na 2 S
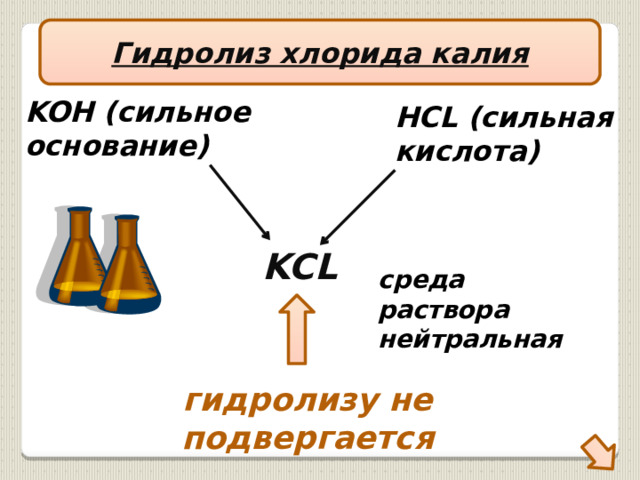
Гидролиз хлорида калия
KOH (сильное
основание)
HCL (сильная
кислота)
KCL
среда
раствора
нейтральная
гидролизу не подвергается
Соли, образованные сильным основанием и сильной кислотой
лакмус
+KCL
Метил-
оранж
+KCL
Фенол
фталеин
+KCL
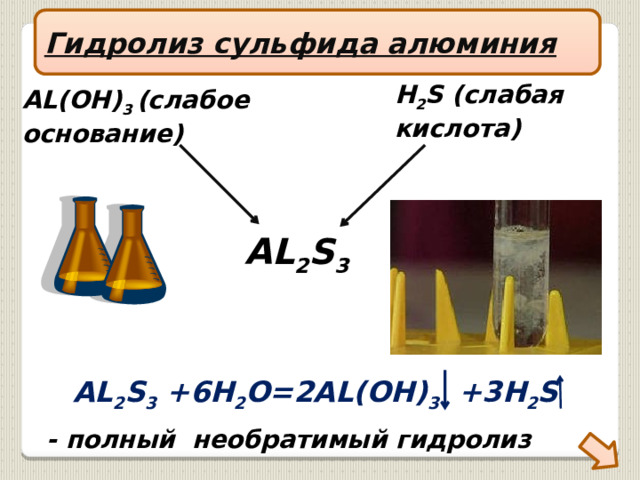
Гидролиз сульфида алюминия
H 2 S (слабая
кислота)
AL(OH) 3 (слабое
основание)
AL 2 S 3
AL 2 S 3 +6H 2 O=2AL(OH) 3 +3H 2 S
- полный необратимый гидролиз
Соли, образованные слабым основанием и слабой кислотой
лакмус
+AL 2 S 3
Метил-
оранж
+AL 2 S 3
Фенол
фталеин
+AL 2 S 3
стирка
мытье
посуды
Роль гидролиза в повседневной
жизни человека
умывание
с мылом

Загрязнения представляют собой смесь твердых частиц (пыли, сажи, соли, жировых, а также потовых пленок, прилипших к поверхности тканей и других предметов).
Чтобы удалить загрязнения необходимо:
- отделить загрязнение от очищаемой поверхности;
- перевести грязевые частицы в моющий раствор;
- удержать их в моющем растворе и устранить возможность повторного осаждения на очищаемую поверхность.
Для умывания, стирки, мытья посуды нужны синтетические моющие средства, в основе которых содержатся в основном соли сильных оснований и слабых кислот.
При их попадании в воду идет гидролиз с созданием щелочной среды (ОН - ), в которой и удаляется грязь.

А ТЕПЕРЬ ВОПРОСЫ….

Найди верный ответ
Нейтральную среду имеет водный раствор:
1)нитрита натрия
2)силиката калия
3)хлорида железа (II)
4)нитрата калия

Найди верный ответ
В водном растворе какой соли фенолфталеин окрашен в малиновый цвет?
1)CaCl 2
2)KNO 3
3)FeSO 4
4)Na 2 CO 3

Найди верный ответ
Одинаковую реакцию среды имеют растворы карбоната натрия и
1) нитрата натрия
2) силиката натрия
3) сульфата калия
4) хлорида алюминия
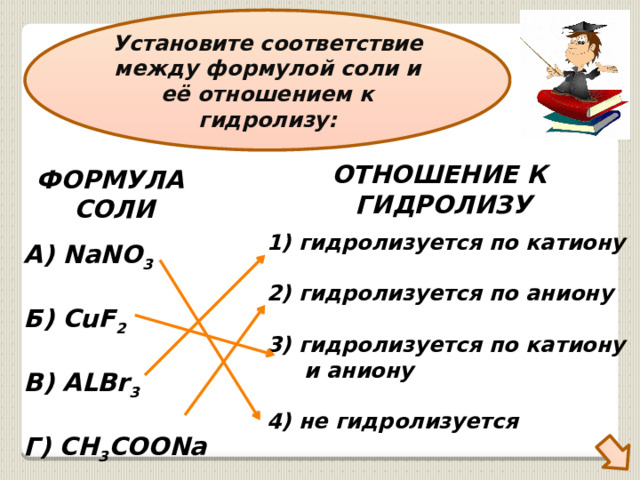
Установите соответствие между формулой соли и её отношением к гидролизу:
ОТНОШЕНИЕ К
ГИДРОЛИЗУ
ФОРМУЛА
СОЛИ
1) гидролизуется по катиону
2) гидролизуется по аниону
3) гидролизуется по катиону
и аниону
4) не гидролизуется
А) NaNO 3
Б) CuF 2
В) ALBr 3
Г) CH 3 COONa
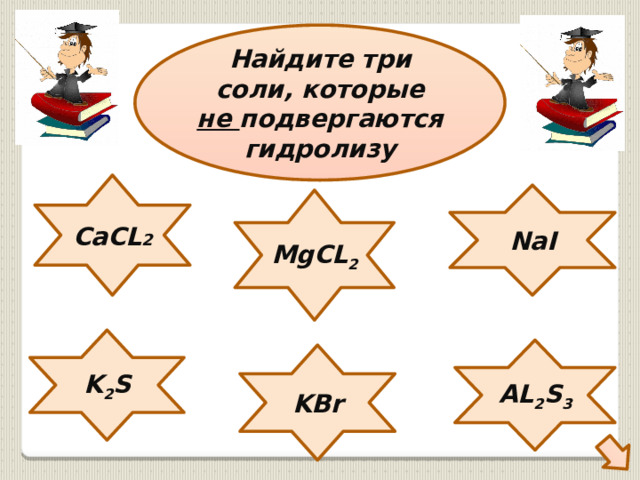
Найдите три соли, которые не подвергаются
гидролизу
CaCL 2
NaI
MgCL 2
K 2 S
AL 2 S 3
KBr

Выберите истинные и ложные утверждения
Гидролиз нитрата алюминия идет по катиону
да
Гидролиз сульфата бария идет по аниону
нет
Гидролиз щелочей не возможен
да
Оксиды подвергаются гидролизу
нет
Хлорид бария не подвергается гидролизу
да
В растворе сульфата меди(ll) кислая среда
да
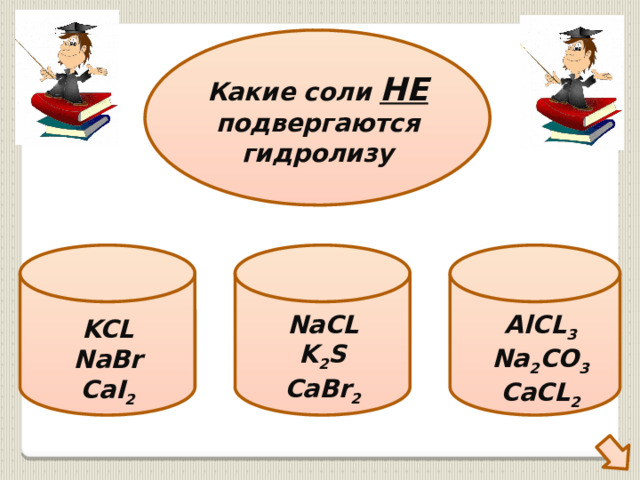
Какие соли НЕ подвергаются гидролизу
NaCL
AlCL 3
K 2 S
Na 2 CO 3
CaBr 2
CaCL 2
KCL
NaBr
CaI 2

Какая соль
подвергается гидролизу
по катиону и по аниону
ВаCL 2
Cr 2 S 3
CuI 2
KNO 2
В Ы В О Д:
Э Т О Н У Ж Н О
З Н А Т Ь И У М Е Т Ь!!!
Определение возможности гидролиза соли (по какой составной части)
Определение среды в растворе соли
Определение цвета индикатора в растворе соли
Составление ионных и молекулярных уравнений
Домашнее задание
§ 1.12
Упр 7 стр 47

СПАСИБО ЗА УРОК!!!




























































