Просмотр содержимого документа
«Презентация по химии на тему "Химические свойства кислот. Кислоты в жизни".»

Кислоты в жизни. Химические реакции кислот

Кислотами называют сложные вещества, молекулы которых состоят из атомов водорода , который может замещаться на атомы металлов, и кислотных остатков.
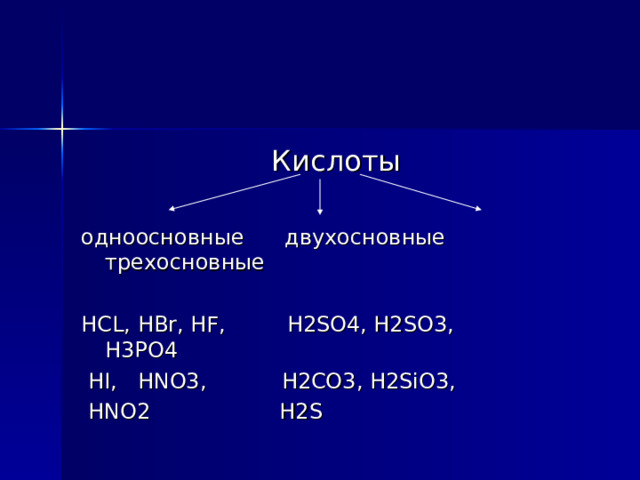
Кислоты
одноосновные двухосновные трехосновные
HCL, HBr, HF, H2SO4, H2SO3, H3PO4
HI, HNO3, H2CO3, H2SiO3,
HNO2 H2S

Основность кислот зависит от количества атомов водорода.
Валентность кислотного остатка зависит от количества атомов водорода.
I II III
H CL , H 2 SO 4 , H 3 PO 4

Классификация кислот
Кислоты
кислородсодержащие бескислородсодержашие
HNO 3 , H 2 SO 4 , H 2 SO 3 , HCL, HF, HBr, HI, H 2 S
H 2 SO 3 , HNO 2 , H 2 SiO 3 ,
H 3 PO 4

Какая кислота в ряду лишняя, назовите её, ответ обоснуйте.
- HCl; HBr; HNO3
- HCl; HNO3; HClO4
- H2SO4; H3PO4; H2CO3
- HBr; HCl; H2CO3

Знаете ли вы, что
… кислоты разрушают живые ткани и вызывают ожоги. Поэтому будьте осторожны в работе с кислотами!
… если кто-то выпил кислоту, то ему дают очень много воды. Для нейтрализации кислоты применять раствор питьевой соды не рекомендуется, так как в органах пищеварения образуется пена, которая может вызвать осложнения.
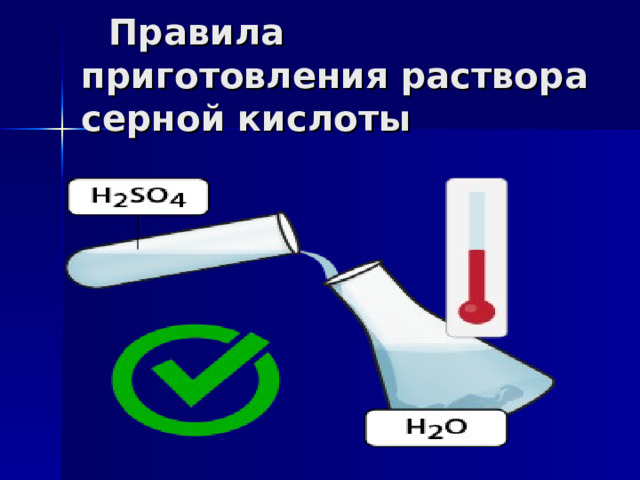
Правила приготовления раствора серной кислоты

Химические свойства кислот
1 . Кислоты изменяют окраску индикаторов.
Лакмус – красный цвет;
Метиловый оранжевый – красно- розовый;
Фенолфталеин - бесцветная.

2 . Взаимодействие с металлами.
Mg + 2HCl= MgCl2 + H2↑
Zn + 2HCl= ZnCl2 + H2↑
Cu + HCl ≠
Запомните, что металлы, стоящие до водорода, вытесняют его из растворов кислот
 CaCL2 + H2O CuО+2HCl = CuCl2 + H2О " width="640"
CaCL2 + H2O CuО+2HCl = CuCl2 + H2О " width="640"
3 . Взаимодействие с оксидами металлов
2HCL + CaO = CaCL2 + H2O
CuО+2HCl = CuCl2 + H2О
 Fe(NO 3 ) 3 + 3 H 2 O " width="640"
Fe(NO 3 ) 3 + 3 H 2 O " width="640"
4. Взаимодействие с растворимыми и не растворимыми основаниями:
HCl+NaOH=NaCl+H2O
Fe(OH) 3 + 3 HNO 3 =Fe(NO 3 ) 3 + 3 H 2 O

Кислоты в жизни

Лимонная кислота



Задание:

Домашнее задание:
- Краткое сообщение о кислоте.
- Творческое задание: составить сказку, кроссворд, ребус, стихотворение о кислотах.

Благодарю за урок!

















 CaCL2 + H2O CuО+2HCl = CuCl2 + H2О " width="640"
CaCL2 + H2O CuО+2HCl = CuCl2 + H2О " width="640"
 Fe(NO 3 ) 3 + 3 H 2 O " width="640"
Fe(NO 3 ) 3 + 3 H 2 O " width="640"


























