Тема урока: Соли (привычные и удивительные) в жизни человека
Цель урока: обобщение и углубление знаний учащихся о солях как одном из основных классов соединений их физических и химических свойствах, знакомство с важнейшими представителями солей их применением.
Задачи урока:
Образовательные.
Привести в систему знания учащихся о составе и классификации солей; составлении их формул, химических свойствах солей как одного из классов неорганических соединений.
Познакомить с некоторыми представителями класса солей, их применением
Воспитательные.
Способствовать развитию навыков коммуникативного общения учащихся, формированию всесторонне развитой личности;
Развивающие.
Создать условия для развития умений учащихся анализировать, обобщать, делать выводы, сравнивать, работать с малым набором реактивов. Применять знания в нестандартных ситуациях.
Уровень: базовый
Форма организации деятельности: коллективная, парная, индивидуальная.
Межпредметные связи: биология, география.
Оборудование:
Учителю - компьютер с мультипроектором,
Ученикам (на каждый стол): Реактивы: нитрат бария, серная кислота, сульфат натрия, гидрокарбонат натрия, карбонат натрия, соляная кислота, карбонат кальция, мрамор пробирки со штативом. Печатная основа с информацией.
Инструктивные карты по проведению лабораторного опыта.
ХОД УРОКА
1. Оргмомент
Здравствуйте! Ребята! Сегодня на уроке мы будем работать над темой, которую вы сможете сформулировать сами, ответив на вопросы
Подсказка:
Это вещество входит в состав крови человека.
Легионеры Древнего Рима получали часть жалованья этим веществом.
Оно содержится в Мировом океане.
Из него в Боливии строят отели.
Наши предки встречали гостей в знак гостеприимства хлебом и … солью!
Верно, наш урок будет посвящен солям, как классу соединений. Солям, которые присутствуют в нашей жизни повсеместно, мы используем их сами того не подозревая.
Поэтому тема нашего урока: СОЛИ (привычные и удивительные) В ЖИЗНИ ЧЕЛОВЕКА
Слайд 1
Мотивация и целеполагание:
С солью люди знакомы еще с глубокой древности. Значение соли отражено во многих пословицах и поговорках: «Хлеб да соль» —в этом выражении подчеркивалось значение соли наравне с хлебом. Хлеб и соль всегда были символом гостеприимства. Говорят: «Чтобы узнать человека, надо с ним пуд соли съесть». Оказывается, двое людей за 2 года съедают пуд соли (16 кг). Каждый человек в год потребляет 3 – 5,5 кг соли. Слайд2
В названиях многих городов и поселков присутствует слово соль: Соликамск, Соль-Илецк, Усолье, Солт-Лейк-Сити, Солтвиль, Зальцбург и др.
Соли образуют мощные отложения в земной коре. В Соль-Илецке, толщина пласта соли превышает 1,5 км. Огромное количество соли содержится в воде морей и океанов. Солью, извлеченной из Мирового океана, можно было бы засыпать сушу земного шара слоем 130 м. Во многих странах Азии и Африки соль добывают из соляных озер, а в европейских странах – из соляных шахт.
Слайд3
Соли могут иметь различную окраску: голубую, синюю, фиолетовую розовую и т.д. Некоторые озера имеют окраску из-за присутствия в них окрашенных солей. Например: Розовое, Красное, Малиновое. Слайд4
Слайд5
Каким образом каждое из изображений относится к теме урока? Поставьте знак «+»если знаете или «-» ,если не знаете. В конце урока мы еще раз вернемся к слайду. М.В.Ломоносов сказал...
| Широко распростирает химия руки свои в дела человеческие … Куда ни посмотрим, куда ни оглянемся, везде обращаются перед очами нашими успехи её прилежания. Действительно химия пронизывает всю жизнь человека, ведь человек живет в мире веществ. И сегодня на уроке нам предстоит еще раз в этом убедиться |
2. Активизация знаний.
Блеф-игра «Верите ли вы…»
Мы употребляем в пищу разные соли
Без солей некоторые продукты имели бы другой внешний вид
Соль спасает наши зубы от кариеса
Соль помогает в борьбе за урожай
Соль помогает людям в получении образования
Соль помогает врачам поставить диагноз
В конце урока мы вернемся и проверим стоило ли верить этим утверждениям….
Слово «соль» мы часто используем в повседневной жизни, а в химии соли –?
Давайте вспомним что мы знаем о солях:
Что такое соли? (учащийся отвечает: сл. вещ-ва...)
Какова классификация солей? Растворимые и нерастворимые
Как определить растворимость соли?
Посмотрите в таблицу растворимости, соли каких металлов – все растворяются в воде
Соли каких кислот все растворимы?
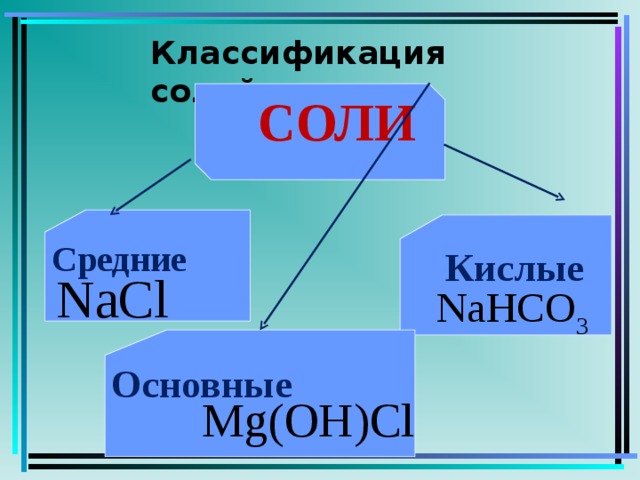
Как еще классифицируют соли? ( Средние, кислые, основные) Слайд 6
Каковы химические свойства солей? Слайд 7
Стадия осмысления информации
Ознакомьтесь с информацией лежащей у вас на столах. Найдите в тексте и выпишите в таблицу названия солей, применяемых в различных областях человеческой деятельности, составьте их формулы, укажите названия и вид солей.
Заполните таблицу
| № | Название соли | Формула соли | Вид соли | Применение соли |
| 1 |
|
|
|
|
| 2 |
|
|
|
|
Проверяем заполнение таблицы, демонстрируя слайды презентации. Учащиеся называют соли и области их применения. Проверяют и корректируют записи.
Вспомните правила ТБ при работе с кислотами, щелочами!
При работе с кислотами и щелочами нужно соблюдать особую осторожность. Если случайно кислота или щелочь попадет на руки или одежду, немедленно следует смыть ее большим количеством воды. Остатки веществ не высыпайте и не выливайте обратно в сосуд с чистыми веществами. Если вы случайно налили слишком много вещества, воспользуйтесь дополнительной чистой пробиркой, имеющейся в вашем штативе. Твердые вещества насыпайте лопаткой. Не оставляйте открытыми пузырьки с веществами.
Учащиеся делятся на группы (можно по рядам) и выполняют опыты по одному на каждую группу (ряд), пользуясь инструкцией (Приложение 2). В печатной форме учащиеся заполняют пропуски, записывают уравнения реакций.
ИНСТРУКЦИЯ 1
Практически осуществите химическую реакцию, протекающую при замешивании теста для блинов. Для этого налейте в пробирку гидрокарбонат натрия и добавьте соляную кислоту
При этом выделяется углекислый газ, что делает тесто пышным.
Почему иногда тесто не поднимается
Опытные повара знают, что для хорошего подъема теста нужно кислоту добавлять в жидкую основу теста, а соду смешивать с мукой
Составьте уравнение химической реакции взаимодействия соды с выделением углекислого газа, придающего тесту необходимую пышность.
ИНСТРУКЦИЯ 2
Приготовьте суспензию, которая используется в рентгенодиагностике под названием «баритовая каша» Для этого проведите реакцию между нитратом бария и сульфатом натрия. Составьте уравнение реакции и ответьте на вопрос, какое применение находит это вещество при производстве конструкторов Lego.
ИНСТРУКЦИЯ 3
При кипячении жесткой воды в чайнике образуется накипь, она состоит из вещества, которое используется при производстве зубных паст в качестве абразивного вещества, способного механически удалять зубной налет и полировать поверхность зубной эмали. Это вещество составляет основу раковин моллюсков, жемчужин, кораллов, из него вновь отстроили Москву после пожара 1812 г. Этот материал хорошо знаком скульпторам, строителям и каждому школьнику, стоящему у доски. Что это за вещество? Как отчистить чайник от накипи. Проведите реакцию в пробирке между ....... Запишите уравнение реакции.
Стадия рефлексии
Что узнали? Возвращение к слайду1: С какими веществами связаны изображения? Возвращение к вопросам блеф-игры
При наличии времени: тест с последующей взаимопроверкой или загадки о солях. Домашнее задание: Выпишите названия и формулы солей, входящих в состав минеральной воды различных источников.
Список литературы
Маркина И.В. Современный урок химии: Технологии, приемы, и разработки учебных занятий. Ярославль: Академия развития, 2008
Маркина И.В. Коррозия металлов и способы защиты от нее//«Химия в школе» 2008 №9 с21-25
http://festival.1september.ru/articles/614547/
https://ru.wikipedia.org/
http://www.myshared.ru/slide/591878/