
Фосфор и его соединения §27, упр.2

История открытия
Считается, что фосфор открыл в 1669 году алхимик из Гамбурга Хеннинг Бранд. Он был разорившимся купцом и пытался разбогатеть с помощью алхимии.
Предполагая, что физиологические продукты могут содержать «первичную материю», которая считалась основой философского камня, Бранд заинтересовался человеческой мочей.

История открытия
Он собрал около тонны мочи из солдатских казарм и выпаривал ее до образования сиропообразной жидкости. Эту жидкость он вновь дистиллировал и получил тяжелое красное «уринное масло», которое перегонялось с образованием твердого остатка. Нагревая последний, без доступа воздуха, он заметил образование белого дыма, оседавшего на стенках сосуда и ярко светившего в темноте.
Бранд назвал полученное им вещество фосфором, что в переводе с греческого означает «светоносец».
И лишь 1777 году К.В. Шееле разработал способ получения фосфора из рога и костей животных.

Природные соединения
И з-за большой химической активности встречается в природе только в виде соединений .
Важнейшими минералами фосфора являются:
Фосфорит
Фторапатит
Апатиты
Хлорапатит
Са 3 (РО 4 ) 2
Са 3 (РО 4 ) 2 • Са F 2
Са 3 (РО 4 ) 2 • Са Cl 2

Природные соединения
Крупнейшее месторождение апатитов находится на Кольском полуострове, в районе Хибинских гор.
Залежи фосфоритов находятся в районе гор Каратау .

Нахождение в природе
Фосфор входит в состав всех живых организмов. А именно он встречается в соединениях:
1. Белковых веществ, содержащихся в генеративных органах растений;
2. Нервной и костной тканей организмов животных и человека;
3. Мозговых клеток.

Получение
Фосфор производят в электрических печах, восстанавливая апатит углем в присутствии кремнезема:
Ca 3 (PO 4 ) 2 +3SiO 2 +5C=3CaSiO 3 +5CO+P 2
Пары фосфора при этой температуре почти полностью состоят из молекул Р2, которые при охлаждении конденсируются в молекулы Р4.
Печь для добывания фосфора

Важнейшие соединения
Н 3 РО 4 фосфорная кислота
Р 2 О 5 оксид фосфора ( V )

Аллотропные модификации фосфора

Физические свойства
- Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропических модификаций; вопрос аллотропии фосфора сложен и до конца не решён. Обычно выделяют четыре модификации простого вещества — белый, красный, черный и металлический фосфор.
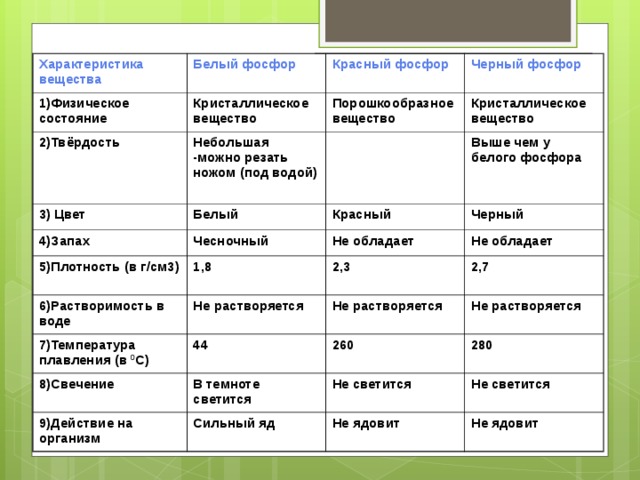
Характеристика вещества
1)Физическое состояние
Белый фосфор
Красный фосфор
Кристаллическое вещество
2)Твёрдость
Порошкообразное вещество
Небольшая -можно резать ножом (под водой)
3) Цвет
Черный фосфор
Кристаллическое вещество
Белый
4)Запах
5)Плотность (в г/см3)
Выше чем у белого фосфора
Красный
Чесночный
1,8
Черный
Не обладает
6)Растворимость в воде
Не обладает
2,3
Не растворяется
7)Температура плавления (в 0 С)
2,7
Не растворяется
44
8)Свечение
Не растворяется
В темноте светится
9)Действие на организм
260
280
Не светится
Сильный яд
Не светится
Не ядовит
Не ядовит

Аллотропные модификации
Горение белого фосфора
Хранение белого фосфора
- Белый фосфор окисляется кислородом уже при обычных условиях, а в тонкоизмельченном состоянии самовоспламеняется, поэтому его хранят под водой. Окисление фосфора сопровождается свечением. Химическая энергия непосредственно превращается в световую .

Химические свойства
В химических реакциях проявляет окислительно-восстановительную двойственность .
Как окислитель взаимодействует со многими металлами , образуя фосфиды .
Фосфор непосредственно с водородом не реагирует .
Как восстановитель взаимодействует с более электроотрицательными неметаллами .
При недостатке кислорода или при комнатной температуре окисляется до оксида фосфора (III).
При сгорании фосфора в кислороде или на воздухе образуется оксид фосфора (V).

Химические свойства
При длительном нагревании белого фосфора без доступа воздуха он желтеет и постепенно превращается в красный фосфор. При нагревании красного фосфора в тех же условиях он превращается в пар, при конденсации которого образуется белый фосфор.
Фосфор проявляет окислительные и восстановительные свойства.
Фосфор – восстановитель:
5О 2 (изб.) + 4Р = 2Р 2 О 5
3О 2 (недост.) + 4Р = 2Р 2 О 3
3Сl 2 + 2P = 2PCl 3 PСl 3 + Cl 2 = PCl 5
3P + 5HNO 3 + 2H 2 O = 3H 3 PO 4 + 5NO
4P + 16H 2 O = 4H 3 PO 4 + 10H 2
Фосфор – окислитель :
2Р + 3Mg = Mg 3 P 2

Оксид фосфора ( V )
Р 2 О 5 – белый порошок, очень гигроскопичен (самый эффективный осушитель).
Является типичным кислотным оксидом .
Взаимодействует с основаниями и основными оксидами .
Оксиду фосфора ( V ) соответствует ортофосфорная кислота .

Физические свойства P 2 O 5
Белый, рыхлый порошок, гигроскопичный. Хранят в герметически закрытых сосудах.

Химические свойства P 2 O 5
Проявляет свойства кислотного оксида.
1) реагирует с водой:
P 2 O 5 + H 2 O 2HPO 3
P 2 O 5 + 3H 2 O t 2H 3 PO 4
2) реагирует с основными оксидами:
P 2 O 5 + 3 К 2 O 2К 3 РО 4
3) реагирует с основаниями:
P 2 O 5 + 6 NaOH 2 Na 3 РО 4 + 3H 2 O

Ортофосфорная кислота
Получение .
t
↔
2
3
О
Н
Р
═
Н
О
+
О
Р
3
4
5
2
2
Взаимодействие оксида фосфора ( V ) с водой при нагревании.
Этим способом получают чистую фосфорную кислоту, которую используют в пищевой промышленности как добавку к безалкогольным напиткам.

Ортофосфорная кислота
Получение .
t
)
═
2
3
3
↓
SO 4
H
PO 4
Ca
(
+
↔
SO 4
H
+
PO 4
Ca
2
2
3
3
КОНЦ.
Вытеснение природных фосфатов более сильной кислотой при нагревании.
Фосфорная кислота, полученная переработкой природных фосфатов, идёт на производство минеральных удобрений.

Ортофосфорная кислота
Ортофосфорная кислота –
- Как трехосновная кислота, диссоциирует ступенчато .
- кристаллическое ,
- нелетучее ,
- твердое ,
- бесцветное вещество.
Н 3 РО 4 ↔ Н + + Н 2 РО 4 ― (дигидрофосфат-ион)
Н 2 РО 4 ― ↔ Н + + НРО 4 2 ― (гидрофосфат-ион)
НРО 4 2 ― ↔ Н + + РО 4 2 ― (фосфат-ион)
- Фосфаты почти всех металлов в воде не растворимы.
Дигидрофосфаты всех металлов хорошо растворимы в воде.
Гидрофосфаты по растворимости занимают промежуточное положение.
- Все нерастворимые в воде фосфаты растворяются в растворах сильных кислот.
- Смешивается с водой в любых отношениях.
- Проявляет все свойства кислот.
- Не является сильной в водном растворе.
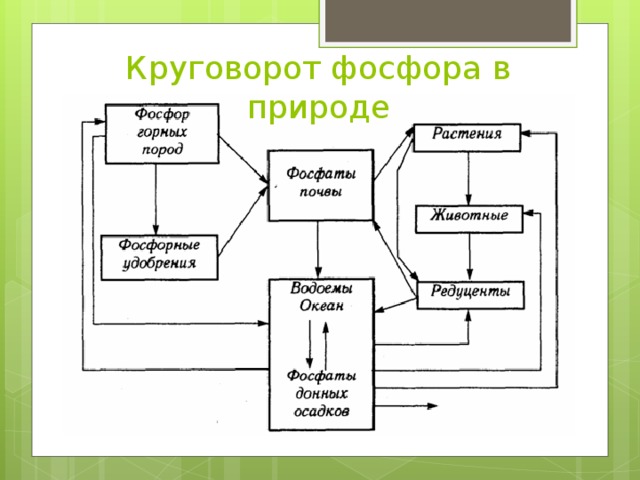
Круговорот фосфора в природе

Применение фосфора

Применение фосфора
Около 80% от всего производства белого фосфора идет на синтез чистой ортофосфорной кислоты. Она используется для получения полифосфатов натрия (их применяют для снижения жесткости питьевой воды) и пищевых фосфатов. Оставшаяся часть белого фосфора расходуется для создания дымообразующих веществ и зажигательных смесей.
Полифосфат натрия

Применение фосфора: спички
Первые фосфорные спички – с головкой из белого фосфора – были созданы лишь 1827 г. Такие спички загорались при трении о любую поверхность, что нередко приводило к пожарам. Кроме того, белый фосфор очень ядовит. Описаны случаи отравления фосфорными спичками как из-за неосторожного обращения, так и с целью самоубийства: для этого достаточно было съесть несколько спичечных головок. Вот почему на смену фосфорным спичкам пришли безопасные, которые верно служат нам и по сей день. Промышленное производство безопасных спичек началось в Швеции в 60-х гг. XIX века.

Применение фосфора: спички
Зажигательная поверхность спичечного коробка покрыта смесью красного фосфора и порошка стекла. В состав спичечной головки входят окислители (PbO 2 , KСlO 3 , BaCrO 4 ) и восстановители (S, Sb 2 S 3 ). При трении от зажигательной поверхности смесь, нанесенная на спичку, воспламеняется.

Применение фосфора
Немало ортофосфорной кислоты потребляет пищевая промышленность . Дело в том, что на вкус разбавленная ортофосфорная кислота очень приятна и небольшие ее добавки в мармелады, лимонады и сиропы заметно улучшают их вкусовые качества. Этим же свойством обладают и некоторые соли фосфорной кислоты. Гидрофосфаты кальция, например, с давних пор входят в хлебопекарные порошки, улучшая вкус булочек и хлеба.

Применение фосфора
Интересны и другие применения ортофосфорной кислоты в промышленности. Например, было замечено, что пропитка древесины самой кислотой и ее солями делают дерево негорючим. На этой основе сейчас производят огнезащитные краски, негорючие фосфодревесные плиты, негорючий фосфатный пенопласт и другие строительные материалы.

Необходим ли фосфор человеку?

Значение фосфора
Фосфор является основой скелета человека и зубов.
Живые организмы не могут обходиться без фосфора.
Значение фосфора состоит в том, что сахара и жирные кислоты не могут быть использованы клетками в качестве источников энергии без предварительного фосфорилирования.
Целый ряд соединений фосфора используют в качестве лекарственных препаратов.

Биологическая роль фосфора
- Суточная потребность для взрослого человека 1 грамм
- Входит в состав скелета
- Входит в состав зубной ткани
- Соединения фосфора принимают участие в обмене энергии
- Необходим для нормальной мышечной и умственной деятельности

Реакция организма на недостаток и избыток фосфора
Развивается заболевание рахит, снижается умственная и мышечная деятельность.
Развивается мочекаменная болезнь, соединения фосфора высоко токсичны (летальная доза 60 мг.).
























































