Т ЕМА: А вогадро
закону

Сабактын тиби: Жаны билимди өздөштүрүү. Сабактын усулу: Интерактивдүү усулдар. Сабактын формасы: Жекеде жана топто Сабактын жабдылышы: Акылдуу доска, маркер, карточка.

Көрсөткүчтөр:
Сабактын максаты:
- Билим беруучулук:
- Авогадро закону: анын биринчи, экинчи корутундусун билишет.
- 1) Авогадро закону: анын биринчи, экинчи корутундусун түшүнүп айта алса.
- Өнүктүрүүчүлүк:
- Моль көлөм, моль масса, бир газдын экинчи газ боюнча салыштырмалуу тыгыздыгы боюнча мисалдарды чыгарышат.
- 2) Моль көлөм, моль масса, бир газдын экинчи газ боюнча салыштырмалуу тыгыздыгы боюнча мисалдарды иштей алса
- Тарбия берүүчүлүк:
- Бири-бирин урматтоого , идеяларын кубаттоого тарбия алышат.
- 3) Жекеде жана топто бирин-бири урматтаса, идеяларды кубаттаса.

Үй тапшырманы текшерүү.

№ 1 тапшырма 2г күкүрт реакцияга кирүүсү үчүн канча грамм темир кошуу керек?
Чыгаруу
Ar(Fe)=56
Ar(s)=32
Ar(Fe) : Ar(S)=56:32=7:4
Темирдин сульфидин алуу үчүн, темир менен күкүрттү төмөнкү массалык катышта аралаштыруу керек 7(темир) : 4(күкүрт).
Эгерде 10г темир алсак, ал эми күкүрттү 4г алчу болсок, химиялык реакция жүрөт бирок калган 3г темир реакцияга кирбейт.

№ 2 тапшырма Жездин эки атому күкүрттүк бир атомуна туура келген зат белгилүү. Жез менен күкүрттү эки зат тең толугу менен реакцияга кирүүчү үчүн кандай массалык катышта алуу керек ?
Чыгаруу
Жездин эки атомунун массасы =64×2=128
Күкүрттүн бир атомунун массасы = 32
Демек, жез менен күкүрттү төмөнкү массалык катышта 128 : 32 же 4 : 1 алуу керек.

№ 3 тапшырма Cуутек менен күкүрт кандай массалык катышта аракеттенишет? (Бул затта күкүрттүн бир жана cуутектин эки атому бар)
Атомдук массаларын таап алабыз Ar(S) жана Ar(H)×2
32 :1×2
32 :2
16 : 1
Бул заттагы бирикмелер 16 : 1 катышында реакцига кирет.

Заттардын курамындагы элементтердин
массалык үлүшүн тапкыла.
NaOH
Мr(NaOH)=23+16+1=40
W ( Na) ==57,5% W ( О) ==40% W ( Н) ==2,5%

Cu(NO 3 ) 2
Mr(Cu(NO3)2=63,5+28+16×6=187,5
W(Сu) ==33,8% W(N) ==15% W(O) ==51,2%
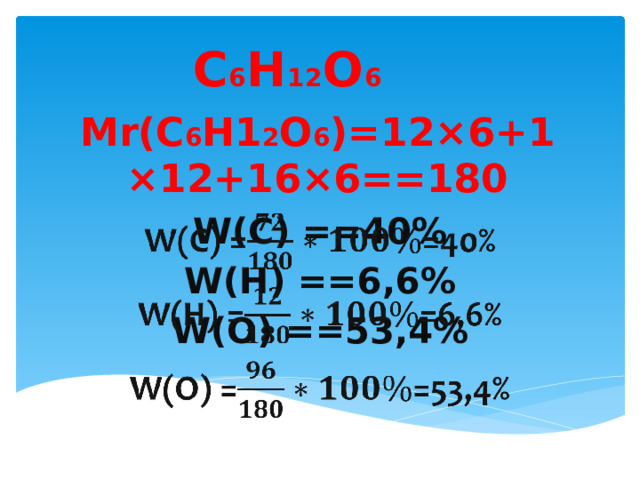
C 6 H 12 O 6
Mr(C 6 H1 2 O 6 )=12×6+1×12+16×6==180
W(C) ==40%
W(H) ==6,6%
W(O) ==53,4%

Сабактагы абалынды баала

Авогадро закону.

Газ абалындагы заттар белгилүү
формага, көлөмгө ээ болбойт.
Кандай гана идишке куюлбасын газ
ошол идиштин көлөмүн ээлеп калат.
Газдын тыгыздыгы өтө төмөн
Болгондуктан алардын илээшкектиги
өтө аз болот.
Газда атом менен молекулалар
баш аламан, иретсиз кыймылда
болуп, бири-бири менен түртүлүшөт.


Авогадро законунун биринчи корутундусу
Бирдей сандагы ар түрдүү газдар бирдей шартта, бирдей көлөмдү ээлейт.
Нормалдуу шарттарда, газдын моль көлөмү 22,4л болот. Бул көлөм газдын моль көлөмү деп аталат.
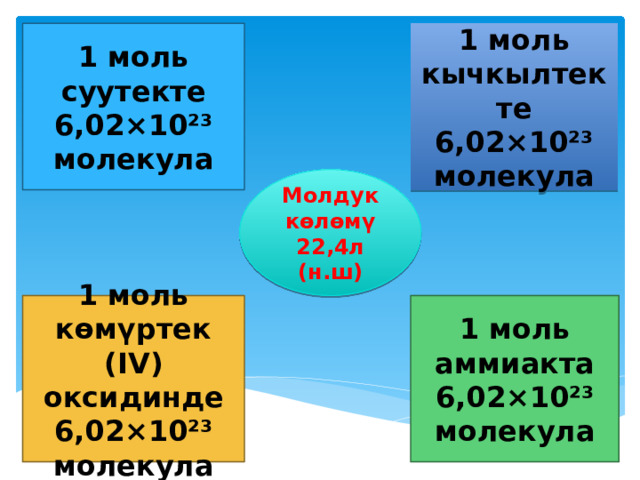
1 моль cуутекте 6,02×10²³ молекула
1 моль кычкылтекте 6,02×10²³ молекула
Молдук көлөмү 22,4л (н.ш)
1 моль көмүртек (IV) оксидинде 6,02×10²³ молекула
1 моль аммиакта 6,02×10²³ молекула

Газдын моль көлөмү – бул берилген газдын бир молунун көлөмү болуп саналат Газдын моль көлөмү газдын көлөмүнүн (н.ш) заттын тийиштүү санына болгон катышы V m =V- газдын көлөмү - заттын саны

Нормалдуу шартта (н.ш) : Температура - 0°С Басым – 101,325 кПа

0,2 моль ар кандай газ (н.ш) кандай көлөмдү ээлейт?
(газ) = 0,2моль
V m = V= V m ×
V(газ)=22,4л/моль××0,2моль=4,48л
табуу керек
Жообу: 4,48л
V(газ)=?

11г көмүртектин (IV) оксиди кандай көлөмдү ээлейт?
М(СО2)=11г
V m = V= V m ×
= M(CO2)=44г/мол
табуу керек
==0,25моль=5,6л
V(CO2)=?
Жообу: 5,6л

Авогадро законунун негизинде төмөнкү жыйынтыкка келүүгө болот: Нормалдуу шартта (н.ш) t=0°С же 273К, Р=760 мм сымап мамычасы=1атм (101,325Па)
1 моль 22,4 6,02×10²³ молекула же атом

Авогадро законунун экинчи корутундусу.
Ар кандай газдын тыгыздыгы төмөнкү формула менен аныкталат.
Р

Бир газдын экинчи газ боюнча салыштырмалуу тыгыздыгы алардын моль же молекулалык массаларынын катышына барабар:
D 2 (1) же D 2 (1)

Ар кандай газдын cуутек боюнча тыгыздыгын табуу: D H 2 (х)
Ар кандай газдын аба боюнча тыгыздыгын табуу:
D аба (х)
Ойлонобуз жана алдыны коздой жылабыз!!!

1) Төмөнкүдөй газдар кандай көлөмдү(н.ш) ээлейт? а) 3,0 моль б) 0,1 моль 2) Нормалдуу шартта төмөнкү заттар кандай көлөмдү ээлейт? а) 22г CO2 көмүртектин (IV) оксиди б) 19г фтор F 3) Төмөнкү заттардын салыштырмалуу тыгыздыгын тапкыла. а) метанды CH 4 cуутек боюнча б) фторду F 2 аба боюнча.

а) Массасы14,2г ………… б) Заттын саны 2 моль …… в) Молекуласынын саны -3,01×10²³ болгон хлордун (н.ш) көлөмүн эсептегиле.

Үйгө тапшырма
Китептен §19 окуп, жумушчу дептерден №6,7 көнүгүүлөрдү иштөө.