
Задачи на растворы

Способы выражения концентрации
Массовая доля растворенного вещества ( ω ), процентная концентрация (С%) – показывает, какая масса вещества растворена в 100 г раствора и вычисляется по формуле
m вещества (г)
ω =------------------
m раствора(г)
Из этой формулы можно получить другие расчетные формулы: m в-ва = ω * m р-ра
m в-ва
m (раствора) =----------
ω
Действия с растворами
3
2
1
Концентри - рование растворов
Разбавление
растворов
Смешивание
2 и более
растворов
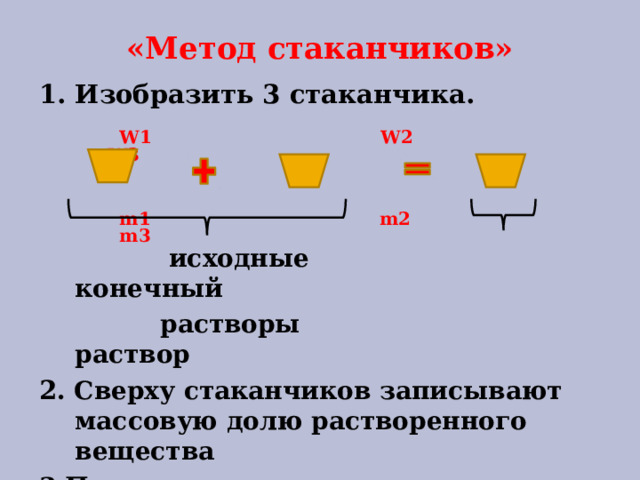
W1 W2 W3
m1 m2 m3
«Метод стаканчиков»
исходные конечный
растворы раствор
2 . Сверху стаканчиков записывают массовую долю растворенного вещества
3.Под стаканчиками – массы компонентов.
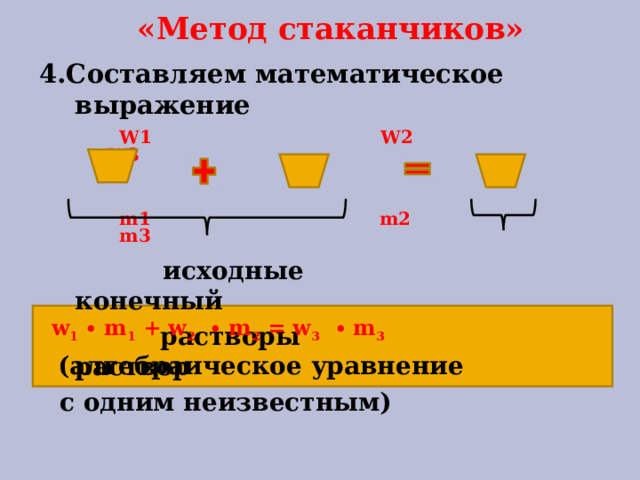
«Метод стаканчиков»
W1 W2 W3
m1 m2 m3
4.Составляем математическое выражение
исходные конечный
растворы раствор
w 1 ∙ m 1 + w 2 ∙ m 2 = w 3 ∙ m 3
( алгебраическое уравнение
с одним неизвестным)

Традиционный способ решения

Решение задач связанные с разбавлением растворов.
Задача. К 120 граммам 5% раствора соли добавили 80 г воды. Вычислите массовую долю соли в полученном растворе.
Решение:
Составляем схему приготовления раствора.
0,05 0 х
120 80 200
Составляем уравнение и решаем его относительно х
- 120 *0,05 + 0 * 80 = 200х
- 6 +0 = 200х
- х = 6/200
х = 0,03 или 3%
Ответ: ω (соли)=0,03 или 3%
│▬│ + │▬│ = │▬│
NB!! Доля в воде
всегда принимается
за 0

Решение задач связанные со смешиванием растворов.
Задача. Смешали 200 граммов раствора с массовой долей соли 0,1 и 20 граммов этого же раствора с массовой долей соли 0,3. Вычислите массовую долю растворенного вещества во вновь полученном растворе?
Решение: Составляем схему приготовления раствора.
0,1 0,3 х
200 20 220
Составляем уравнение и решаем его относительно х
- 200 *0,1 + 20 * 0,3 = 220х
- 20 +6 = 220х
- х = 0,11 или 11%
Ответ: ω (соли)=0,11 или 11%
│▬│ + │▬│ = │▬│

Решение задач связанные с концентрированием раствора
Задача . К 200 граммам 4% раствора соды добавили еще 5 г вещества. Определите массовую долю вещества в полученном растворе.
Дано: Решение:
m (р-ра) = 200г Составляем схему приготовления раствора
ω 1 = 4%или 0,04 0,04 1 х
m добав. в-ва = 5г
Найти ω 2 -? 200 5 205
Составляем уравнение и решаем его относительно х
- 200 *0,04 + 5 * 1= 205х
- 8+5 = 205х
- х = 0,063 или 6,3%
Ответ: ω (соды)=0,063 или 6,3%
│▬│ + │▬│ = │▬│
NB!! Доля самого
c ухого вещества
(без раствора)
всегда =1 (100%).

Решение задач связанные с концентрированием раствора
Задача . Из 400 граммов 20% раствора соли упариванием удалили 100 граммов воды. Чему стала равна массовая доля соли в полученном растворе?
Дано: Решение:
m (р-ра) = 400г Составляем схему приготовления раствора
ω 1 = 20%или 0,2 0,2 0 х
m удал. в-ва = 100г
Найти ω 2 -? 400 100 300
Составляем уравнение и решаем его относительно х
- 400 *0,2 - 100 * 0 = 300х
- 80 = 300х
- х = 0,266 или 26,6%
Ответ: ω (соли)=0,266 или 26,6%
│▬│ ▬ │▬│ = │▬│
NB!! Доля в воде
всегда принимается
за 0

1) К раствору хлорида кальция массой 160г и массовой долей 5% добавили 12г этой же соли. Массовая доля соли в полученном растворе равна ____ %. (Запишите число с точностью до сотых)
2) Массовая доля сахара в сиропе, полученном упариванием 1 кг 10%-го раствора сахара до массы 250 г, равна _____ %. (Запишите число с точностью до целых).
(11,63 %)
(40%)

(19%)
- К 200 г 20%-го раствора гидроксида натрия добавили 80 г воды и 16 г гидроксида натрия. Массовая доля щелочи в полученном растворе равна_______(Запишите число с точностью до целых).
2)Массовая доля соли в растворе, полученном при добавлении 120г воды к 200 г раствора с массовой долей соли 8% равна ______%. (Запишите число с точностью до целых)
3)Рассчитайте массу(г)соли, которую необходимо добавить к 240 мл воды, чтобы получить 16%-й раствор. .( Запишите число с точностью до десятых)
4)Смешали 120 г 12%-го раствора натриевой селитры и 360 г 8%-го раствора этой же соли. Массовая доля соли в полученном растворе составила ______%. (Запишите число с точностью до целых).
(5%)
(45,7 г)
(9%)








































