Тема: Валентность. Валентные возможности атомов
Цели.
Развить представления о валентности как основном свойстве атома, выявить закономерности изменения радиусов атомов химических элементов в периодах и группах периодической системы. Используя интегрированный подход, развивать у учащихся умения сравнивать, сопоставлять, находить аналогии, предсказывать практический результат на основании теоретических рассуждений. Создавая ситуации успеха, преодолевать психологическую инерцию учащихся. Развивать образное мышление, способности к рефлексии.
Оборудование: Таблица « Валентность и электронные конфигурации элементов», мультимедиа.
Эпиграф. «Логика, если она отражается в истине и здравом смысле, всегда ведёт к цели, к правильному результату».
Урок комбинированный, с элементами интеграции. Используемые методы обучения: объяснительно-иллюстрированый, эвристический и проблемный.
Ход урока
I этап. Ориентировочно – мотивационный
Урок начинается с « настройки» (звучит музыка – симфония №3 Й. Брамса).
Учитель: Слово «валентность» (от лат. valentia) возникло в середине XIX в., в период завершения второго химико-аналитического этапа развития химии. К тому времени было открыто более 60 элементов.
Истоки понятия «валентность» содержатся в работах разных ученых. Дж. Дальтон установил, что вещества состоят из атомов, соединенных в определенных пропорциях Э.Франкланд, собственно, и ввел понятие валентности как соединительной силы. Ф.А.Кекуле отождествлял валентность с химической связью. А.М.Бутлеров обратил внимание на то, что валентность связана с реакционной способностью атомов. Д.И.Менделеев создал периодическую систему химических элементов, в которой высшая валентность атомов совпадала с номером группы элемента в системе. Он же ввел понятие «переменная валентность».
Вопрос. Что такое валентность?
Вчитайтесь в определения, взятые из разных источников (учитель показывает слайды через мультимедиа):
«Валентность химического элемента - способность его атомов соединяться с другими атомами в определенных соотношениях».
«Валентность - способность атомов одного элемента присоединять определенное количество атомов другого элемента».
«Валентность - свойство атомов, вступая в химические соединения, отдавать или принимать определенное количество электронов (электровалентность) или объединять электроны для образования общих для двух атомов электронных пар (ковалентность)».
Какое определение валентности, по вашему мнению, более совершенно и в чем вы видите недостатки других? (Обсуждение в группах.)
Валентность и валентные возможности - важные характеристики химического элемента. Они определяются структурой атомов и периодически изменяются с увеличением зарядов ядер.
Учитель. Таким образом, делаем вывод, что:
Валентность электровалентность ( n e )
ковалентность ( A ( x ) B )

(учитель показывает следующий слайд)
Что, по-вашему, означает понятие « валентная возможность»?
Учащиеся высказывают свое мнение. Вспоминают значение слов «возможность», «возможный», уточняют смысл этих слов в толковом словаре С.И.Ожегова:
«Возможность - средство, условие, необходимое для осуществления чего-нибудь»;
«Возможный - такой, который может произойти, осуществимый, допустимый, дозволительный, мыслимый».
(учитель показывает следующий слайд)
Потом учитель подводит итог.
Учитель. Валентные возможности атомов - это допустимые валентности элемента, весь спектр их значений в различных соединениях.
II этап. Операционно – исполнительный
Работа с таблицей « Валентность и электронные конфигурации элементов».
Учитель. Поскольку валентность атома зависит от числа неспаренных электронов, полезно рассмотреть структуры атомов в возбужденных состояниях, учитывая валентные возможности. Запишем электронографические формулы распределения электронов по орбиталям в атоме углерода. С их помощью определим, какую валентность проявляет углерод С в соединениях. Звездочкой (*) обозначают атом в возбужденном состоянии:
|  1s2 2s2 2p2 1s2 2s2 2p2 |
| С(+6) | | , | |
| | |
| II ? |
|  1s2 2s1 2p3 1s2 2s1 2p3 |
| С*(+6) | | , | |
| | | |
Таким образом, углерод проявляет валентность IV за счёт расспаривания
2s2 - электронов и перехода одного из них на вакантную орбиталь. (Вакантный - незанятый, пустующий (С. И. Ожегов).)
Почему валентность С- II и IV , а H-I , He-O , Be – II , B – III , P -V ?
Сопоставьте электронографические формулы элементов (схема №1) и установите причину разной валентности.
Работа в группах:
Схема №1
| + 1 H 1 s1 | | О тсутствие вакансии тсутствие вакансии |
|
|
|
| +2He 1 s2 | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| + 4Be 1 s2 2s2 | |
| |
|
|
|
| II |
| Be* | |
| |
| |
|
| I I I | Распреде-ление элек-тронов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| + 5B 1s2 2s2 2s1 | |
| |
| |
|
| I |
| B* | |
| |
| | |
| III |
|
|
|
|
|
| + 15P 1s2 2s2 2s6 3s2 3s3 | III | P* 1s2 2s2 2p6 3s1 3p3 3d1 | V |
Учитель. Итак, от чего зависят валентность и валентные возможности атомов? Давайте рассмотрим эти два понятия во взаимосвязи (схема №2).
Схема №2

Валентность валентная возможность
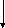
зависит от: зависит от:
| 1) числа неспаренных электронов | 1) наличие вакантной орбитали |
| 2) распределения электронов на энергетическом уровне | 2) распределения электронов по орбиталям при поглощении атомом энергии |
Расход энергии (Е) на перевод атома в возбужденное состояние компенсируется энергией, выделяющейся при образовании химической связи.
В чем отличие атома в основном (стационарном) состоянии от атома в возбужденном состоянии (схема №3)?
Схема№3
Стационарный атом Возбужденный атом
1) расспаривание электронов внешнего энергетического уровня;
2) переход электронов на вакантные орбитали
Учитель. Могут ли быть следующие валентности у элементов: Li - III , О – IV ,
Ne – II ?
Поясните свой ответ, используя электронные и электронографические формулы этих элементов (схема №4).
Работа в группах.
Схема №4
| Li(+3) 1s2 2s1 | | |
|
|
| 1 s 2p s 2p |
|
|
|
|
|
|
|
|
|
|
| O(+8) 1s2 2s2 2p4 | | | | | | 2p 3s | Это возможно? |
|
|
|
|
|
|
|
|
|
| Ne(+10) 1s2 2s2 2p6 | | | | | | 2p 3s |
|
Ответ. Нет, так как в этом случае затраты энергии на перемещение электрона
(1s 2p или 2p 3s) настолько велики, что не могут быть компенсированы энергией , выделяющейся при образовании химической связи.
Учитель. Есть ещё один вид валентной возможности атомов – это наличие неподеленных электронных пар (образование ковалентной связи по донорно – акцепторному механизму):

Н апример: вносит
апример: вносит
| Н:О:Н | + | Н+ | | (Н:О:Н)+ |
|
|
|
|
| или | Н2О + Н+ Н3 О+ |
III этап. Оценочно – рефлексивный
Подводятся итоги, характеризуется работа учащихся на уроке (возвращение к эпиграфу урока). Затем подводится резюме – отношение ребят к уроку, учебному предмету, учителю.
Резюме
1. Что не понравилось на уроке?
2. Что понравилось?
3. Какие вопросы остались для тебя неясными?
4. Оценка работы преподавателя и своей работы? (обоснованная).
Домашнее задание (по учебнику О.С.Габриеляна «Химия-11» параграф №4, упр.6 стр.25)
4








 1s2 2s2 2p2
1s2 2s2 2p2 тсутствие вакансии
тсутствие вакансии  I
I
 Стационарный атом Возбужденный атом
Стационарный атом Возбужденный атом  s 2p
s 2p 
 апример: вносит
апример: вносит
















