Урок № Тема: Удельная теплоемкость
Цель урока: ввести и выяснить физический смысл удельной теплоемкости.
Демонстрации: нагревание жидкостей на двух горелках.
Ход урока
Повторение. Проверка домашнего задания
Дайте определение количества теплоты.
От каких величин зависит количество теплоты, полученное телом в процессе теплопередачи?
Какова единица количества теплоты? Дайте определение старинной единицы количества теплоты - калории.
Каково соотношение между калорией и джоулем? килокалорией и килоджоулем?
Какое количество теплоты нужно сообщить 2 г воды для ее нагрева на 2 °С? (Устно.)
Изучение нового материала
План изложения нового материала:
Понятие удельной теплоемкости.
Удельная теплоемкость различных веществ.
Теплоемкость тела.
Понятие удельной теплоемкости
Прежде чем перейти к рассмотрению нового материала желательно продемонстрировать опыт по нагреванию воды и масла на одинаковых по мощности спиртовках. При этом исходные массы воды и масла, а также их температуры должны быть равны.
Опыт достаточно наглядный, и даже за 3-5 минут нагревания все замечают, что температура масла повысилась больше, чем у воды. Следовательно, строение вещества или род вещества определяет отношение вещества к поглощению энергии извне.
Таким образом, для нагревания одинаковых масс различных веществ требуется разное количество теплоты. Естественно, что нагревание производится в одинаковом диапазоне изменения температуры  t, где
t, где  t =
t = 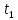 -
- 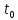
Это свойство веществ определяется удельной теплоемкостью вещества (с).
Опр. Под удельной теплоемкостью понимают физическую величину с, которая численно равна количеству теплоты, которое необходимо для нагревания вещества массы 1 кг на 1 °С.
Таким образом, размерность удельной теплоемкости: 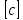 =
= 
Удельная теплоемкость различных веществ
Значение удельной теплоемкости вещества - табличная величина.
Например, для воды с = 4200  . Это значит, что для нагревания 1 кг воды на 1 °С нужно передать воде 4200 Дж тепла.
. Это значит, что для нагревания 1 кг воды на 1 °С нужно передать воде 4200 Дж тепла.
Большинство значений удельной теплоемкости вещества определено экспериментально.
Значение удельной теплоемкости зависит не только от рода вещества, но и от его агрегатного состояния. Если вода при нормальных условиях имеет теплоемкость с = 4200  , то лед уже имеет с = 2100
, то лед уже имеет с = 2100  а водяной пар - другое значение.
а водяной пар - другое значение.
Таким образом, удельная теплоемкость зависит от характера движения и расположения молекул в веществе.
Можно обратить внимание учащихся на то, что для воды значение удельной теплоемкости очень велико. Т. е. для нагревания воды требуется очень много тепла. При понижении температуры окружающей среды вода остывает медленно, отдавая в окружающую среду также много тепла. В результате, наличие больших водоемов (озера, моря) влияем на климат в данном районе.
Теплоемкость тела
Иногда используют еще одну характеристику, которая называется теплоемкостью тела (с*).
Опр. Под теплоемкостью тела понимают то количество теплоты, которое необходимо для нагревания тела на 1°С.  =
= 
Скажем, теплоемкость медного сосуда равна с* = 800 Дж/°С . Это значит, что для нагревания сосуда на 1°С нужно затратить 800 Дж тепла. По таблице можно найти, что удельная теплоемкость меди равна 400  . Следовательно, масса медного сосуда равна 2 кг.
. Следовательно, масса медного сосуда равна 2 кг.
Закрепление изученного материала
Удельная теплоемкость свинца равна 130  . Что это означает?
. Что это означает?
Почему близость водоемов влияет на температуру воздуха?
Что нужно знать, чтобы вычислить количество теплоты, отданное телом при остывании?
Какое количество теплоты необходимо для нагревания на 1°С одного килограмма алюминия? Воды? Ртути?
Что эффективнее использовать в качестве грелки - 2 кг воды или 2 кг песка при той же температуре?
Решение качественных задач
В каком из двух стаканов, содержащих одинаковые количества кипятка, больше понизится температура после того, как в один из них опустят алюминиевую, а в другой - серебряную ложку, массы которых равны?
Какое из тел нагревается до более высокой температуры при получении одинакового количества теплоты: вода массой 1 кг или кирпич такой же массы?
В чем причина различия между морским и континентальным климатом?
Домашнее задание: §8 учебника; вопросы и задания к параграфу; № 933, 1003, 1004, 1030.
Дополнительный материал
Теплоемкость - это величина, характеризующая одно из тепловых свойств тела. Она показывает, какое количество теплоты нужно подвести к телу или отвести от него, чтобы изменить его температуру (соответственно, повысить или понизить ее) на один градус. Отнесенную к единице массы, ее называют удельной теплоемкостью. Все это хорошо вам знакомо. Но причем тут слово «емкость»? Ведь им обычно пользуются, когда говорят об объеме какого-нибудь сосуда, точнее - о его вместимости.
Термин «теплоемкость» появился в физике более 200 лет назад, во второй половине XVIII в., и он остался в физике как память о тех кажущихся теперь странными представлениях о тепле, холоде, температуре, которые существовали тогда в науке.
Начиная с XVII века, в физике шла борьба двух представлений о природе теплоты. Борьба эта закончилась сравнительно недавно - в середине прошлого столетия; в результате одна из теорий теплоты была отброшена полностью, а вторая восторжествовала лишь частично.
Первая теория (точнее было бы сказать - гипотеза) состояла в том, что теплота - это особое вещество, способное проникать в любое тело. Чем больше этого вещества в теле, тем выше его температуру. Опытным фактором, на котором основывалось это представление, служило то, что при контакте двух по-разному нагретых тел более теплое из них охлаждается, а более холодное нагревается. Дело, в самом деле, выглядит так, как будто бы нечто переливается из более теплого тела в более холодное. Это нечто, своего рода тепловое вещество, называли по-разному, но чаще всего - теплородом. Считалось, что всякое тело представляет собой смесь вещества самого тела с теплородом, а температура, измеряемая термометром, характеризует концентрацию теплорода в теле. Слово «температура» по-латыни как раз и означает смесь. Бронза, например, называлась температурой (смесью) меди и олова.
Вторая теория (гипотеза), впервые предложенная в начале XVII века английским ученым Бэконом, утверждала, что теплота - это движение малых частиц внутри тела (молекул, атомов, или, как тогда говорили, нечувствительных частиц). Эта гипотеза тоже основывалась на опытных наблюдениях, показывающих, например, что движением можно вызвать нагревание. У этой теории было много сторонников, и даже очень знаменитых - Декарт, Бойль, Гук, Ломоносов.
Обе теории при всем их различии имели и кое-что общее. И та, и другая сходились на том, что теплота - это нечто, содержащееся в теле. По первой гипотезе, в теле содержится теплород, по второй - частицы с их «живой силой» (так тогда называли кинетическую энергию). Сходились они и в том, что теплота не пропадает и не появляется: если при контакте двух тел одно из них теряет теплоту, то другое получает ее, так что потерянное одним тепло приобретается другим. Тем не менее, подавляющее большинство исследователей вплоть до XIX века придерживались первой, так сказать, вещественной теории теплоты, и XVIII век был, безусловно, веком торжества именно этого представления о теплоте.
Чем же закончился спор о природе теплоты? Какая из двух гипотез победила? Работы, связанные с теплоемкостью, да и другие тепловые исследования XVIII века спора решить не могли. Понадобились эксперименты, которые показали, что температура тепла может повышаться и без подвода теплоты - за счет механической работы. Понадобилось получить и более подробные сведения об атомах и молекулах («нечувствительных частицах»), которых «подозревали» в причастности к теплоте. Все это было сделано в XIX веке. В результате выяснилось, что теория теплорода не имеет никакого отношения к действительности и что теплота действительно связана с движением частиц внутри тел, но не так, как это себе представляли раньше. То, что «содержится» внутри тел, - это не теплота, а внутренняя энергия (т. е. кинетическая энергия поступательного беспорядочного движения частиц - которая и определяет температуру тела, кинетическая энергия вращательного и колебательного движения частиц, а также потенциальная энергия их взаимодействия). Теплота же - это энергия беспорядочного движения частиц тела, передаваемая (например, при контакте) другому телу, или тела. Уравнение 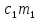 (t -
(t - 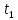 ) -
) - 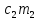 (
(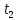 - t),
- t),
в частности, не выражает, как думали прежде, закон сохранения количества теплоты (такого закона нет!). Это просто частный случай закона сохранения энергии для тепловых процессов (т. е. первого закона термодинамики) Q =  U + А. Оно справедливо, когда сама система или внешние силы над системой не совершают механической работы (А = Q), а изменение внутренней энергии системы (
U + А. Оно справедливо, когда сама система или внешние силы над системой не совершают механической работы (А = Q), а изменение внутренней энергии системы ( U) непосредственно связано с процессом теплопередачи (с количеством теплоты Q).
U) непосредственно связано с процессом теплопередачи (с количеством теплоты Q).






 t, где ∆
t, где ∆ - t0
- t0
 t, где
t, где 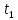 -
- 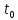
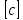 =
= 
 =
= 
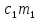 (t -
(t - 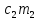 (
(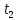 - t),
- t),

















