Просмотр содержимого документа
«Решение задач по теме растворы.»

Решение задач по теме растворы.
m раствора
W вещества
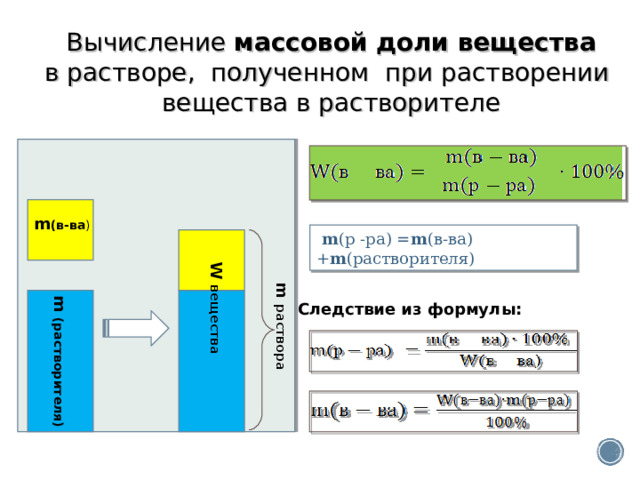
Вычисление массовой доли вещества
в растворе, полученном при растворении
вещества в растворителе
m (в-ва )
m (р -ра) = m (в-ва) + m (растворителя)
m ( растворителя)
Следствие из формул ы:
1. Растворение вещества в воде
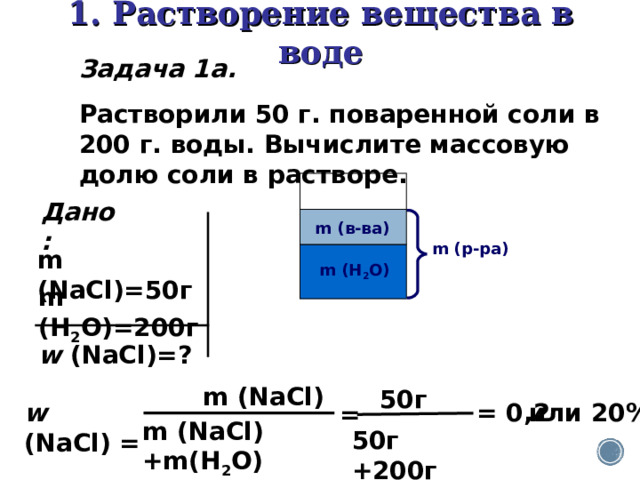
Задача 1а.
Растворили 50 г. поваренной соли в 200 г. воды. Вычислите массовую долю соли в растворе.
Дано:
m ( в-ва )
m (р -ра )
m (N аCl )=50 г
m (H 2 O)
m (H 2 O)=200 г
w (N аCl )=?
m (N аCl )
50г
или 20%
= 0,2
w (N аCl ) =
=
m (N аCl )+m(H 2 O)
50г +200г
3

- Сколько грамм соли и воды нужно взять для приготовления 150 г 15% раств о ра?
Дано:
m ( раствора )= 1 50 г
w (N аCl )= 15 %
m (H 2 O) - ?
m (N аCl ) - ?
m ( H 2 O) = m ( раствора ) - m(N аCl )

- Сколько грамм воды и сахара нужно взять для приготовления 300 г 15% раств о ра?
Дано:
m ( раствора )= 300г
w ( сахара )= 15 %
m (H 2 O) - ?
m ( сахара ) - ?
m ( H 2 O) = m ( раствора ) - m(N аCl )

Составить и решить на отдельном листике две СВО И задачи
Задача 1.
В ________ г воды растворили ______ г поваренной соли. Рассчитайте массовую долю соли в полученном растворе.
Задача 2.
Требуется приготовить __________ г раствора с массовой долей _________ %. Рассчитайте массу требуемых сахара и воды.

Отметьте, какие из следующих четырех утверждений относительно массовой доли растворенного вещества правильные, а какие — неправильные.
А. Массовая доля — это доля молекул растворенного вещества в растворе.
Б. Массовая доля — это отношение массы растворенного вещества к массе раствора, выраженное в процентах.
В. Массовая доля — это отношение массы молекулы растворенного вещества к массе молекулы воды.
Г. Массовая доля — это отношение количества молекул растворенного вещества к количеству молекул растворителя.
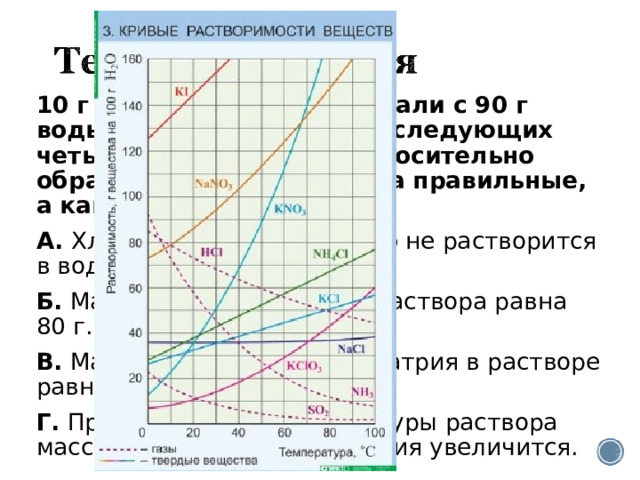
10 г хлорида натрия смешали с 90 г воды. Отметьте, какие из следующих четырех утверждений относительно образовавшегося раствора правильные, а какие — неправильные.
А. Хлорид натрия полностью не растворится в воде.
Б. Масса образовавшегося раствора равна 80 г.
В. Массовая доля хлорида натрия в растворе равна 11,1%.
Г. При повышении температуры раствора массовая доля хлорида натрия увеличится.

- В 250 г раствора сульфата меди (II) содержится 50 г этой соли. Отметьте, какие из следующих четырех утверждений относительно этого раствора правильные, а какие — неправильные.
- А. Раствор сульфата меди имеет красную окраску.
- Б. Масса воды в этом растворе равна 300 г.
- В. Массовая доля сульфата меди в этом растворе равна 17%.
- Г. При понижении температуры из этого раствора начнут выделяться пузырьки газа.
![Решить задачу №5 (стр. 59 - учебник) по образцу на следующем слайде Готовиться к СР по задачам (выберу из составленных Вами) Пусть вас не пугают [МЛ] в задаче Вспомните (или узнайте в инете) плотность воды и как относятся друг к другу плотность и масса воды](https://fsd.multiurok.ru/html/2023/12/05/s_656ed4c26a9c2/img9.jpg)
- Решить задачу №5 (стр. 59 - учебник) по образцу на следующем слайде
- Готовиться к СР по задачам (выберу из составленных Вами)
Пусть вас не пугают [МЛ] в задаче
Вспомните (или узнайте в инете) плотность воды и как относятся друг к другу плотность и масса воды
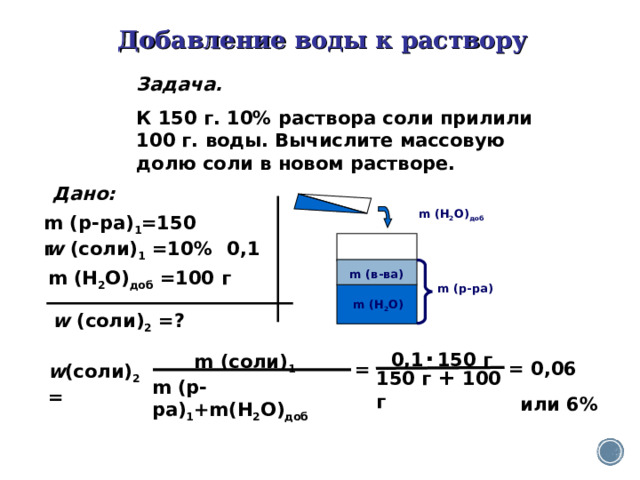
Добавление воды к раствору
Задача.
К 150 г. 10% раствора соли прилили 100 г. воды. Вычислите массовую долю соли в новом растворе.
Дано:
m (H 2 O) доб
m (р-ра) 1 =150 г
0,1
w (соли) 1 =10%
m (H 2 O) доб =100 г
m ( в-ва )
m (р -ра )
m (H 2 O)
w (соли) 2 =?
.
0,1 150 г
m (соли) 1
= 0,06
=
w (соли) 2 =
150 г + 100 г
m (р-ра) 1 +m(H 2 O) доб
или 6%
11
















![Решить задачу №5 (стр. 59 - учебник) по образцу на следующем слайде Готовиться к СР по задачам (выберу из составленных Вами) Пусть вас не пугают [МЛ] в задаче Вспомните (или узнайте в инете) плотность воды и как относятся друг к другу плотность и масса воды](https://fsd.multiurok.ru/html/2023/12/05/s_656ed4c26a9c2/img9.jpg)



















