Тема урока: Реакции ионного обмена и условия их протекания
Тип урока: Урок новых знаний
Вид урока: Проблемно-исследовательский
Цель: сформировать представление учащихся о реакциях, протекающих межу ионами, условий протекания реакций ионного обмена до конца, обратимых реакциях, полных и сокращенных ионных уравнениях.
Задачи:
Образовательные: Актуализировать и углубить знания о ТЭД; рассмотреть реакции обмена в свете представлений ТЭД; сформировать у учащихся представление о сущности реакций ионного обмена; продолжить формировать навыки составления уравнений диссоциации электролитов, сформировать навыки написания полных и сокращенных ионных уравнений.
Развивающие: Продолжить развивать умения применять знания и собственный опыт в различных ситуациях: способствовать развитию мышления, анализу полученных знаний, выделения главного, обобщения и систематизации.
Воспитательные: Создать условия для формирования культуры умственного и практического труда, интереса к знаниям, умений проводить самооценку. Содействовать формированию гуманности, доброты, толерантности, ответственности.
Метод обучения: частично-поисковый.
Ход работы:
Организационный момент:
Здравствуйте, ребята! Я рада приветствовать вас сегодня на уроке! Эпиграфом нашего сегодняшнего урока будут слова:
Три пути ведут к знанию:
Путь размышления –самый благородный,
Путь подражания – самый легкий,
И путь опыта –это самый горький!
Я желаю вам идти к достижению цели трудными, но благородными путями. Сегодня мы должны, ребята, применять полученные знания по теме ТЭД
2.Фронтальная беседа:
1.Какие вещества относятся к электролитам? Приведите примеры
2. Какие вещества относятся к неэлектролитам? Приведите примеры.
3.Ребята перед вами задания (слайд . Из приведенного перечня веществ одной чертой подчеркните , пожалуйста, электролиты, двумя –неэлектролиты.
3.Изучение нового материала. (Объяснение учителя. 15 мин)
До сих пор мы рассматривали процессы, происходящие при растворении одного электролита в воде, сегодня мы рассмотрим .когда в растворе присутствуют два электролита.
Мы с вами знакомы с реакциями обмена. До изучения ТЭД реакции обмена рассматривались как взаимодействие молекул кислот, оснований, солей. Теперь известно, что в растворах этих веществ молекул практически нет, а имеются ионы. Отсюда следует логический вывод.. Реакции между растворами этих веществ сводятся к взаимодействию ионов.
Как вы думаете , как будет звучать тема нашего урока?(слайд 3)
Реакции обмена протекают между ионами, поэтому называются реакции ионного обмена Выводится определение (слайд 4):
При сливании некоторых растворов электролитов реакция протекают, а некоторых случаях нет. По каким признакам можно судить о протекании реакций?
Открываем тетради и пишем сегодняшнюю дату и тему урока
Реакции ионного обмена идут до конца в трех случаях:
рассматриваем первое условие, когда образуется осадок:
Лабораторная работа№1
Выполняем лабораторную работу и заполняем таблицу.
| Исходные вещества | Признаки реакций | Уравнения реакций | Выводы |
|
|
|
|
|
1 группа: Взаимодействие растворов гидрокида натрия и сульфата меди (II) (образуется осадок гидроксида меди (II) (Слайд 5)
2 группа: Взаимодействие растворов карбоната натрия и соляной кислоты (Образуется газ) ) (Слайд 6)
3 группа: Взаимодействие растворов гидроксида натрия и азотная кислота (образуется вода) ) (Слайд 7)
4.Физкультминутка (2 мин)
(Слайд 8) Для реакций ионного обмена составляют полные и сокращенные ионные уравнения. При этом на ионы никогда не раскладывают :
Рассмотрим первое уравнение, когда образуется осадок.(Слайд 9)
CuSO4+2NaOH→Cu(OH)2+Na2SO4
5. Закрепление изученного материала (20 мин)
Колдунья с вороном отравили лечебный колодец, в котором был раствор хлористого кальция, который помогал целому городу. Он использовался горожанами при отравлениях, кровотечениях, аллергиях. Они превратили раствор СaCl2 в нерастворимый известняк CaCO3. Помогите жителям “расколдовать” колодец, если в вашем распоряжении есть растворы NaCl, Na2CO3, HCl, H2SO4, Zn(NO3)2.
Олененок спешит к друзьям. Он шел долгих 3 дня. Ему осталось только перейти реку, но река оказалась испорчена – она наполнена раствором серной кислоты. Помогите Олененку воссоединиться с друзьями, если в вашем распоряжении есть растворы NaCl, Ba(OH)2 HCl, CuSO4, Ba(NO3)2.
Проверка задания 3 (слайд ):
H2SO4 + Ba(OH)2 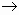 BaSO4
BaSO4  + 2H2O
+ 2H2O
Слайд №
Тигренок и крокодил поранились, а у доктора Айболита закончились все лекарства. У него в распоряжении есть некоторые химикаты: NaNO3, CuOH)2 H2SO4, НCl, BaCl2. Он знает, что раствор сульфата меди (II) может оказывать антисептическое, вяжущее, ранозаживляющее действие. Помогите доктору приготовить раствор и вылечить тигренка и крокодила.
Проверка задания 4 (слайд 18):
Cu(OH)2 + H2SO4 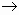 CuSO4 + 2H2O
CuSO4 + 2H2O
Слайд №
Однажды русалка заметила, что ее друзья рыбы перестали с ней играть и уплывают подальше от ее дома. Она не могла понять, в чем дело, ведь они не ссорились... И тогда ее мама рассказала ей, что рыбы уплывают, потому что около их дома почти нет растений, и рыбам не хватает кислорода... Русалка подумала, что можно посадить растения, но они будут расти долго... А из старых мудрых книжек она узнала, что можно насытить воду углекислым газом – повышение концентрации СО2 в воде приводит к значительному ускорению в росте растений. В распоряжении русалки оказались: NaOH, ВaCO3, K2SO4, НCl, Ba(NO3)2. помогите русалке получить углекислый газ.
Проверка задания 5 (слайд 20):
BаСО3 + 2HCl 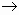 BaCl2 + H2O + CO2
BaCl2 + H2O + CO2 
Вывод урока.
Рефлексия
«я» - как я себя чувствовал в процессе урока, доволен ли я своей работой.
«мы»- насколько комфортно и эффективно мне было работать в малой группе.
«дело» - достиг ли я цели обучения , в чем испытал затруднения, как преодолеть проблемы.























