И.В. Савельев
Путешествие в мир химии
8А класс МБОУ «Школа №53»
2016 Рязань
Станция № 1. «Разминка»
Загадки:
1. Нахожусь, друзья, везде:
В минералах и в воле.
Без меня вы как без рук:
Нет меня - огонь потух. (Кислород)
2.Я блестящий, светло-серый,
Образую хлорофилл,
И меня фотограф первый
Очень поджигать любил! (Магний)
3.Я - металл незаменимый,
Очень летчиком любимый,
Легкий, электропроводный,
А характер - переходный. (Алюминий)
4.Меня любит человек!
Мною назван целый век!
Я блестяща и рыжа,
Очень в сплавах хороша! (Медь)
5.Я светоносный элемент.
Я спички вам зажгу в момент.
Сожгут меня - и под водой
Оксид мой статен кислотой. (Фосфор)
Станция № 8. «Кодирование»
Определить валентность элементов в веществах:
SiH4, CrO3, H2S, CO2, SO3
CO, SO2, Fe2O3, HCl, Cl2O5
FeO, HBr, Cl2O7, РН3, MnO,
Станция № 7. «Химические реакции»
Расставить коэффициенты в уравнениях реакций и определить тип реакций.
H2 + O2 → H2O
Ba + H2O → Ba(OH)2 + H2
P + O2 → P2O5
AlCl3 + NaOH → Al(OH)3 + NaCl
CuCl2 + Mg → Cu + MgCl2
Al(OH)3 + H2SO4 → Al2(SO4)3 + H2O
K + Cl2 → KCl
Fe(OH)2 + HCl → FeCl2 + H2O
MnO2 + HCl → MnCl2 + Cl2 + H2O
Al + Cl2 → AlCl3
P2O5 + KOH → K3PO4 + H2O
KClO3 → KCl + O2
6. Предупреждаю вас заранее:
Я непригоден для дыхания!
Но все как будто бы не слышат
И постоянно мной дышат. (Азот)
7. У меня дурная слава:
Я - известная отрава.
Даже имя говорит,
Что я страшно ядовит. (Мышьяк)
8. В горах далеких Шао Линь
Копали глину – каолин.
Из этой глины с давних пор
В Китае делали … (Фарфор)
9. Такова моя природа:
Известняк, песок и сода,
Много требуют огня,
Чтобы выплавить меня
Я прозрачно и светло
И зовут меня … (Стекло)
10. Сообщаю: я спешу!
Я живу, пока пишу.
Исчертил всю доску белым…
Исчезаю. Был я … (Мелом)
Станция № 2. «Угадай слово»

ЗАДАНИЕ: Заполните пустые клетки русскими названиями следующих элементов: 1) Cl; 2) Zn; 3) Br; 4) K; 5) Ni. Ключевым словом является профессия, связанная с химией. За правильно выполненное задание жюри выдаёт командам вагоны: за полностью правильно выполненное задание – вагон красного цвета, за выполненное задание на половину – синий вагон, за не выполненное задание – команда вагон не получает. Время работы - 1 минута.
Вопрос № 5. Процесс горения – это
А) физическое явление;
Б) химическая реакция, идущая с поглощением теплоты;
В) химическая реакция, идущая с выделением теплоты;
Г) химическая реакция, идущая с выделением тепла и света.
Вопрос № 6. Основными компонентами воздуха являются газы:
А) кислород, водород, аргон;
Б) азот, кислород, благородные газы;
В) кислород, сероводород, углекислый газ;
Г) азот, благородные газы, углекислый газ.
Вопрос № 7. Воздух обогащается кислородом в результате процесса:
А) дыхания;
Б) гниения;
В) горения;
Г) фотосинтеза.
Вопрос № 8. В промышленности кислород получают:
А) из воды;
Б) из бертолетовой соли;
В) из перманганата калия;
Г) из воздуха.
Станция № 6. «Агент 007»
Тест «Воздух. Кислород. Горение.»
Вопрос № 1. Химический знак кислорода:
А). Os
Б). H
В). K
Г). O
Вопрос № 2. Впервые кислород получил:
А) Дж. Дальтон;
Б) Дж. Пристли;
В) А.Лавуазье;
Г) М.В.Ломоносов.
Вопрос № 3. Получение кислорода из воздуха основано
А) на разнице температур кипения жидких азота и кислорода;
Б) на способности кислорода поддерживать процесс горения;
В) на разнице относительных молекулярных масс азота и кислорода;
Г) на малой растворимости кислорода в воде.
Вопрос № 4. Кислород при обычных условиях это:
А) твёрдое вещество голубоватого цвета, без вкуса и запаха;
Б) газообразное вещество, голубого цвета, без вкуса, с запахом свежести;
В) бесцветный газ, без вкуса и запаха;
Г) твёрдые бесцветные кристаллы, сладковатого вкуса, без запаха.
Станция № 3. «Простое - сложное»
В первой колонке подчеркнуть простые вещества, а во второй колонке – сложные вещества.
| ПРОСТЫЕ ВЕЩЕСТВА | СЛОЖНЫЕ ВЕЩЕСТВА |
| 1. Сахар, медь, кислород. | 1. Малахит, золото, серебро. |
| 2. Сера, хлороводород, магний. | 2. Графит, оксид натрия, цинк. |
| 3. Сульфид цинка, вода, водород. | 3. Железо, поваренная соль, оксид магния. |
| 4. Натрий, иод, железо. | 4. Углекислый газ, бромоводород, алюминий. |
| 5. Сульфид натрия, углерод, ртуть. | 5. Азот, сульфид кальция, фосфор. |
| 6. Марганец, хлор, оксид лития. | 6. Оксид магния, бром, сероуглерод. |
Станция № 4. «Надо посчитать»


Решить задачу:
Ученику необходимо было взять для проведения опытов 8,8 г. FeS. Он рассчитал количество вещества 0,1 моль. Правильно ли сделал расчет ученик?
![]()
 Дано: Решение:
Дано: Решение: 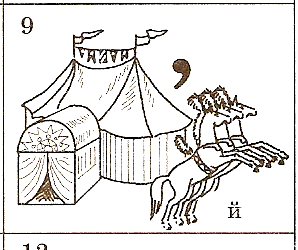

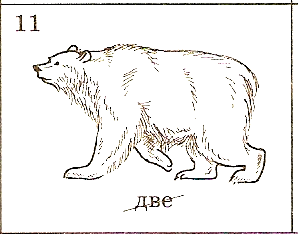







Станция № 5. «Ребусы»






















 Дано: Решение:
Дано: Решение: 





















