
«Гидролиз неорганических веществ»
Подготовила учитель химии Ильясова Б.Н.
МКОУ «Герменчикская СОШ»

Задача:
При сливании раствора, содержащего 5 моль хлорида железа (III), с избытком раствора кальцинированной соды выделяется газ и выпадает осадок. Определите массу выпавшего осадка.

Гидролиз – это реакция обменного взаимодействия вещества с водой, приводящая к их разложению.
Необратимый
Обратимый
Гидролиз

Соль – продукт взаимодействия кислоты и основания.

В процессе гидролиза в водном растворе появляется избыток катионов Н + или анионов ОН – . В зависимости от силы исходной кислоты и исходного основания , образовавших соль выделяют 4 типа солей:
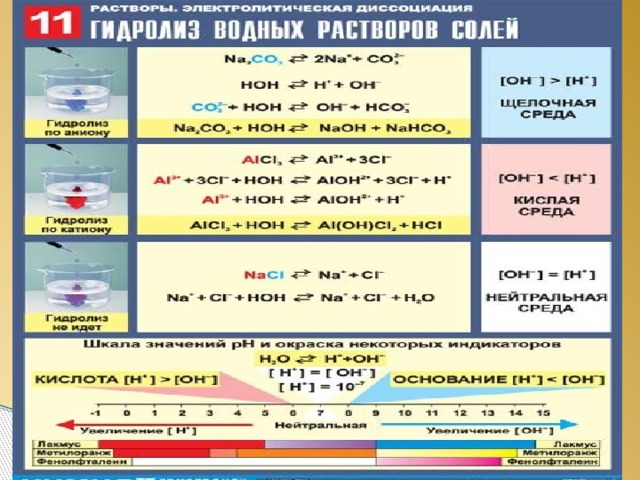
1. Соли, образованные катионом сильного основания и анионом слабой кислоты, подвергаются гидролизу по аниону , среда раствора щелочная:
Na 2 S ↔ 2Na + +S -2
S -2 + Н + ОН – ↔ Н + S -2 + ОН –

2. Соли, образованные катионом слабого основания и анионом сильной кислоты, подвергаются гидролизу по катиону. Их растворы имеют кислую среду, рН
FeCl 2 ↔Fe +2 +2Cl -
Fe +2 +Н + ОН – ↔(FeOH) + + Н +

3.Соли, образованные катионом слабого основания и анионом слабой кислоты, подвергаются гидролизу по катиону и аниону одновременно. Среда их растворов может быть нейтральной, слабо щелочной и слабо кислотной в зависимости от константы диссоциации образующихся продуктов.
- ZnCO 3 ↔Zn 2+ +CO 3 2-
- Zn +2 + Н + ОН – ↔ (Zn OH) + + Н +
- CO 3 2- +Н + ОН – ↔ Н + CO 3 - +ОН –

4.Соли, образованные катионом сильного основания и анионом сильной кислоты не подвергаются гидролизу. Их растворы имеют нейтральную среду, окраска индикаторов в таких растворах не меняется.

Необратимый гидролиз
- Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
слаб.основ-е слаб.к-та
Al(OH)3 H2S
CaC2 + 2H2O = Ca(OH)2 + C2H2
ацетилен
– Соли, образованные слабым основанием и слабой летучей кислотой, подвергаются необратимому гидролизу, т.е. полностью разлагаются с образованием осадка и выделением газа.

Гидролиз органических соединений и его практическое значение
Получение гидролизного спирта:
(С 6 Н10О 5 )n + nН2О nС 6 Н12О 6
ЦЕЛЛЮЛОЗА
(опилки, щепа)
С 6 Н12О 6 2С2Н5ОН + 2 СО2
этанол
ферменты

Гидролиз органических соединений и его практическое значение
Получение мыла:
Жиры + вода мыло + глицерин
(низкого качества)
Обменные процессы в организме:
АТФ + вода АДФ + Н3РО4 + 40 кДж
сода

№ 1. Верны ли утверждения?
1.В чистой воде рН=7.
2.Раствор соляной кислоты – слабый электролит
3.Соль Na 2 CO 3 образована сильным основанием и слабой кислотой.
4.Соль AlCl 3 образована слабым основанием и сильной кислотой.

№ 2.Установите соответствие между формулой соли и отношением ее к гидролизу.
ФОРМУЛА СОЛИ ОТНОШЕНИЕ К ГИДРОЛИЗУ
А) NaNO 3 1) гидролизуется по катиону
Б) HgF 2 2) гидролизуется по аниону
В) Fe(NO 3 ) 3 3) гидролизуется по катиону и аниону
Г) Ca(CH 3 COO) 2 4) не гидролизуется
А
Б
В
Г

№ 3. Установите соответствие между солью и окраской лакмуса в ее растворе.
СОЛЬ ОКРАСКА ЛАКМУСА
А) NH 4 NO 3 1) синяя
Б) K 2 SO 4 2) красная
В) CaCO 3 3) фиолетовая
Г) BaBr 2
А
Б
В
Г

Домашнее задание:
§16, упражнение №1 и2 устно
№ 3 письменно

Спасибо за урок!








































