
Тема урока:
КИСЛОТЫ

ЦЕЛИ УРОКА:
- дать определение кислотам,
- рассмотреть состав кислот,
- классифицировать кислоты,
- ознакомиться с формулами и названиями основных неорганических кислот.

Кислоты в животном мире
Есть в муравьях и крапиве невинная,
С пользой для нас – кислота муравьиная.
Жжет она кожу, но есть в ней и прок –
Ваш ревматизм она вылечит в срок.
Голожаберные моллюски в порядке самообороны выстреливают парами серной кислоты
Тропический паук педипальпида
стреляет во врагов струйкой жидкости,
содержащей 84% уксусной кислоты .

Кислоты в растительном мире
Лишайники выделяют кислоты,
которые разрушают
горные породы
Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито, что мухомору незачем прятаться.
Очень популярен в народе щавель,
который содержит щавелевую кислоту

Кислоты в организме человека
Аскорбиновая кислота
Молочная кислота
соляная кислота

Прочитайте формулы кислот. H Cl , H 2 S O 4 , H 3 P O 4
Что общего во всех этих формулах?
все общие свойства кислот
связаны с элементом водородом.
Остальная часть молекулы называется кислотным остатком .
Заряд кислотного остатка определяется числом атомов водорода в кислоте
Кислоты HR – это сложные вещества, состоящие из ионов водорода и кислотного остатка.
А чем ещё кроме разных кислотных остатков
отличаются формулы кислот?
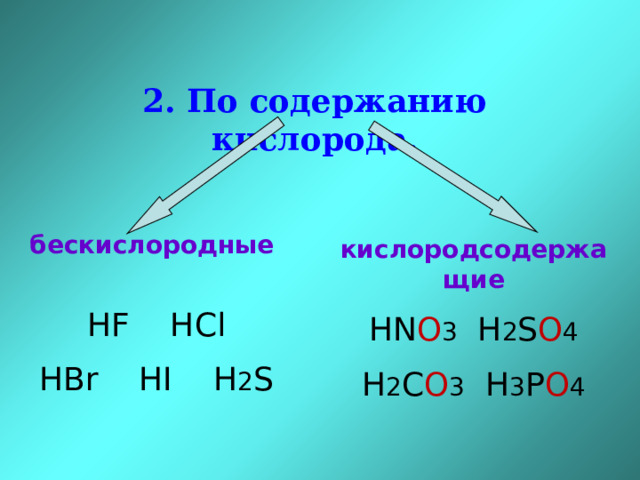
2. По содержанию кислорода.
бескислородные
HF HCl
HBr HI H 2 S
кислородсодержащие
HN O 3 H 2 S O 4
H 2 C O 3 H 3 P O 4
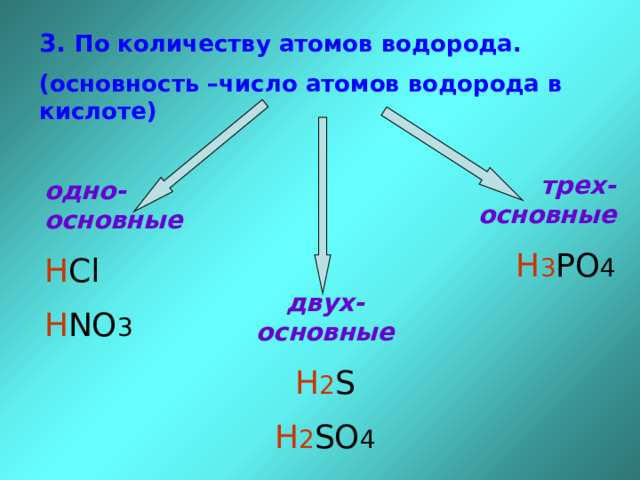
3. По количеству атомов водорода.
(основность –число атомов водорода в кислоте)
трех-основные
H 3 PO 4
одно-основные
H Cl
H NO 3
двух-основные
H 2 S
H 2 SO 4
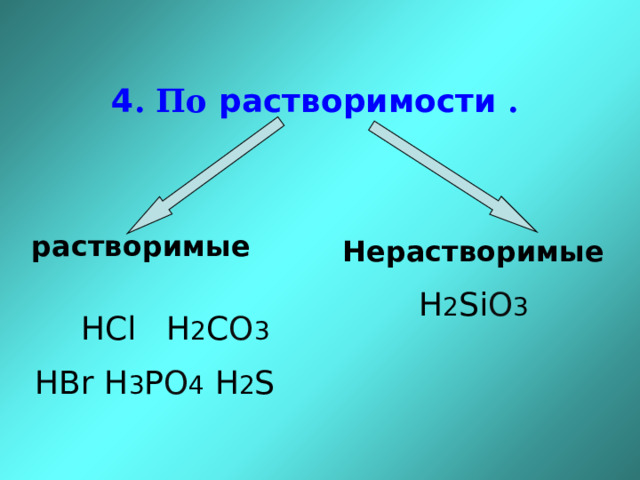
4 . По растворимости .
растворимые
HCl H 2 C O 3
HBr H 3 P O 4 H 2 S
Нерастворимые
H 2 Si O 3

4. По агрегатному состоянию
и вкусу
- Жидкие ( HCI, H 2 SO 4 )
- Твердые (H 3 PO 4 , H 2 SiO 3 )
- Кислые( большинство)
- Сладкие(салициловая кислота)
- Горькие(никотиновая кислота)

Правила техники безопасности при работе с кислотами: 1. Большинство кислот кислые на вкус, однако пробовать химические вещества на вкус запрещено.
2. Помните! В связи с выделением большого количества теплоты при растворении кислоты
в воде к ней воду добавлять нельзя. В таком случае вода, которая имеет меньшую плотность окажется на поверхности, закипит и её брызги вместе с кислотой, попадут наружу.
В случае попадания кислоты на кожу следует промыть водой, раствором соды либо мылом.
Сначала вода, потом кислота – иначе будет большая беда!
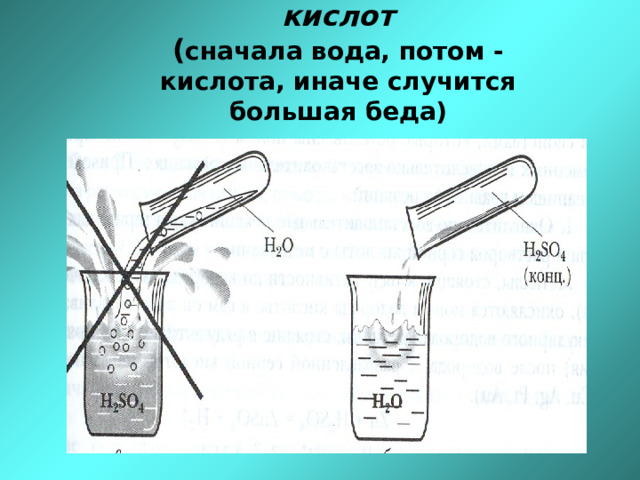
Правило разбавления кислот
( сначала вода, потом - кислота, иначе случится большая беда)

ДЕЙСТВИЕ КИСЛОТ НА ИНДИКАТОРЫ
Индикатор
лакмус
Окраска индикатора в воде
фиолетовый
Фенолфталеин
Окраска индикатора в растворе соляной кислоты (HCl)
Окраска индикатора в серной кислоте
красная
бесцветная
Метилоранж
красная
бесцветная
желтая
бесцветная
розовый
розовый
Вывод : в растворах кислот индикаторы изменяют свой цвет одинаково ( определяют ионы водорода); а это означает, что все кислоты обладают сходными свойствами .
С помощью какого индикатора нельзя обнаружить кислоту?

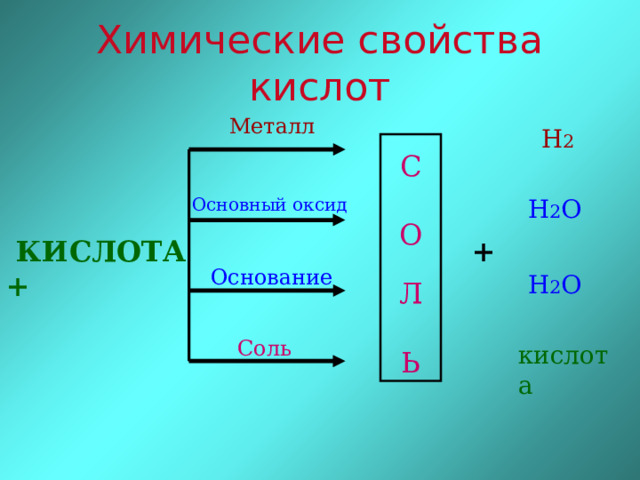
Химические свойства кислот
Металл
Н 2
С
О
Л
Ь
Н 2 О
Основный оксид
+
КИСЛОТА +
Основание
Н 2 О
Соль
кислота

Химические свойства кислот взаимодействие с металлами
Кислота + металл = соль + водород
Ряд активности металлов:
Li K Ba Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
Активность металлов уменьшается
Опыт 1. Взаимодействие магния с соляной кислотой
Опыт 2. Взаимодействие цинка с соляной кислотой
Опыт 3. Взаимодействие меди с соляной кислотой

Химические свойства кислот
взаимодействие с основными
оксидами
Кислота + основной оксид = соль + вода
Опыт. Взаимодействие оксида меди(II) с серной кислотой.

Химические свойства кислот
взаимодействие с основаниями
Кислота + основнование = соль + вода
Опыт 1. Взаимодействие гидроксида калия с соляной кислотой.
Опыт 2. Взаимодействие гидроксида меди (II) с соляной кислотой.

Химические свойства кислот
Взаимодействие с солями слабых кислот
Кислота 1 + соль 1 = соль 2 + Кислота 2
Опыт 1. Взаимодействие хлорида бария с серной кислотой.
Опыт 2. Взаимодействие карбоната натрия с соляной
кислотой.

Закрепление знаний
- Про какие химические свойства кислот вы сегодня узнали, перечислить.
- Какими правилами нужно пользоваться при работе с кислотами.
- Как правильно смешивать кислоту с водой

Тест по теме «КИСЛОТЫ»

1. Выберите группу веществ, в которой указаны только формулы кислот .
а) НСL, H 2 O, H 2 CO 3
б) НСL, HNO 3 , H 2 CO 3
в) NaСL, H 3 PO 4 , H 2 SO 3
ВЕРНО!
НЕВЕРНО!

2. Выберите группу, в которой указаны формулы только кислородсодержащих кислот
а)НС L, Н 2 SО 4 , НNO 3
б)Н 2 SО 4, НNO 3 , Н 3 PO 4б
в)НС L, Н 2 S , НNO 3
НЕВЕРНО!
ВЕРНО!

3. Выберите группу, в которой указаны формулы только одноосновных кислот
а) НСL, Н NO 3, НFа
б) Н 2 SО 4, Н 3 PO 4 , Н 2 S
в) Н 3 PO 4 , НСL, НNO 3
НЕВЕРНО!
ВЕРНО!

4. Под действием растворов кислот лакмус синий становится:
а) малиновым
б) не изменяет окраску
в) красным
г) фиолетовым
НЕВЕРНО!
ВЕРНО!

5. «Купоросным маслом» называют:
а)Соляную кислоту HСL
б)Азотную кислоту HNO 3
в)Фосфорную кислоту H 3 PO 4
г)Серную кислоту H 2 SO 4
ВЕРНО!
НЕВЕРНО!

6. При разбавлении кислоты:
а)Воду приливают к кислоте
б)Кислоту приливают к воде
в)Воду и кислоту смешивают одновременно
ВЕРНО!
НЕВЕРНО!

7.Формула оксида, соответствующего H 2 SO 4 ?
- SO 2 2) SO 3 3)SiO 2 4)CO 2
8.Формула кислоты, соответствующей N 2 O 3 ?
1) HNO3 2) HNO 2 3) H 2 SO 4 4) H 3 PO 4





















































