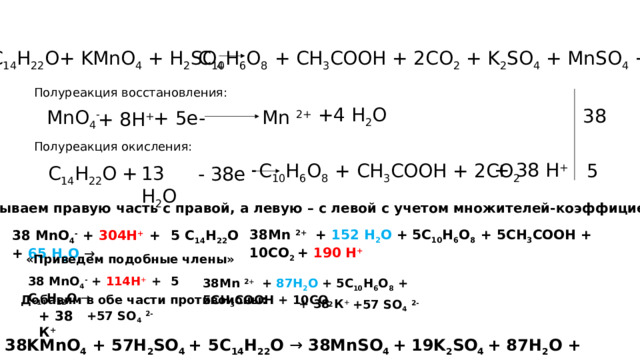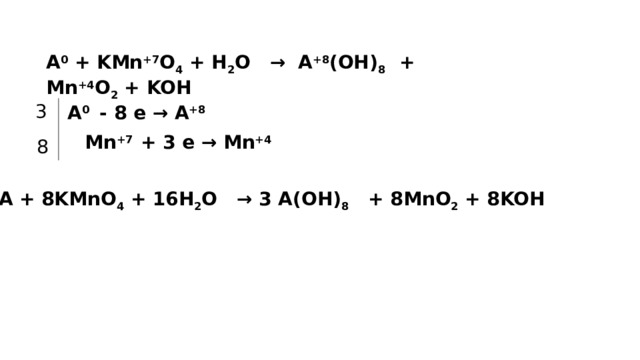Просмотр содержимого документа
«ОВР в органической химии»

ОВР в органической химии
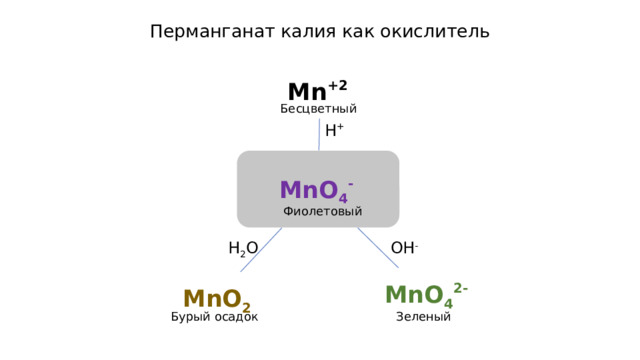
Перманганат калия как окислитель
Mn +2
Бесцветный
H +
MnO 4 -
Фиолетовый
H 2 O
OH -
MnO 4 2-
MnO 2
Бурый осадок
Зеленый
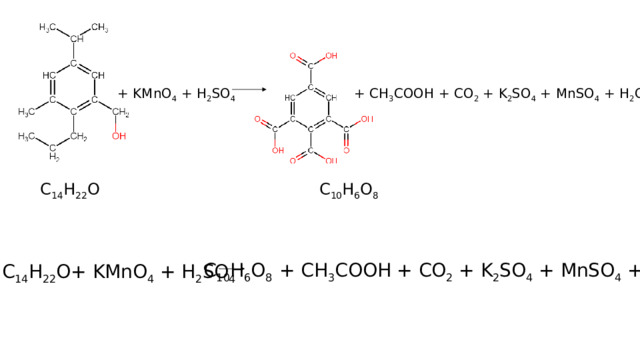
+ KMnO 4 + H 2 SO 4
+ CH 3 COOH + CO 2 + K 2 SO 4 + MnSO 4 + H 2 O
C 14 H 22 O
C 10 H 6 O 8
C 10 H 6 O 8 + CH 3 COOH + CO 2 + K 2 SO 4 + MnSO 4 + H 2 O
C 14 H 22 O+ KMnO 4 + H 2 SO 4
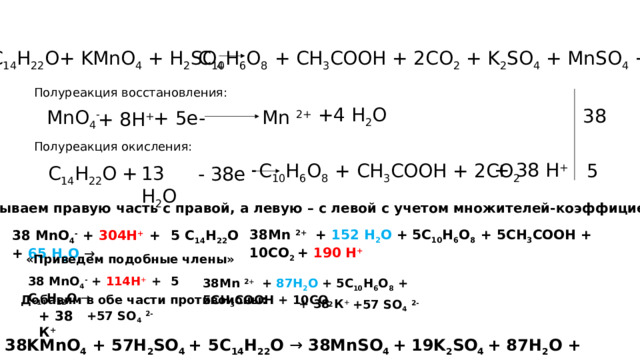
C 10 H 6 O 8 + CH 3 COOH + 2CO 2 + K 2 SO 4 + MnSO 4 + H 2 O
C 14 H 22 O+ KMnO 4 + H 2 SO 4
Полуреакция восстановления:
+
4 H 2 O
38
MnO 4 -
Mn 2+
+ 5е-
+ 8Н +
Полуреакция окисления:
+ 38 Н +
C 10 H 6 O 8 + CH 3 COOH + 2CO 2
5
- 38е -
13 H 2 O
+
C 14 H 22 O
Складываем правую часть с правой, а левую – с левой с учетом множителей-коэффициентов:
38Mn 2+ + 152 H 2 O + 5C 10 H 6 O 8 + 5CH 3 COOH + 10CO 2 + 190 Н +
38 MnO 4 - + 304Н + + 5 C 14 H 22 O + 65 H 2 O →
«Приведем подобные члены»
38 MnO 4 - + 114Н + + 5 C 14 H 22 O →
38Mn 2+ + 87H 2 O + 5C 10 H 6 O 8 + 5CH 3 COOH + 10CO 2
Добавим в обе части противоионы:
+ 38 К +
+57 SO 4 2-
+ 38 К +
+57 SO 4 2-
38KMnO 4 + 57H 2 SO 4 + 5C 14 H 22 O → 38MnSO 4 + 19K 2 SO 4 + 87H 2 O + 5C 10 H 6 O 8 + 5CH 3 COOH + 10CO 2
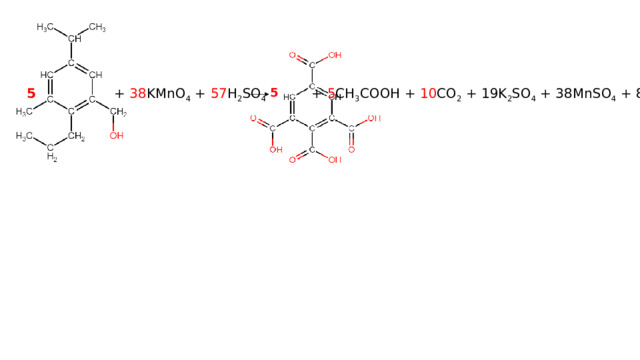
+ 38 KMnO 4 + 57 H 2 SO 4
+ 5 CH 3 COOH + 10 CO 2 + 19K 2 SO 4 + 38MnSO 4 + 87H 2 O
5
5
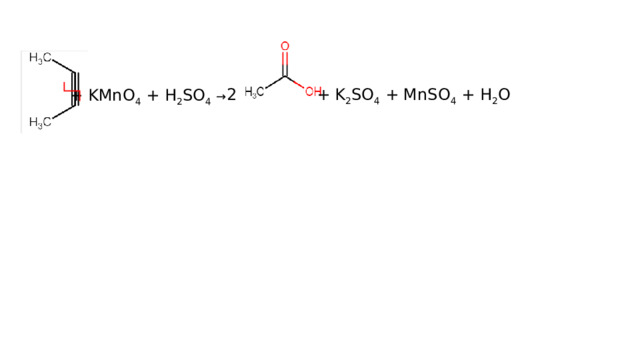
2
+ K 2 SO 4 + MnSO 4 + H 2 O
+ KMnO 4 + H 2 SO 4 →
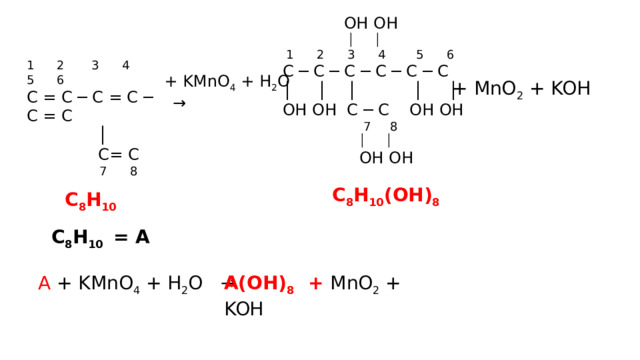
ОН ОН
│ │
1 2 3 4 5 6
С ─ С ─ С ─ С ─ С ─ С
│ │ │ │ │
ОН ОН С ─ С ОН ОН
7 8
│ │
ОН ОН
1 2 3 4 5 6
С = С ─ С = С ─ С = С
│
С= С
7 8
+ KMnO 4 + H 2 O →
+ MnO 2 + KOH
С 8 Н 10 (ОН) 8
С 8 Н 10
С 8 Н 10 = A
A + KMnO 4 + H 2 O →
A(ОН) 8 + MnO 2 + KOH
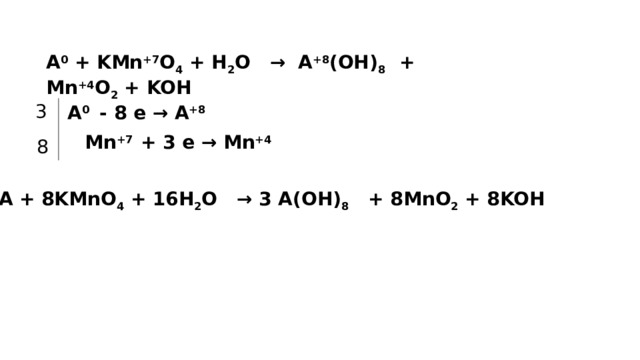
A 0 + KMn +7 O 4 + H 2 O → A +8 (ОН) 8 + Mn +4 O 2 + KOH
3
A 0 - 8 e → A +8
Mn +7 + 3 e → Mn +4
8
3A + 8KMnO 4 + 16H 2 O → 3 A(ОН) 8 + 8MnO 2 + 8KOH
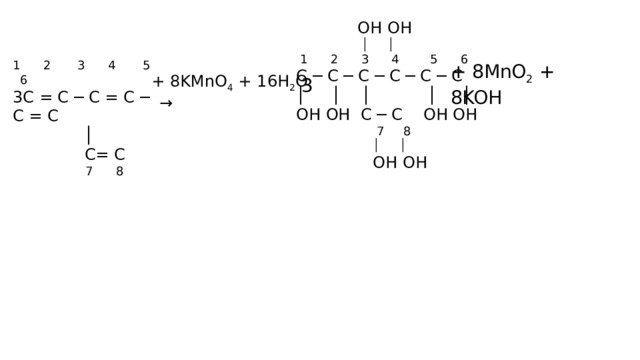
ОН ОН
│ │
1 2 3 4 5 6
С ─ С ─ С ─ С ─ С ─ С
│ │ │ │ │
ОН ОН С ─ С ОН ОН
7 8
│ │
ОН ОН
1 2 3 4 5 6
3С = С ─ С = С ─ С = С
│
С= С
7 8
+ 8MnO 2 + 8KOH
+ 8KMnO 4 + 16H 2 O →
3