Просмотр содержимого документа
«Общая характеристика неметаллов»

Общая характеристика неметаллов

Неметаллические химические элементы широко распространены в земной коре
Кислород и кремний составляют около 76 % (практически три четверти) от массы земной коры (O 2 — 49,4 %, Si — 25,8 %)
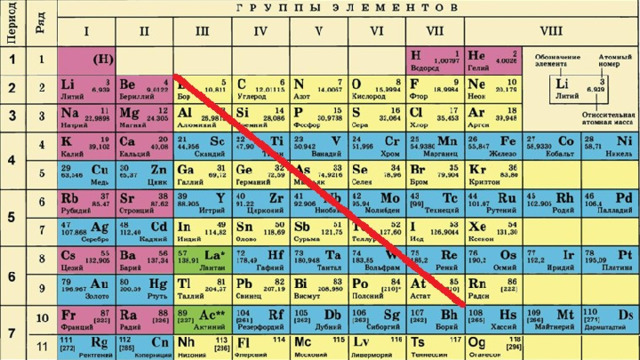

В электронной оболочке атомов неметаллов на внешнем энергетическом уровне, как правило, содержится от 4 до 8 электронов.
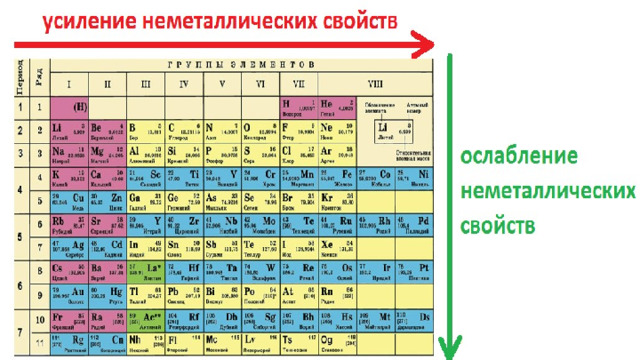

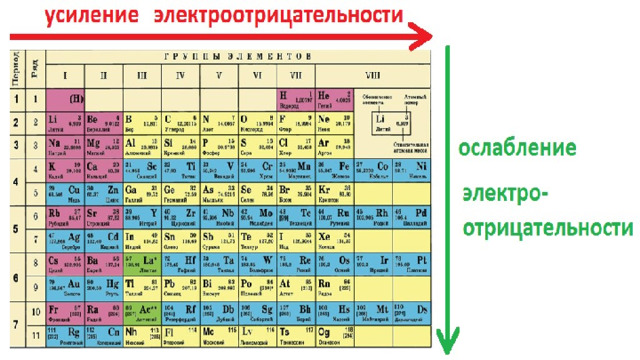
Главное отличительное свойство неметаллов — это их высокая электроотрицательность,
т. е. способность в химических соединениях притягивать электроны.

Физические свойства неметаллов
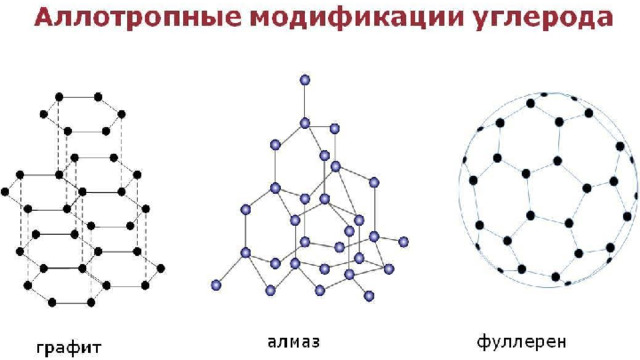
1. Аллотропия — это способность атомов данного химического элемента образовывать несколько простых веществ, называемых аллотропными модификациями.
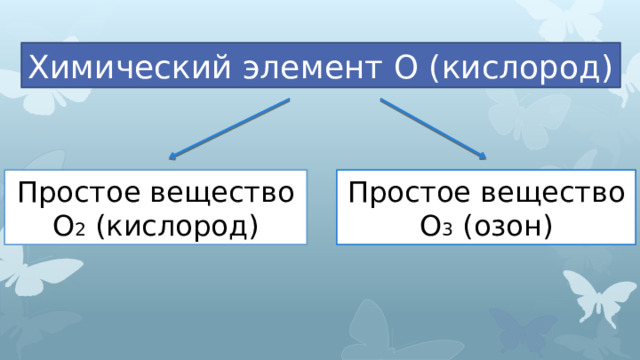
Химический элемент О (кислород)
Простое вещество О 2 (кислород)
Простое вещество О 3 (озон)
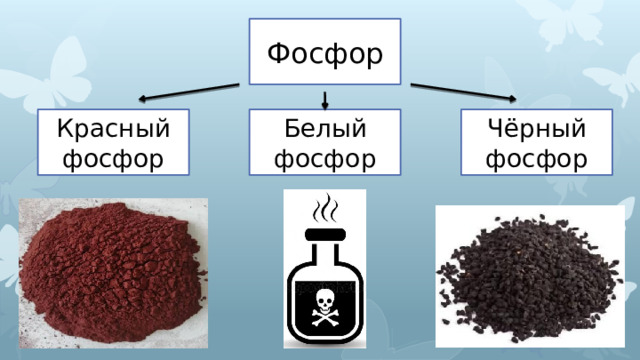
Фосфор
Красный фосфор
Белый фосфор
Чёрный фосфор

2. Агрегатное состояние.
Неметаллы при обычных условиях могут быть газообразными, жидкими и твёрдыми веществами.

Cl 2

Br 2


3. Запах .
Некоторые неметаллы имеют запах.
Например, резкий удушливый запах имеют озон O 3 , фтор F 2 (при попадании в органы дыхания практически моментально разрушает ткани), хлор Cl 2 , бром Br 2 и иод I 2 .

4. Хрупкость
Неметаллы в твёрдом агрегатном состоянии не обладают пластичностью.
Они являются хрупкими

5. Не Электро- и теплопроводность .
Неметаллы, за исключением графита, плохо проводят тепло и практически не проводят электрический ток (являются диэлектриками).

Химические свойства неметаллов
галоген + металл = галогенид металла
2Al + 3I 2 → 2AlI 3 катализатор: вода
2Fe + 3Cl 2 → 2FeCl 3 условия реакции: температура
видео

сера + металл = сульфид металла
2Al + 3S → Al 2 S 3
условия реакции: температура
2Na +S →Na 2 S

Неметалл + водород = летучее водородное соединение
H 2 + Cl 2 → 2HCl
условия реакции: температура
N 2 + 3H 2 ⇄ 2NH 3
условия реакции: температура, давление

Неметалл + кислород = кислотный оксид
S +O 2 → SO 2
4P + 5O 2 → 2P 2 O 5
N 2 + O 2 → 2NO
условия реакции: температура

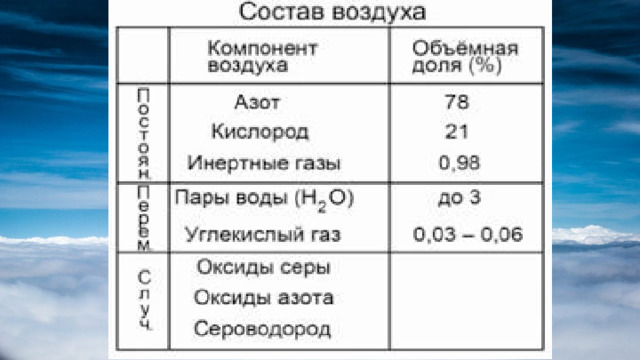
Воздух
Уже в конце 18 века выдающийся химик А. Лавуазье установил, что воздух является смесью газов – азота и кислорода.
В настоящее время выделяют постоянные, переменные и случайные составные части воздуха