Химический состав клетки
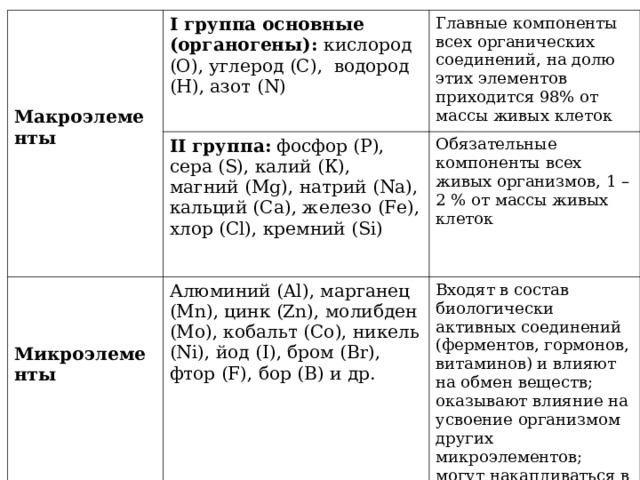
Макроэлементы
I группа основные (органогены): кислород ( O) , углерод (С), водород (H ), азот ( N)
Микроэлементы
Главные компоненты всех органических соединений, на долю этих элементов приходится 98% от массы живых клеток
II группа: фосфор (Р), сера (S) , калий (К), магний ( Mg) , натрий ( Na) , кальций ( Ca) , железо (Fe) , хлор ( Cl ), кремний ( Si)
Обязательные компоненты всех живых организмов, 1 – 2 % от массы живых клеток
Алюминий (Al) , марганец (Mn) , цинк (Zn) , молибден (Mo) , кобальт (Co) , никель (Ni) , йод (I) , бром (Br) , фтор (F) , бор (B) и др.
Входят в состав биологически активных соединений (ферментов, гормонов, витаминов) и влияют на обмен веществ; оказывают влияние на усвоение организмом других микроэлементов; могут накапливаться в живых организмах (например, водоросли накапливают йод, лютики – литий, ряска – радий и др.). Сумарное содержание около 0.1 %

Ультрамикроэлементы
Золото (Au) , бериллий (Be) , серебро (Ag) , уран (U) , ртуть (Hg) , радий (Ra) , селен (Se)
Физиологическая роль этих компонентов в живых организмах пока до конца не изучена, суммарное содержание менее 0,01%

Вода: свойства и функции
Количество воды в клетках костной ткани – 20%
жировой ткани – 40 %
мышечной ткани – 76 %
клетки эмбриона – более 90 %
С возрастом количество воды в клетках снижается!!!!

Свойства воды
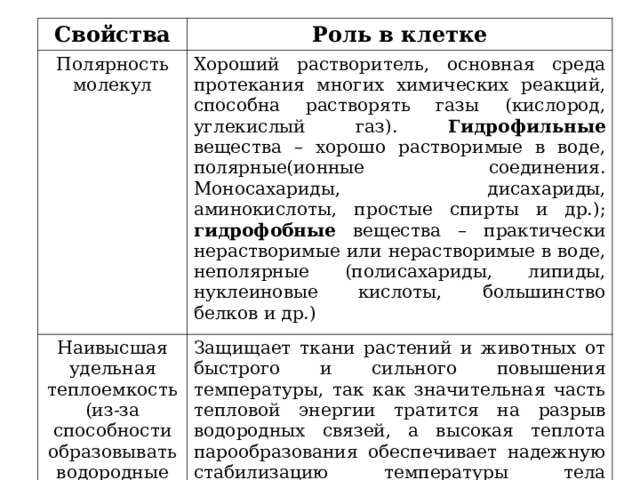
Свойства
Роль в клетке
Полярность молекул
Хороший растворитель, основная среда протекания многих химических реакций, способна растворять газы (кислород, углекислый газ). Гидрофильные вещества – хорошо растворимые в воде, полярные(ионные соединения. Моносахариды, дисахариды, аминокислоты, простые спирты и др.); гидрофобные вещества – практически нерастворимые или нерастворимые в воде, неполярные (полисахариды, липиды, нуклеиновые кислоты, большинство белков и др.)
Наивысшая удельная теплоемкость (из-за способности образовывать водородные связи между молекулами)
Защищает ткани растений и животных от быстрого и сильного повышения температуры, так как значительная часть тепловой энергии тратится на разрыв водородных связей, а высокая теплота парообразования обеспечивает надежную стабилизацию температуры тела организма. Испарение сопровождается испарением (например, потоотделение у животных, тепловая одышка у собак, транспирация у растений)
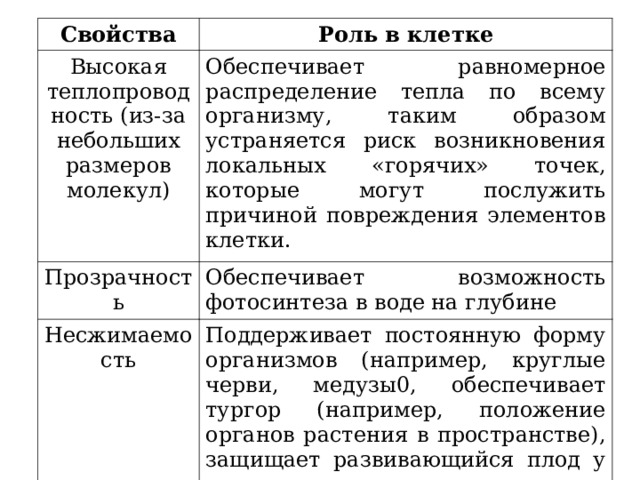
Свойства
Роль в клетке
Высокая теплопроводность (из-за небольших размеров молекул)
Обеспечивает равномерное распределение тепла по всему организму, таким образом устраняется риск возникновения локальных «горячих» точек, которые могут послужить причиной повреждения элементов клетки.
Прозрачность
Обеспечивает возможность фотосинтеза в воде на глубине
Несжимаемость
Поддерживает постоянную форму организмов (например, круглые черви, медузы0, обеспечивает тургор (например, положение органов растения в пространстве), защищает развивающийся плод у млекопитающих
Свойства
Роль в клетке
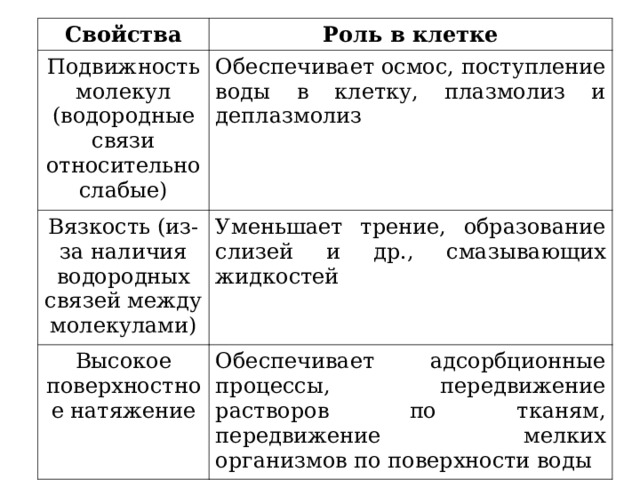
Подвижность молекул (водородные связи относительно слабые)
Обеспечивает осмос, поступление воды в клетку, плазмолиз и деплазмолиз
Вязкость (из-за наличия водородных связей между молекулами)
Уменьшает трение, образование слизей и др., смазывающих жидкостей
Высокое поверхностное натяжение
Обеспечивает адсорбционные процессы, передвижение растворов по тканям, передвижение мелких организмов по поверхности воды

Свойства
Роль в клетке
Расширение при замерзании (каждая молекула воды способна образовывать 4 водородные связи)
Обеспечивает теплоизоляцию организмов в воде в зимнее время (вода имеет максимальную плотность при 4 градусах, лед легче воды и поэтому плавает на ее поверхности)
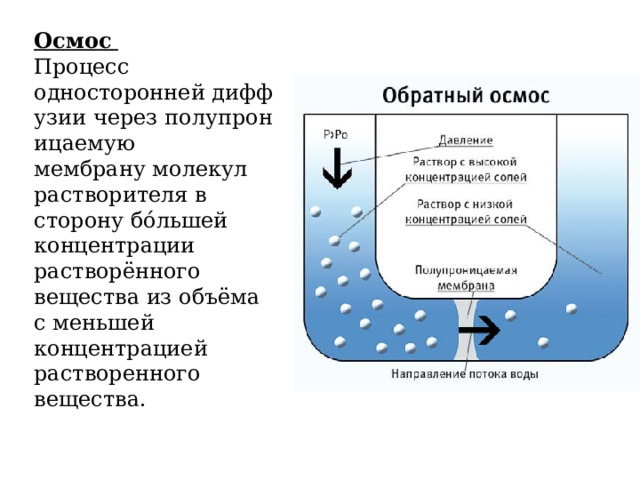
Осмос
Процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества из объёма с меньшей концентрацией растворенного вещества.



Минеральные соли: функции
Функция
Значение
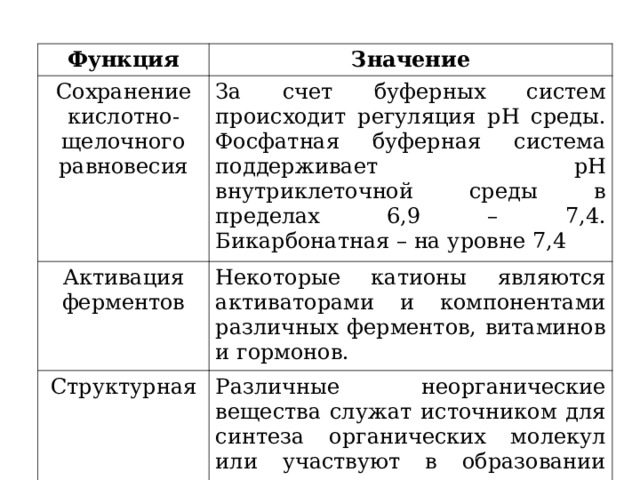
Сохранение кислотно-щелочного равновесия
За счет буферных систем происходит регуляция pH среды. Фосфатная буферная система поддерживает pH внутриклеточной среды в пределах 6,9 – 7,4. Бикарбонатная – на уровне 7,4
Активация ферментов
Некоторые катионы являются активаторами и компонентами различных ферментов, витаминов и гормонов.
Структурная
Различные неорганические вещества служат источником для синтеза органических молекул или участвуют в образовании внутреннего и наружного скелета организмов
Функция
Значение
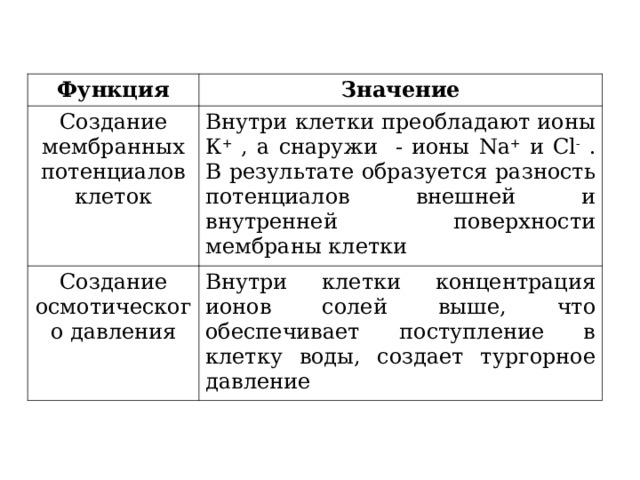
Создание мембранных потенциалов клеток
Внутри клетки преобладают ионы К + , а снаружи - ионы Na + и Cl - . В результате образуется разность потенциалов внешней и внутренней поверхности мембраны клетки
Создание осмотического давления
Внутри клетки концентрация ионов солей выше, что обеспечивает поступление в клетку воды, создает тургорное давление

БИОПОЛИМЕРЫ

Биологические полимеры – высокомолекулярные
органические соединения, молекулы которых состоят из
большого числа повторяющихся звеньев – мономеров.
Сюда относятся:
- Белки – состоят из аминокислот
- Нуклеиновые кислоты – состоят из нуклеотидов
- Полисахариды – состоят из моносахаридов
По форме биополимеры делятся на 2 группы:
- Линейные – белки, нуклеиновые кислоты, целлюлоза
- Ветвящиеся – гликоген, крахмал
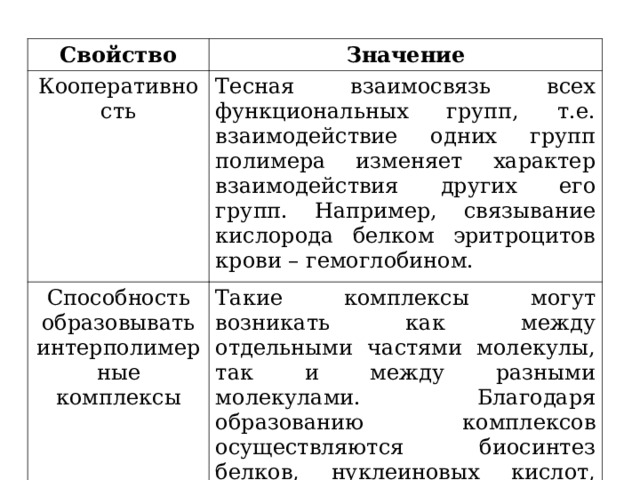
Свойство
Значение
Кооперативность
Тесная взаимосвязь всех функциональных групп, т.е. взаимодействие одних групп полимера изменяет характер взаимодействия других его групп. Например, связывание кислорода белком эритроцитов крови – гемоглобином.
Способность образовывать интерполимерные комплексы
Такие комплексы могут возникать как между отдельными частями молекулы, так и между разными молекулами. Благодаря образованию комплексов осуществляются биосинтез белков, нуклеиновых кислот, регуляция обмена веществ и др. биологические процессы.

УГЛЕВОДЫ
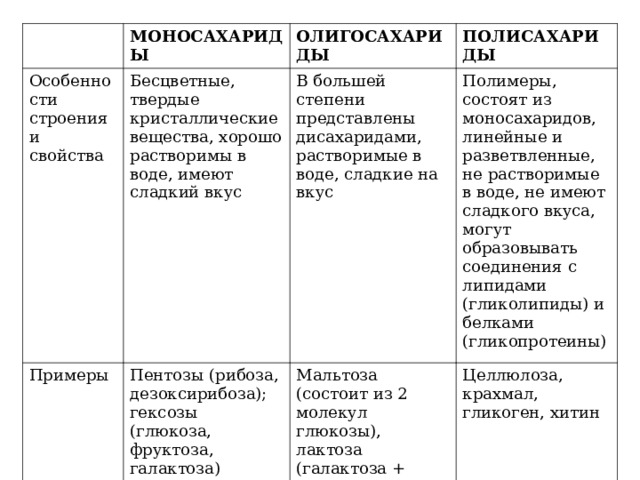
МОНОСАХАРИДЫ
Особенности строения и свойства
Бесцветные, твердые кристаллические вещества, хорошо растворимы в воде, имеют сладкий вкус
Примеры
ОЛИГОСАХАРИДЫ
Пентозы (рибоза, дезоксирибоза); гексозы (глюкоза, фруктоза, галактоза)
ПОЛИСАХАРИДЫ
В большей степени представлены дисахаридами, растворимые в воде, сладкие на вкус
Полимеры, состоят из моносахаридов, линейные и разветвленные, не растворимые в воде, не имеют сладкого вкуса, могут образовывать соединения с липидами (гликолипиды) и белками (гликопротеины)
Мальтоза (состоит из 2 молекул глюкозы), лактоза (галактоза + глюкоза), сахароза (глюкоза+фруктоза)
Целлюлоза, крахмал, гликоген, хитин

МОНОСАХАРИДЫ
Функции
ОЛИГОСАХАРИДЫ
- Энергетическая – основной источник энергии, при полном расщеплении 1 г глюкозы освобождается 17,6 кДж энергии.
- Запасающая – крахмал (у растений) и гликоген (у животных и грибов)
- Строительная – входят в состав нуклеиновых кислот, клеточных мембран, клеточных стенок растений и грибов
- Рецепторная – гликопротеины, которые входят в состав клеточных мембран, обеспечивают узнавание клетками друг друга
- Защитная – растворы углеводов защищают от механических повреждений ткани и органы
ПОЛИСАХАРИДЫ

ЛИПИДЫ
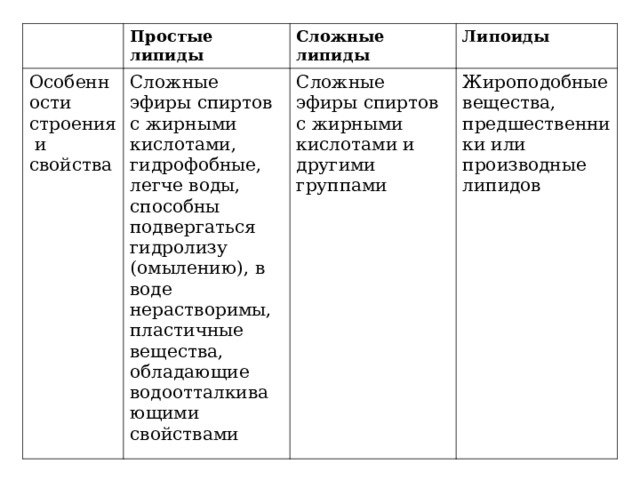
Простые липиды
Особенности строения и свойства
Сложные эфиры спиртов с жирными кислотами, гидрофобные, легче воды, способны подвергаться гидролизу (омылению), в воде нерастворимы, пластичные вещества, обладающие водоотталкивающими свойствами
Сложные липиды
Липоиды
Сложные эфиры спиртов с жирными кислотами и другими группами
Жироподобные вещества, предшественники или производные липидов
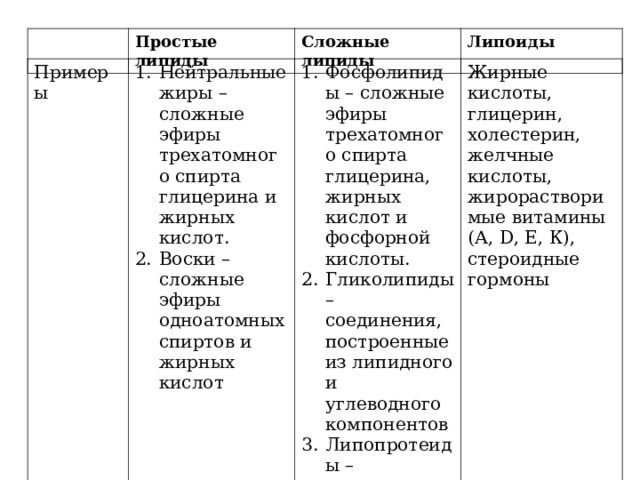
Простые липиды
Сложные липиды
Липоиды
Примеры
- Нейтральные жиры – сложные эфиры трехатомного спирта глицерина и жирных кислот.
- Воски – сложные эфиры одноатомных спиртов и жирных кислот
- Фосфолипиды – сложные эфиры трехатомного спирта глицерина, жирных кислот и фосфорной кислоты.
- Гликолипиды – соединения, построенные из липидного и углеводного компонентов
- Липопротеиды – комплексы липидов и белков
Жирные кислоты, глицерин, холестерин, желчные кислоты, жирорастворимые витамины (А, D , Е, К), стероидные гормоны
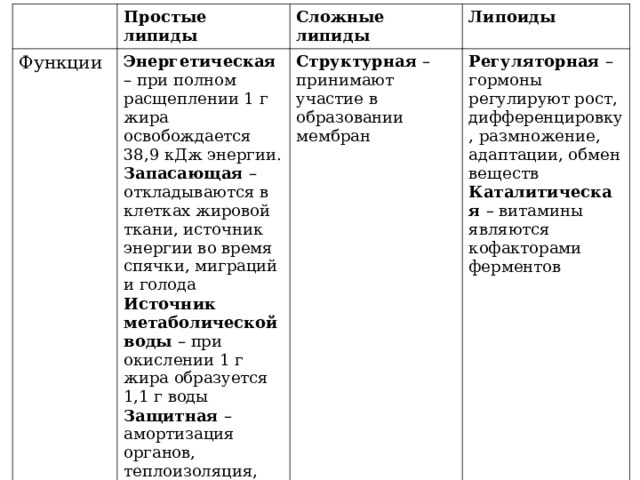
Простые липиды
Функции
Сложные липиды
Энергетическая – при полном расщеплении 1 г жира освобождается 38,9 кДж энергии.
Запасающая – откладываются в клетках жировой ткани, источник энергии во время спячки, миграций и голода
Источник метаболической воды – при окислении 1 г жира образуется 1,1 г воды
Защитная – амортизация органов, теплоизоляция, воск образует водоотталкивающее покрытие предохраняя от смачивания
Липоиды
Структурная – принимают участие в образовании мембран
Регуляторная – гормоны регулируют рост, дифференцировку, размножение, адаптации, обмен веществ
Каталитическая – витамины являются кофакторами ферментов

БЕЛКИ

Белки – биологические гетерополимеры, мономерами
которых являются аминокислоты .
В образовании белков участвует 20 аминокислот!!!
Из них 8 являются для человека незаменимыми , так как не могут синтезироваться в организме и должны поступать с пищей , - это ЛИЗИН, ВАЛИН, ЛЕЙЦИН, ИЗОЛЕЙЦИН, ТРЕОНИН, ФЕНИЛАЛАНИН, ТРИПТОФАН и МЕТИОНИН.
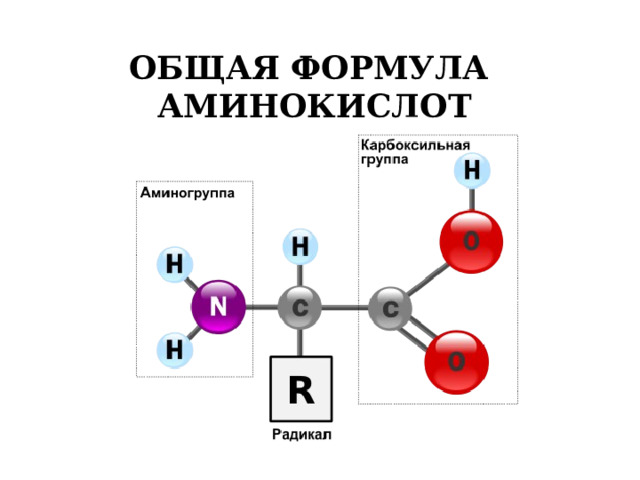
ОБЩАЯ ФОРМУЛА
АМИНОКИСЛОТ

Образование пептидной связи ( ковалентные полярные связи )


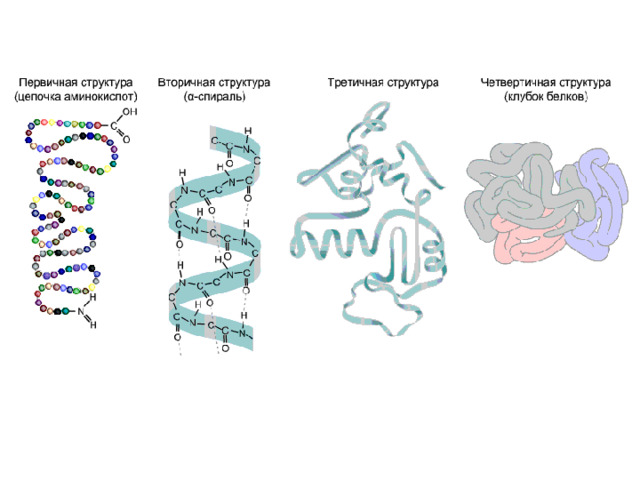
Структуры белковой молекулы
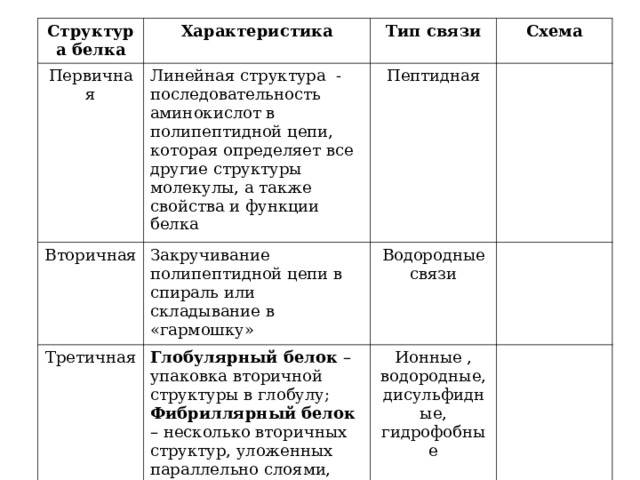
Структура белка
Характеристика
Первичная
Линейная структура - последовательность аминокислот в полипептидной цепи, которая определяет все другие структуры молекулы, а также свойства и функции белка
Вторичная
Тип связи
Закручивание полипептидной цепи в спираль или складывание в «гармошку»
Схема
Пептидная
Третичная
Водородные связи
Глобулярный белок – упаковка вторичной структуры в глобулу;
Фибриллярный белок – несколько вторичных структур, уложенных параллельно слоями, или скручивание нескольких вторичных структур наподобие каната в суперспираль
Ионные , водородные, дисульфидные, гидрофобные
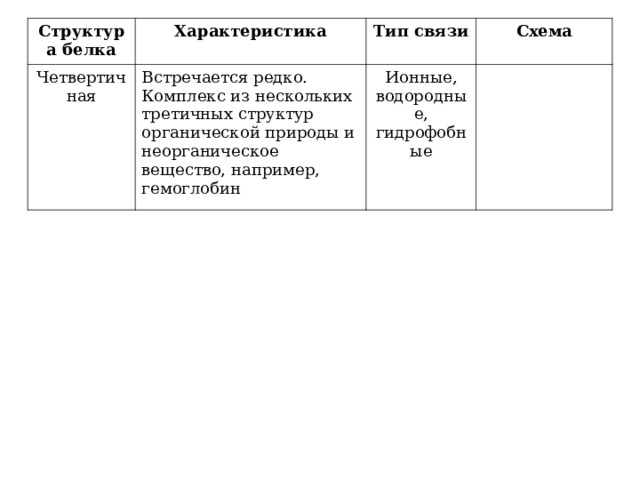
Структура белка
Характеристика
Четвертичная
Встречается редко. Комплекс из нескольких третичных структур органической природы и неорганическое вещество, например, гемоглобин
Тип связи
Схема
Ионные, водородные, гидрофобные

Свойства белков

Физические и химические свойства белков обусловлены их различным аминокислотным составом.
ДЕНАТУРАЦИЯ – нарушение природной структуры белка, происходит под влиянием различных факторов: высокая температура, действия химических веществ, облучение, механическое воздействие
Если воздействие перечисленных факторов было недолгим и несильным, то белок может вернуть свою природную структуру – ОБРАТИМАЯ ДЕНАТУРАЦИЯ (РЕНАТУРАЦИЯ)

Если воздействие было долгим или сильным, то происходит нарушение не только третичной и вторичной структур, но и первичной– НЕОБРАТИМАЯ ДЕНАТУРАЦИЯ (РЕНАТУРАЦИЯ)


ФЕРМЕНТЫ (ЭНЗИМЫ)

ФЕРМЕНТЫ (ЭНЗИМЫ) – это специфические белки, которые присутствуют во всех живых организмах и играют роль биологических катализаторов.
Ферменты ускоряют реакцию без изменения ее общего результата за счет снижения энергии активации, т.е. в их присутствии требуется значительно меньше энергии для придания реакционной способности молекулам, которые вступают в реакцию.
Фермент катализирует только одну реакцию или действует только на один тип связи (высокая специфичность ферментов)

Классификация ферментов

ГРУППА
Катализируемые реакции, примеры
ОКСИДОРЕДУКТАЗЫ
Окислительно-восстановительные реакции: перенос атомов водорода и кислорода и электронов от одного вещества к другому, при этом окисляется первый и восстанавливается второй. Участвуют во всех процессах биологического окисления, например. В дыхании: АН+В А+ВН (окислительный) или
А+О АО (восстановительный)
ТРАНСФЕРАЗЫ
Перенос группы атомов (метильной, ацильной, фосфатной или аминогруппы) от одного вещества к другому. Например, перенос остатков фосфорной кислоты от АТФ на глюкозу или фруктозу под действием фототрансфераз:
АТФ+глюкоза глюкозо-6-фосфат+АДФ
ГИДРОЛАЗЫ
Реакции расщепления сложных органических соединений на более простые путем присоединения молекул воды в месте разрыва химической связи (гидролиз). Например, амилаза (гидролизирует крахмал), липаза (расщепляет жиры), трипсин (расщепляет белки) и др.:
АВ + Н 2 О АОН+ВН
ГРУППА
Катализируемые реакции, примеры
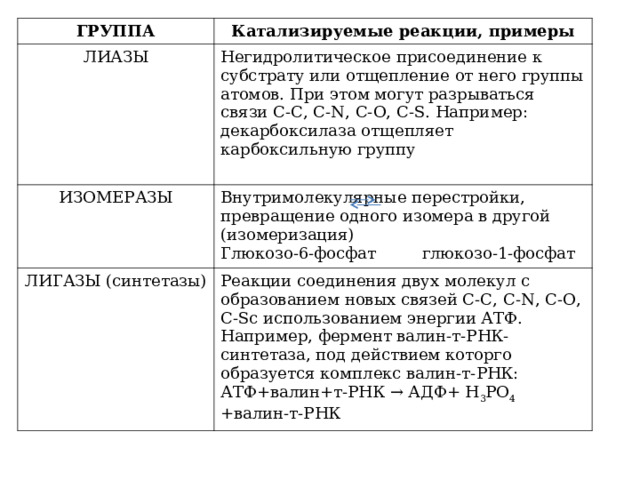
ЛИАЗЫ
Негидролитическое присоединение к субстрату или отщепление от него группы атомов. При этом могут разрываться связи С-С, С -N , С-О, С- S . Например: декарбоксилаза отщепляет карбоксильную группу
ИЗОМЕРАЗЫ
Внутримолекулярные перестройки, превращение одного изомера в другой (изомеризация)
Глюкозо-6-фосфат глюкозо-1-фосфат
ЛИГАЗЫ (синтетазы)
Реакции соединения двух молекул с образованием новых связей С-С, С -N , С-О, С- S с использованием энергии АТФ. Например, фермент валин-т-РНК-синтетаза, под действием которго образуется комплекс валин-т-РНК:
АТФ+валин+т-РНК → АДФ+ Н 3 РО 4 +валин-т-РНК