«ВСЯКОЕ ВЕЩЕСТВО –ОТ САМОГО ПРОСТОГО ДО САМОГО СЛОЖНОГО – ИМЕЕТ ТРИ РАЗЛИЧНЫЕ, НО ВЗАИМОСВЯЗАННЫЕ СТОРОНЫ – СВОЙСТВА, СОСТАВ, СТРОЕНИЕ»
Б.М.КЕДРОВ

“ Она вынула из уха одну из тех огромных жемчужин … и …опустила жемчужину в уксус. Наступило молчание, потрясенные гости, замерев, наблюдали, как жемчужина медленно растворяется в крепком уксусе. Вот от нее не осталось и следа, и тогда Клеопатра подняла кубок, покрутила его, взбалтывая уксус, и выпила весь до последней капли”

«Химические свойства карбоновых кислот»

Цель урока: - Продолжить знакомство учащихся с кислородсодержащими соединениями, на примере уксусной и муравьиной кислот; - изучить химические свойства предельных одноосновных карбоновых кислот; - показать сходство и отличие неорганических и органических кислот; - изучить качественные реакции на карбоновые кислоты.


Классификация карбоновых кислот


Генетический ряд кислот

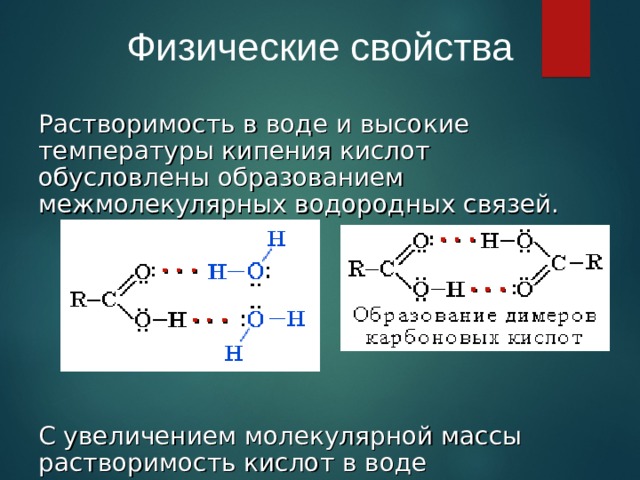
Физические свойства
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
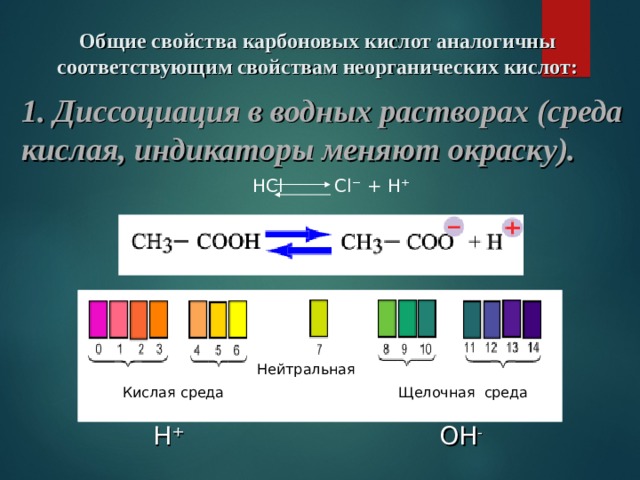
Общие свойства карбоновых кислот аналогичны соответствующим свойствам неорганических кислот:
1. Диссоциация в водных растворах (среда кислая, индикаторы меняют окраску).
НС l С l ⁻ + Н⁺
Нейтральная
Кислая среда
Щелочная среда
Н⁺
ОН -

2. Взаимодействие с металлами (до Н):
2 НС l + Mg = MgCl 2 + H 2
Карбоновые кислоты вступают в реакцию замещения с металлами, стоящими в ряду напряжений до водорода.
2НСООН + Zn = ( НСОО ) 2 Zn + H 2
формиат цинка

3. Взаимодействие с основными оксидами:
2 НС l + С u О = С uCl 2 + H 2 О
2НСООН + С u О = (НСОО) 2 С u + H 2 O
Карбоновые кислоты реагируют с основными оксидами с образованием соли и воды.
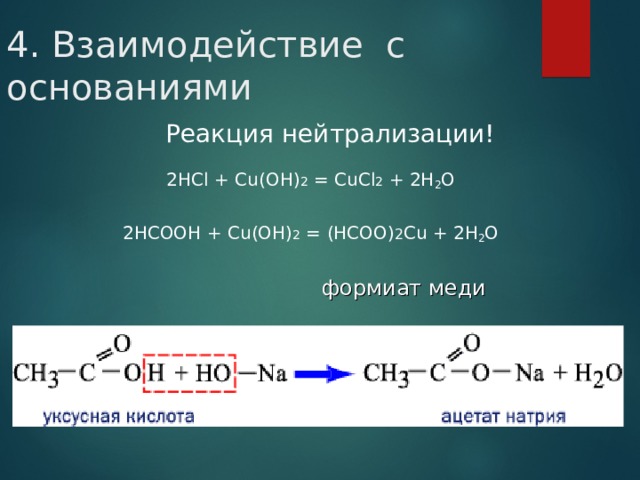
4. Взаимодействие с основаниями
Реакция нейтрализации!
2 НС l + Cu( О H) 2 = CuCl 2 + 2 H 2 О
2 НСООН + Cu( О H) 2 = ( НСОО ) 2 Cu + 2 H 2 O
формиат меди
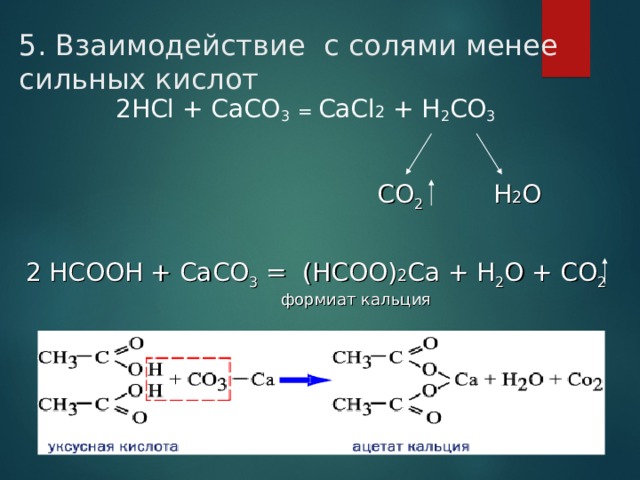
5. Взаимодействие с солями менее сильных кислот
2 НС l + Ca СО 3 = CaCl 2 + H 2 C О 3
СО 2
Н 2 О
2 НСООН + Ca СО 3 = ( НСОО ) 2 Ca + H 2 O + CO 2
формиат кальция
Йорданс Якоб «Пир Клеопатры» 1653
Картина написана на сюжет из «Естественной истории» Плиния Старшего (I в.). Египетская царица Клеопатра (I в. до н. э.), славившаяся красотой и умом, отличалась также экстравагантностью своего поведения. Однажды на глазах своего возлюбленного, римского полководца Марка Антония, Клеопатра растворила в бокале с уксусом крупную жемчужину, а затем выпила его содержимое. На картине изображен момент, когда царица опускает в бокал серьгу, а Марк Антоний, его спутник Энобард и негр-слуга застыли в немом изумлении, всем своим видом выражая сожаление о погибшей ценности и одновременно — восхищение поступком Клеопатры. А вот ухмылка и презрительный жест придворного шута яснее всяких слов говорят о нелепости и глупости подобного расточительства. Картина заставляет вспомнить нравоучительные аллегории Х. Босха и П. Брейгеля Старшего.
Учитель зачитывает отрывок из произведения Г.Р.Хаггарда “Клеопатра”:
“… Она вынула из уха одну их тех жемчужин … и … опустила жемчужину в уксус. Наступило молчание, потрясенные гости, замерев наблюдали, как несравненная жемчужина медленно растворяется в крепком уксусе. Вот от ней осталось и следа, и тогда Клеопатра подняла кубок, покрутила его, взбалтывая уксус, и выпила весь до последней капли…”
Римский историк Плиний-старший в своем труде «Естественная история» рассказывает об эпизоде, когда Клеопатра побилась об заклад с Марком Антонием, что сумеет приготовить самое драгоценное яство из когда-либо подававшихся. Клеопатра сняла одну из своих жемчужных серег (как утверждал Плиний, ценой в баснословные 10 миллионов сестерциев) и опустила ее в чашу кислого вина (уксуса). Жемчуг якобы растворился в уксусе, и Клеопатра выпила чашу до дна, тем самым победив в этой затее.
15
=
–
=
–
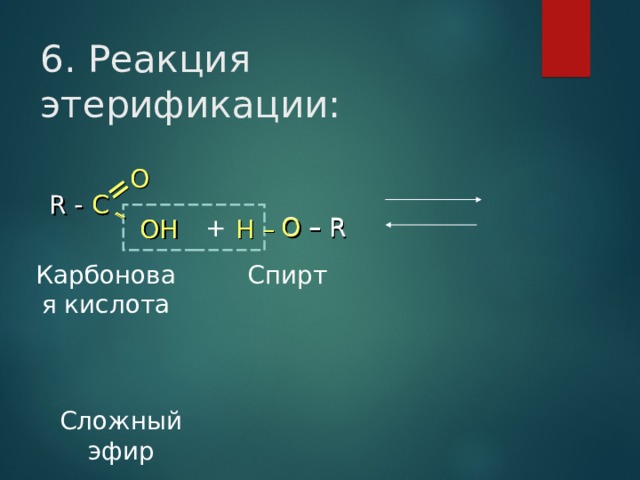
6. Реакция этерификации:
O
O
R - C
R - C
O – R
+
O – R
H –
OH
OH
H –
Карбоновая кислота
Спирт
Сложный эфир

8. Галогенирование
Cl – Cl + CH 3 COOH → Cl CH 2 COOH + HCl
монохлоруксусная кислота
хлор

Муравьиная кислота - это «вещество с двойственной функцией», т.е. содержит два типа функциональных групп. Она является альдегидокислотой.


Мне для консервирования нужно 300 г 3%-ного раствора уксуса. Какой объем воды необходимо добавить к 50 г уксусной эссенции, массовая доля уксусной кислоты в которой равна 70%?

Рефлексия
Если согласны с утверждением, поставьте «+»
- Тема урока вызвала интерес.
- Я с удовольствием работал(а)
- Я вижу практическое применение темы.
- Думаю, что тему урока усвоил(а) на (баллы)

§ 20 , упр. 4,6,7,17

Спасибо за внимание!