Практическая работа «Правила ТБ при работе в химическом кабинете. Ознакомление с лабораторным оборудованием».
1. Штатив. Спиртовка.
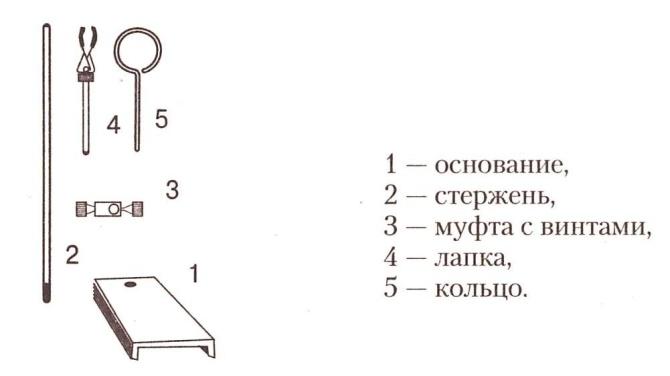
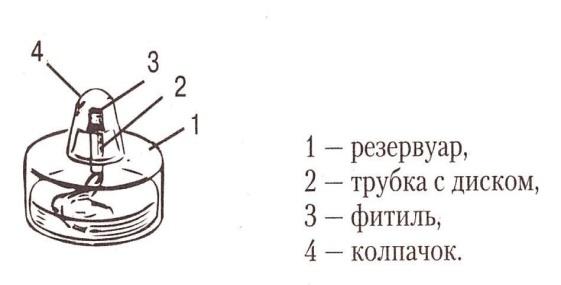
Рассмотрите штатив и спиртовку. Согласно рисункам, определите их составные части.
2.Соблюдая правила ТБ, подожгите спиртовку. Внимательно рассмотрите её пламя. Аккуратно поднесите одну спичку к нижней, вторую - к средней, третью - к внешней части пламени.
Сделайте выводы, результаты оформите в виде таблицы:
| Зона пламени | Цвет пламени | Характеристика температуры | Состав |
| А. Нижняя |
|
|
|
| Б. Средняя |
|
|
|
| В. Внешняя |
|
|
|
3. Соберите лабораторный штатив. Закрепите в нём пробирку с водой. При помощи спиртовки нагрейте воду в пробирке.
Дайте письменные ответы на вопросы: А. В какой части пламени следует нагревать пробирку? Почему? Б. Какие правила ТБ необходимо соблюдать для выполнения этого задания?
Практическая работа. Очистка загрязнённой поваренной соли.
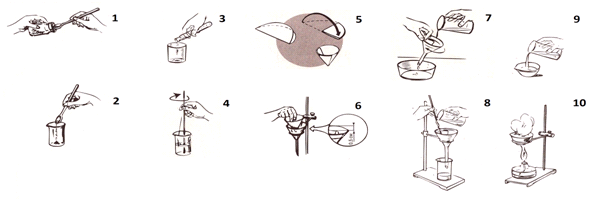
1.Возьмите из банки сухой чистой ложкой загрязнённую поваренную соль. 2. Насыпьте в стакан порцию соли. 3. Добавьте в стакан воды на 1/3 его высоты. 4. Осторожно размешайте содержимое стеклянной палочкой. 5. Приготовьте фильтр как показано на рисунке. 6. Вложите фильтр в воронку так, чтобы он: А) плотно прилегал к стенкам, Б) не доходил до края воронки на 0,5 см. 7. Слегка смочите фильтр водой.
8. Наливайте фильтруемую жидкость на фильтр по стеклянной палочке, направив её нижний конец к стенке воронки, а не в середину фильтра, чтобы не прорвать его. 9. Вылейте фильтрат (раствор соли) в фарфоровую выпаривательную чашку до ½ её объёма. 10. Поставьте чашку на кольцо штатива. Зажгите спиртовку. Нагревайте фильтрат до начала образования кристаллов соли.
11. Оформите в тетради отчёт о работе в виде таблицы:
| Основные операции (что сделано). | Рисунки, наблюдения. | Результаты наблюдений (выводы). |
| Растворение соли в воде. |
|
|
| Фильтрование. |
|
|
| Выпаривание фильтрата (раствора соли). |
|
|
12. Приведите в порядок своё рабочее место: демонтируйте штатив, разместите на своих местах принадлежности и посуду в чистом виде!
Практическая работа. Получение и свойства кислорода.
1. Соберите прибор как показано на рисунке и проверьте его на герметичность.
В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода. 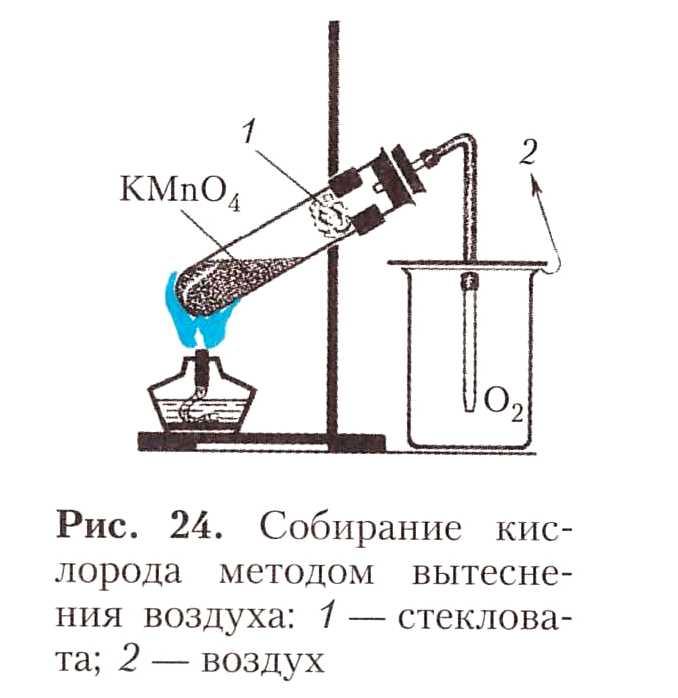
2. Положите в железную ложечку кусочек древесного угля и раскалите его в пламени. Затем ложечку с тлеющим углём внесите в сосуд с кислородом и наблюдайте за происходящим. Запишите уравнение реакции горения угля (С).
Результаты работы оформите в виде таблицы:
| Действия (что делали) | Наблюдения (описание наблюдений) | Уравнения реакций | Выводы |
| 1. |
|
|
|
| 2. |
|
|
|
Практическая работа.
Приготовление растворов солей с определённой массовой долей растворённого вещества.
Задача. Приготовьте 100 граммов раствора поваренной соли в воде, с массовой долей соли 20%.
Инструкция:
1. Вычислите, сколько соли и сколько воды потребуется для приготовления данного раствора.
2. Отмерьте на весах необходимую массу соли и поместите её в стаканчик.
3. Отмерьте необходимый объём воды и влейте её в стакан с солью. Содержимое стакана тщательно перемешайте.
Для оформления работы продолжите предложения:
1. Для вычисления массы соли производились следующие расчёты:
2. Для вычисления массы воды производились следующие расчёты:
3. Необходимая масса соли отмерялась с помощью…
4. Необходимый объём (масса) воды отмерялся с помощью…
5. Выводы. Раствор получили путём ….. Растворителем является …. Растворённым веществом…
Практическая работа.
Решение экспериментальных задач по теме
«Основные классы неорганических соединений».
Инструкция
В вашем распоряжении вещества: универсальный индикатор; растворы хлорида натрия, гидроксида натрия, соляной кислоты, хлорида меди (II); металлический магний.
С помощью имеющихся веществ решите экспериментальные задачи:
Задача 1. Даны растворы следующих веществ: хлорид натрия, гидроксид натрия, соляная кислота.
Как опытным путём можно различить эти вещества?
Задача 2. Из металлического магния получите гидроксид магния.
Осуществите превращения: магний → хлорид магния→ гидроксид магния.
Задача 3. Из хлорида меди (II) получите оксид меди (II).
Осуществите превращения: хлорид меди (II) → гидроксид меди(II) → оксид меди(II).
Результаты работы оформите в виде таблицы:
| Задачи | Действия | Наблюдения | Уравнения реакций | Выводы |
| 1. |
|
|
|
|
| 2. |
|
|
|
|
| 3. |
|
|
|
|
Литература:
Химия. Неорганическая химия. 8 класс. Учебник для общеобразовательных учреждений. Базовый уровень.
Г.Е. Рудзитис, Ф.Г. Фельдман М.: Просвещение 2015.





























