
КАРБОНОВЫЕ
КИСЛОТЫ
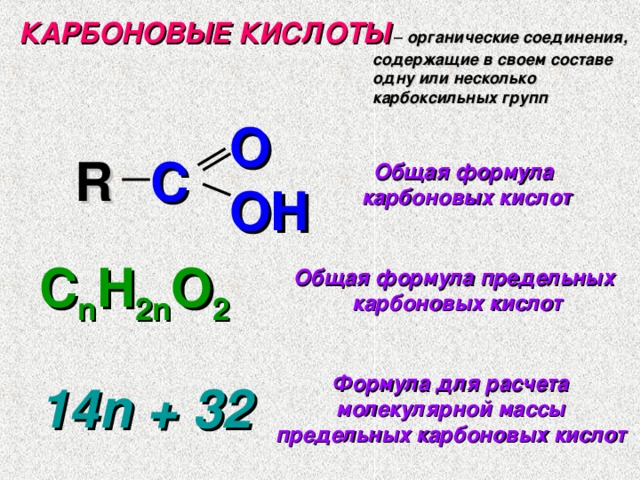
КАРБОНОВЫЕ КИСЛОТЫ органические соединения,
содержащие в своем составе
одну или несколько
карбоксильных групп
O
OH
R
C
Общая формула
карбоновых кислот
С n H 2n O 2
Общая формула предельных
карбоновых кислот
Формула для расчета
молекулярной массы
предельных карбоновых кислот
14n + 32
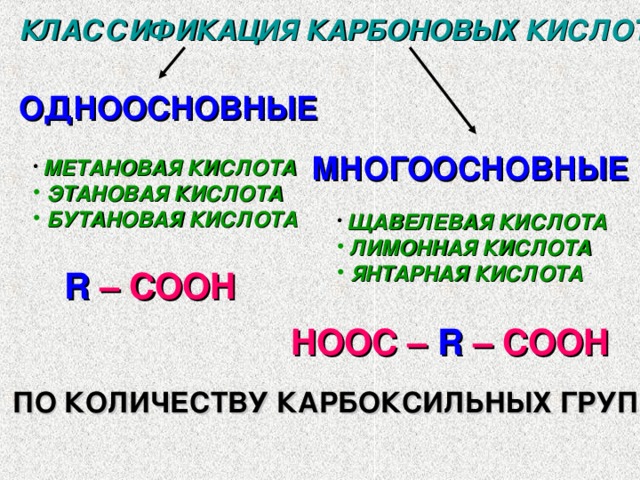
КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ
ОДНООСНОВНЫЕ
МНОГООСНОВНЫЕ
- ЭТАНОВАЯ КИСЛОТА
- БУТАНОВАЯ КИСЛОТА
- ЛИМОННАЯ КИСЛОТА
- ЯНТАРНАЯ КИСЛОТА
R – COOH
HOOC – R – COOH
ПО КОЛИЧЕСТВУ КАРБОКСИЛЬНЫХ ГРУПП
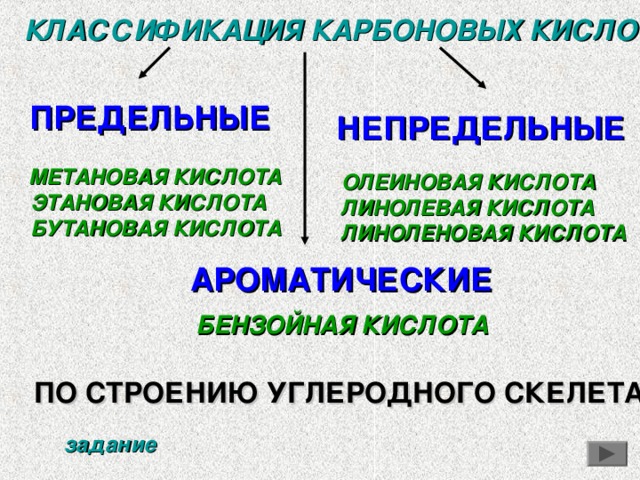
КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ
ПРЕДЕЛЬНЫЕ
НЕПРЕДЕЛЬНЫЕ
МЕТАНОВАЯ КИСЛОТА
ЭТАНОВАЯ КИСЛОТА
БУТАНОВАЯ КИСЛОТА
ОЛЕИНОВАЯ КИСЛОТА
ЛИНОЛЕВАЯ КИСЛОТА
ЛИНОЛЕНОВАЯ КИСЛОТА
АРОМАТИЧЕСКИЕ
БЕНЗОЙНАЯ КИСЛОТА
ПО СТРОЕНИЮ УГЛЕРОДНОГО СКЕЛЕТА
задание

Классифицируйте предложенные кислоты
- СН 3 – СН 2 – СН 2 – СООН
- СН 3 – СН = СН – СООН
- СН 3 – СН(СН 3 ) – СН(СН 3 ) – СООН
- НООС - СН = СН – СН 2 – СООН
- СН 3 – СН = С = СН – СООН
проверить

Классифицируйте предложенные кислоты
- СН 3 – СН 2 – СН 2 – СООН
- СН 3 – СН = СН – СООН
- СН 3 – СН(СН 3 ) – СН(СН 3 ) – СООН
- НООС - СН = СН – СН 2 – СООН
- СН 3 – СН = С = СН – СООН
проверить
ОТВЕТЫ
2. ОДНООСНОВНАЯ НЕПРЕДЕЛЬНАЯ
3. ОДНООСНОВНАЯ ПРЕДЕЛЬНАЯ
4. ДВУХОСНОВНАЯ, НЕПРЕДЕЛЬНАЯ
5. ОДНООСНОВНАЯ, НЕПРЕДЕЛЬНАЯ

ОТВЕТЫ
2. ОДНООСНОВНАЯ НЕПРЕДЕЛЬНАЯ
3. ОДНООСНОВНАЯ ПРЕДЕЛЬНАЯ
4. ДВУХОСНОВНАЯ, НЕПРЕДЕЛЬНАЯ
5. ОДНООСНОВНАЯ, НЕПРЕДЕЛЬНАЯ
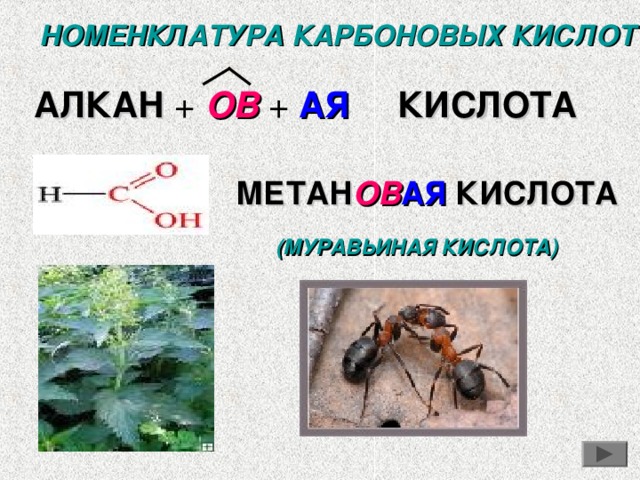
НОМЕНКЛАТУРА КАРБОНОВЫХ КИСЛОТ
АЛКАН + ОВ + АЯ
КИСЛОТА
МЕТАН ОВ АЯ КИСЛОТА
(МУРАВЬИНАЯ КИСЛОТА)

МУРАВЬИНАЯ КИСЛОТА
Н - СООН
Бесцветная жидкость с резким запахом. Получена
в 1831 г Т.Пелузом из синильной кислоты. В ряду
одноосновных карбоновых кислот самая сильная
и самая активная. Муравьиная кислота содержится
в некоторых растениях (крапиве, хвое) и насекомых
(в выделениях муравьев и пчел). Само название -
муравьиная – связано с муравьями, из которых
эта кислота была впервые выделена.По той же
причине жгутся листья крапивы, если их неосторожно
задеть рукой.

Н - СООН
МУРАВЬИНАЯ КИСЛОТА
Бесцветная жидкость с резким запахом. Получена
в 1831 г Т.Пелузом из синильной кислоты. В ряду
одноосновных карбоновых кислот самая сильная
и самая активная. Муравьиная кислота содержится
в некоторых растениях (крапиве, хвое) и насекомых
(в выделениях муравьев и пчел). Само название -
муравьиная – связано с муравьями, из которых
эта кислота была впервые выделена.По той же
причине жгутся листья крапивы, если их неосторожно
задеть рукой.

1
2
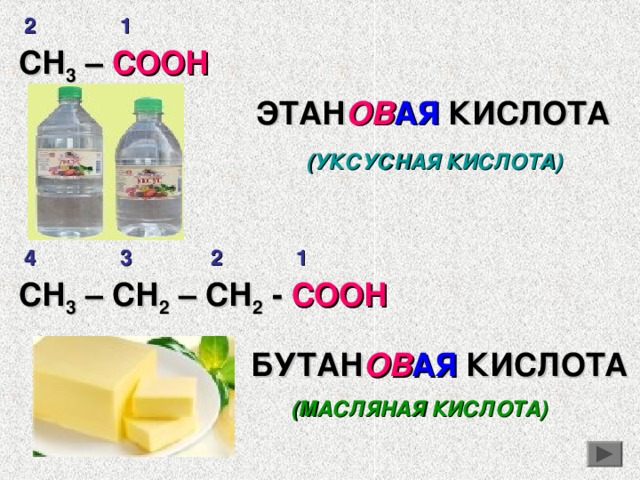
СН 3 – СООН
ЭТАН ОВ АЯ КИСЛОТА
(УКСУСНАЯ КИСЛОТА)
1
2
3
4
СН 3 – СН 2 – СН 2 - СООН
БУТАН ОВ АЯ КИСЛОТА
(МАСЛЯНАЯ КИСЛОТА)
СН 3 - СООН
УКСУСНАЯ КИСЛОТА
Уксусная кислота известна человеку с незапамятных
времен. В чистом виде выделили только в 1700 г. В
1845 г. Ее получил синтетическим путем Г.Кольбе.
Уксусная кислота – бесцветная жидкость с резким
кисловатым запахом. Если кислота не содержит воду,
то при 16,6 0 С она образует бесцветные кристаллы и
называется «ледяной». Водный раствор (70-80 % )
кислоты известен как уксусная эссенция , а 5 – 7 %
раствор называется столовым уксусом . Уксусная
кислота – слабая кислота.

СН 3 - СООН
УКСУСНАЯ КИСЛОТА
Уксусная кислота известна человеку с незапамятных
времен. В чистом виде выделили только в 1700 г. В
1845 г. Ее получил синтетическим путем Г.Кольбе.
Уксусная кислота – бесцветная жидкость с резким
кисловатым запахом. Если кислота не содержит воду,
то при 16,6 0 С она образует бесцветные кристаллы и
называется «ледяной». Водный раствор (70-80 % )
кислоты известен как уксусная эссенция , а 5 – 7 %
раствор называется столовым уксусом . Уксусная
кислота – слабая кислота.

3
5
4
1
2
СН 3 – СН 2 – СН 2 – СН 2 – СООН
ПЕНТАН ОВ АЯ КИСЛОТА
(ВАЛЕРИАНОВАЯ КИСЛОТА)
1
2
НООС – СООН
ЭТАН ДИ ОВ АЯ КИСЛОТА
(ЩАВЕЛЕВАЯ КИСЛОТА)

НООС – СООН
ЩАВЕЛЕВАЯ КИСЛОТА
Щавелевая кислота относится к простейшей
двухосновной кислоте. Впервые эта кислота была
обнаружена в кислом щавеле (конский щавель) в виде
кислой калиевой соли, а в 1776 г. Она была получена
в свободном виде. В 1824г. щавелевую кислоту
синтезировал Ф.Велер при взаимодействии дициана
с водой. Известно, что ни сам Ф.Велер, ни его
c овременники не обратили внимание особого внимания
y а этот синтез. А ведь при этом происходило
превращение неорганического вещества
в органическое !
Ф.Велер

НООС – СООН
ЩАВЕЛЕВАЯ КИСЛОТА
Щавелевая кислота относится к простейшей
двухосновной кислоте. Впервые эта кислота была
обнаружена в кислом щавеле (конский щавель) в виде
кислой калиевой соли, а в 1776 г. Она была получена
в свободном виде. В 1824г. щавелевую кислоту
синтезировал Ф.Велер при взаимодействии дициана
с водой. Известно, что ни сам Ф.Велер, ни его
c овременники не обратили внимание особого внимания
y а этот синтез. А ведь при этом происходило
превращение неорганического вещества
в органическое !
Ф.Велер
1
2
3
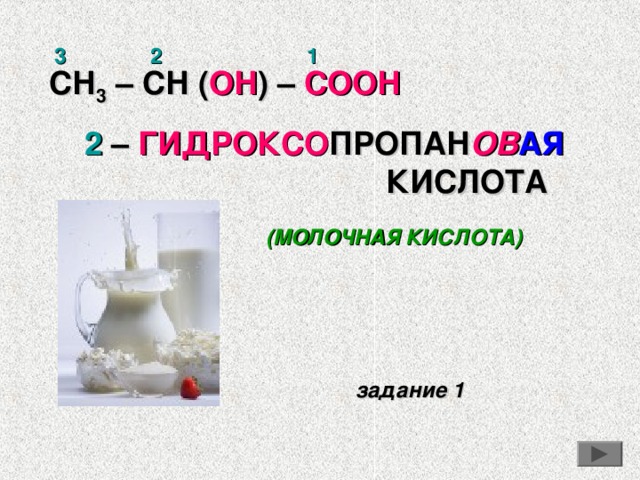
СН 3 – СН ( ОН ) – СООН
2 – ГИДРОКСО ПРОПАН ОВ АЯ
КИСЛОТА
(МОЛОЧНАЯ КИСЛОТА)
задание 1
ДАЙТЕ НАЗВАНИЕ ВЕЩЕСТВАМ
ПО МЕЖДУНАРОДНОЙ НОМЕНКЛАТУРЕ
- СН 3 – СН(СН 3 ) – СООН
- СН 3 – СН 2 – СН(СН 3 ) – СН(СН 3 ) – СООН
- СН 3 – СН = СН – СН(СН 3 ) – СООН
- СН 3 – СН = СН – СН(ОН) – СООН
- НООС – СН 2 – СН(СН 3 ) – СООН
ПРОВЕРИТЬ
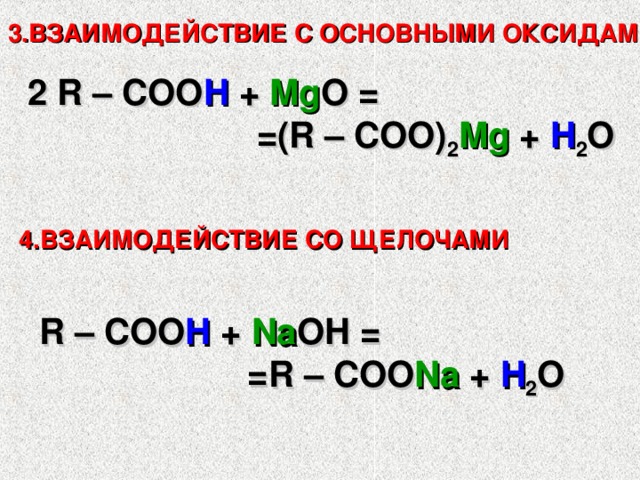
ОТВЕТЫ
- 2 – МЕТИЛПРОПАНОВАЯ КИСЛОТА
- 2, 3 – ДИМЕТИЛПЕНТАНОВАЯ КИСЛОТА
- 2 – МЕТИЛПЕНТЕН – 3 – ОВАЯ КИСЛОТА
- 2 – ГИДРОКСОПЕНТЕН – 3 – ОВАЯ КИСЛОТА
- 2 – МЕТИЛБУТАНДИОВАЯ КИСЛОТА
ИЗОМЕРИЯ КАРБОНОВЫХ КИСЛОТ
Для предельных карбоновых кислот
- УГЛЕРОДНОГО СКЕЛЕТА
- МЕЖКЛАССОВАЯ (СЛОЖНЫЕ ЭФИРЫ)
Для непредельных карбоновых кислот
- УГЛЕРОДНОГО СКЕЛЕТА
- ПОЛОЖЕНИЯ КРАТНОЙ СВЯЗИ
- МЕЖКЛАССОВАЯ
 " width="640"
" width="640"
ФИЗИЧЕСКИЕ СВОЙСТВА
Жидкости с характерным резким
запахом,
хорошо растворимые в воде
С 1 – С 3
Вязкие маслянистые жидкости с
неприятным запахом, плохо
растворимые
в воде
С 4 – С 9
Твердые вещества,
не имеющие запаха, не растворимые
в воде
C 10 и
ХИМИЧЕСКИЕ СВОЙСТВА
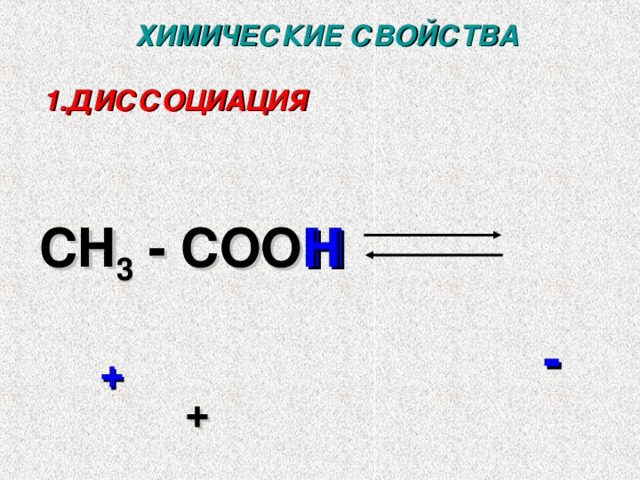
CH 3 - COO
H
CH 3 - COO H
-
+
+

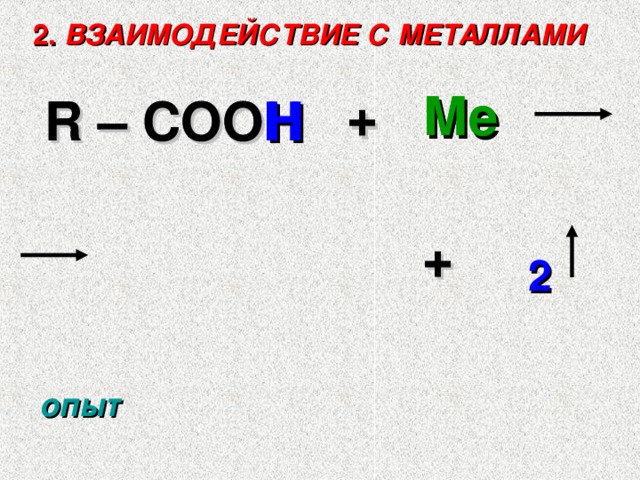
2. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ
+
Ме
Ме
R – COO H
R – COO
H
+
2
опыт

3.ВЗАИМОДЕЙСТВИЕ С ОСНОВНЫМИ ОКСИДАМИ
2 R – COO H + Mg O =
=(R – COO) 2 Mg + H 2 O
4 .ВЗАИМОДЕЙСТВИЕ СО ЩЕЛОЧАМИ
R – COO H + Na OH =
=R – COO Na + H 2 O

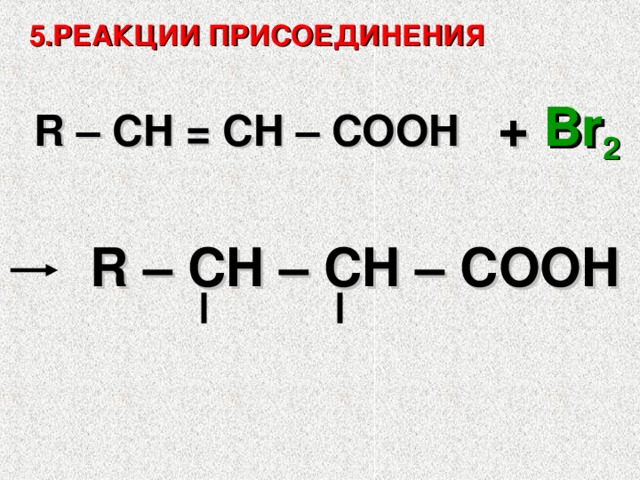
5 .РЕАКЦИИ ПРИСОЕДИНЕНИЯ
R – CH = С H – COOH
+ Br 2
Br
Br
R – CH – CH – COOH

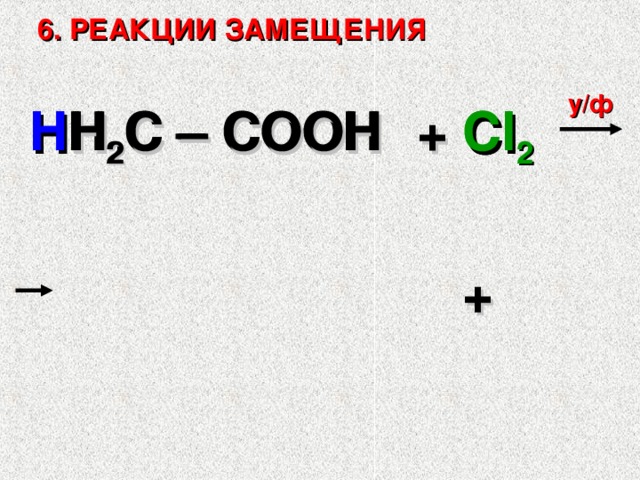
6. РЕАКЦИИ ЗАМЕЩЕНИЯ
у/ф
H H 2 C – COOH
+ Cl 2
H 2 C – COOH
Cl
Cl
H
+
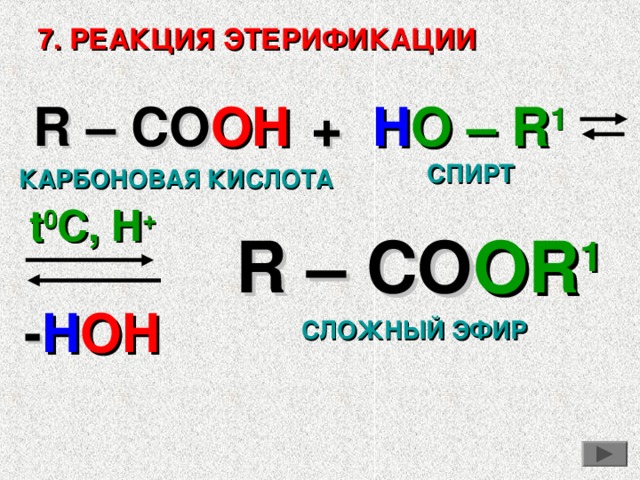
7. РЕАКЦИЯ ЭТЕРИФИКАЦИИ
+ H O – R 1
R – CO OH
СПИРТ
КАРБОНОВАЯ КИСЛОТА
t 0 C, H +
R – CO OR 1
- H OH
СЛОЖНЫЙ ЭФИР
УИЛЬЯМСОН (Williamson), Александер Уильям
1 мая 1824 г. – 6 мая 1904 г.
Английский химик-органик
Александр Уильям Уильямсон родился в Лондоне.
Изучал химию в Гейдельбергском университете
у Леопольда Гмелина (1840-1843) и в Гисенском
университете у Юстуса Либиха.
В 1848 г. стал профессором химии университетского
колледжа в Лондоне.
В 1863, 1865, 1869-1871 гг. являлся Президентом
Лондонского химического
общества. Иностранный член-корреспондент Петербургской АН (1891 ).
Основные научные работы Уильямсона посвящены огранической химии.
Изучая механизм реакций этерификации, Уильямсон установил, что при
действии серной кислоты на этиловый спирт образуется этилсерная кислота,
которая затем реагирует со спиртом и даёт эфир.
Действуя на этилсерную кислоту амиловым спиртом он получил
этиламиловый эфир. Исследуя сложные эфиры, Уильямсон показал,
что реакции этерификации являются обратимыми и приводят к наступлению
динамического равновесия, в котором присутствуют и исходные вещества,
и продукты реакции. В 1852 г. Уильямсон предложил способ
кетонизации кислот – получение кетонов нагреванием смеси солей различных
карбоновых кислот.
УИЛЬЯМСОН (Williamson), Александер Уильям
1 мая 1824 г. – 6 мая 1904 г.
Английский химик-органик
Александр Уильям Уильямсон родился в Лондоне.
Изучал химию в Гейдельбергском университете
у Леопольда Гмелина (1840-1843) и в Гисенском
университете у Юстуса Либиха.
В 1848 г. стал профессором химии университетского
колледжа в Лондоне.
В 1863, 1865, 1869-1871 гг. являлся Президентом
Лондонского химического
общества. Иностранный член-корреспондент Петербургской АН (1891 ).
Основные научные работы Уильямсона посвящены огранической химии.
Изучая механизм реакций этерификации, Уильямсон установил, что при
действии серной кислоты на этиловый спирт образуется этилсерная кислота,
которая затем реагирует со спиртом и даёт эфир.
Действуя на этилсерную кислоту амиловым спиртом он получил
этиламиловый эфир. Исследуя сложные эфиры, Уильямсон показал,
что реакции этерификации являются обратимыми и приводят к наступлению
динамического равновесия, в котором присутствуют и исходные вещества,
и продукты реакции. В 1852 г. Уильямсон предложил способ
кетонизации кислот – получение кетонов нагреванием смеси солей различных
карбоновых кислот.

СЛОЖНЫЕ ЭФИРЫ
Сложные эфиры широко используются в качестве
растворителей, пластификаторов, ароматизаторов.
Эфиры МУРАВЬИНОЙ КИСЛОТЫ
HCOOCH 3 — метилформиат , tкип = 32 °C; растворитель жиров, минеральных
и растительных масел, целлюлозы, жирных кислот; ацилирующий агент;
используют в производстве некоторых уретанов, формамида.
HCOOC 2 H 5 — этилформиат , tкип = 53 °C; растворитель нитрата и ацетата
целлюлозы; ацилирующий агент; отдушка для мыла, его добавляют
к некоторым сортам рома, чтобы придать ему характерный аромат; применяют
в производстве витаминов B1, A, E.
HCOOCH 2 CH(CH 3 ) 2 — изобутилформиат несколько
напоминает запах ягод малины.
HCOOCH 2 CH 2 CH(CH 3 ) 2 — изоамилформиат (изопентилформиат)
растворитель смол и нитроцеллюлозы.
HCOOCH 2 C 6 H 5 — бензилформиат , tкип = 202 °C; имеет запах жасмина ; ;
используется как растворитель лаков и красителей.
HCOOCH 2 CH 2 C 6 H 5 — 2 - фенилформиат имеет запах хризантем .

СЛОЖНЫЕ ЭФИРЫ
Сложные эфиры широко используются в качестве
растворителей, пластификаторов, ароматизаторов.
Эфиры МУРАВЬИНОЙ КИСЛОТЫ
HCOOCH 3 — метилформиат , tкип = 32 °C; растворитель жиров, минеральных
и растительных масел, целлюлозы, жирных кислот; ацилирующий агент;
используют в производстве некоторых уретанов, формамида.
HCOOC 2 H 5 — этилформиат , tкип = 53 °C; растворитель нитрата и ацетата
целлюлозы; ацилирующий агент; отдушка для мыла, его добавляют
к некоторым сортам рома, чтобы придать ему характерный аромат; применяют
в производстве витаминов B1, A, E.
HCOOCH 2 CH(CH 3 ) 2 — изобутилформиат несколько
напоминает запах ягод малины.
HCOOCH 2 CH 2 CH(CH 3 ) 2 — изоамилформиат (изопентилформиат)
растворитель смол и нитроцеллюлозы.
HCOOCH 2 C 6 H 5 — бензилформиат , tкип = 202 °C; имеет запах жасмина ; ;
используется как растворитель лаков и красителей.
HCOOCH 2 CH 2 C 6 H 5 — 2 - фенилформиат имеет запах хризантем .

Эфиры УКСУСНОЙ КИСЛОТЫ
CH 3 COOCH 3 — метилацетат , tкип = 58 °C; по растворяющей способности
аналогичен ацетону и применяется в ряде случаев как его заменитель, однако
он обладает большей токсичностью, чем ацетон.
CH 3 COOC 2 H 5 — этилацетат , tкип = 78 °C; подобно ацетону растворяет
большинство полимеров. По сравнению с ацетоном его преимущество в
более высокой температуре кипения (меньшей летучести).
CH 3 COOC 3 H 7 — н -пропилацетат , tкип = 102 °C; по растворяющей
способности подобен этилацетату.
CH 3 COOCH(CH 3 ) 2 — изопропилацетат , tкип = 88 °C; по растворяющим
свойствам занимает промежуточное положение между этил- и пропилацетатом.
CH 3 COOC 5 H 11 — н -амилацетат ( н -пентилацетат) , tкип = 148 °C; напоминает
по запаху грушу, применяется как растворитель для лаков, поскольку он
испаряется медленнее, чем этилацетат.
CH 3 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилацетат (изопентилацетат)
напоминает по запаху бананы.
CH 3 COOC 8 H 17 — н -октилацетат имеет запах апельсинов.

Эфиры УКСУСНОЙ КИСЛОТЫ
CH 3 COOCH 3 — метилацетат , tкип = 58 °C; по растворяющей способности
аналогичен ацетону и применяется в ряде случаев как его заменитель, однако
он обладает большей токсичностью, чем ацетон.
CH 3 COOC 2 H 5 — этилацетат , tкип = 78 °C; подобно ацетону растворяет
большинство полимеров. По сравнению с ацетоном его преимущество в
более высокой температуре кипения (меньшей летучести).
CH 3 COOC 3 H 7 — н -пропилацетат , tкип = 102 °C; по растворяющей
способности подобен этилацетату.
CH 3 COOCH(CH 3 ) 2 — изопропилацетат , tкип = 88 °C; по растворяющим
свойствам занимает промежуточное положение между этил- и пропилацетатом.
CH 3 COOC 5 H 11 — н -амилацетат ( н -пентилацетат) , tкип = 148 °C; напоминает
по запаху грушу, применяется как растворитель для лаков, поскольку он
испаряется медленнее, чем этилацетат.
CH 3 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилацетат (изопентилацетат)
напоминает по запаху бананы.
CH 3 COOC 8 H 17 — н -октилацетат имеет запах апельсинов.

Эфиры МАСЛЯНОЙ КИСЛОТЫ
C 3 H 7 COOCH 3 — метилбутират , tкип = 102,5 °C; по запаху напоминает ранет.
C3H7COOC 2 H 5 — этилбутират , tкип = 121,5 °C; имеет характерный запах
ананасов.
C 3 H 7 COOC 4 H 9 — бутилбутират , tкип = 166,4 °C;
C 3 H 7 COOC 5 H 11 — н -амилбутират ( н -пентилбутират) и
C 3 H 7 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилбутират (изопентилбутират)
имеют запах груш, а также служат растворителями в лаках для ногтей.
Эфиры ИЗОВАЛЕРИАНОВОЙ КИСЛОТЫ
(CH 3 ) 2 CHCH 2 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилизовалерат
(изопентилизовалерат) имеет запах яблока.

Эфиры МАСЛЯНОЙ КИСЛОТЫ
C 3 H 7 COOCH 3 — метилбутират , tкип = 102,5 °C; по запаху напоминает ранет.
C3H7COOC 2 H 5 — этилбутират , tкип = 121,5 °C; имеет характерный запах
ананасов.
C 3 H 7 COOC 4 H 9 — бутилбутират , tкип = 166,4 °C;
C 3 H 7 COOC 5 H 11 — н -амилбутират ( н -пентилбутират) и
C 3 H 7 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилбутират (изопентилбутират)
имеют запах груш, а также служат растворителями в лаках для ногтей.
Эфиры ИЗОВАЛЕРИАНОВОЙ КИСЛОТЫ
(CH 3 ) 2 CHCH 2 COOCH 2 CH 2 CH(CH 3 ) 2 — изоамилизовалерат
(изопентилизовалерат) имеет запах яблока.
![СПОСОБЫ ПОЛУЧЕНИЯ ОКИСЛЕНИЕ ПЕРВИЧНЫХ СПИРТОВ И АЛЬДЕГИДОВ [ О ] СН 3 – СН 2 – ОН - Н 2 О ПЕРВИЧНЫЙ СПИРТ [ О ] СН 3 – СООН СН 3 – СОН - Н 2 О КАРБОНОВАЯ КИСЛОТА АЛЬДЕГИД](https://fsd.multiurok.ru/html/2017/02/16/s_58a5508000a4c/img36.jpg)
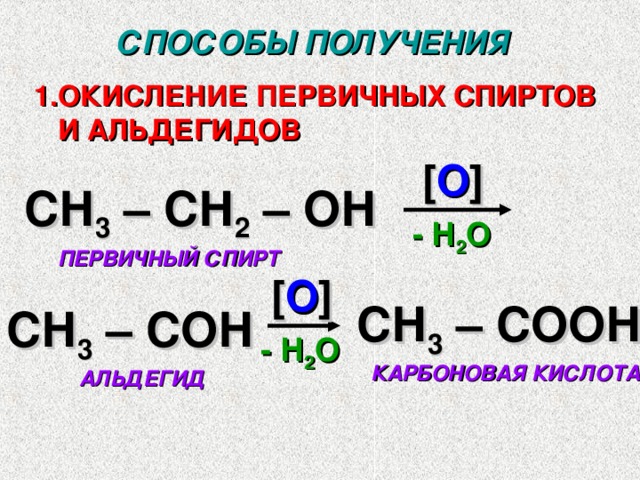
СПОСОБЫ ПОЛУЧЕНИЯ
- ОКИСЛЕНИЕ ПЕРВИЧНЫХ СПИРТОВ
И АЛЬДЕГИДОВ
[ О ]
СН 3 – СН 2 – ОН
- Н 2 О
ПЕРВИЧНЫЙ СПИРТ
[ О ]
СН 3 – СООН
СН 3 – СОН
- Н 2 О
КАРБОНОВАЯ КИСЛОТА
АЛЬДЕГИД

2. ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ
Н +
СН 3 – СО ОС 2 Н 5
+ Н ОН
СН 3 – СООН + С 2 Н 5 ОН

ОБЛАСТИ ПРИМЕНЕНИЯ
УКСУСНАЯ
КИСЛОТА
МУРАВЬИНАЯ
КИСЛОТА
ЩАВЕЛЕВАЯ
КИСЛОТА
ТЕСТ

МУРАВЬИНАЯ КИСЛОТА
- в текстильной промышленности
(в качестве протравы при крашении тканей);
- в кожевенной (при дублении кож);
- в пищевой (для консервирования фруктов);
- в производстве некоторых полимеров;
- хороший растворитель для многих полимеров
(капрона, найлона, поливинилхлорида),

МУРАВЬИНАЯ КИСЛОТА
- в текстильной промышленности
(в качестве протравы при крашении тканей);
- в кожевенной (при дублении кож);
- в пищевой (для консервирования фруктов);
- в производстве некоторых полимеров;
- хороший растворитель для многих полимеров
(капрона, найлона, поливинилхлорида),

УКСУСНАЯ КИСЛОТА
красителей, сложных эфиров,
ацетатного шелка, негорючей фото – и
кинопленки;
- широко используют соли уксусной
кислоты:
АЦЕТАТ ЖЕЛЕЗА, АЦЕТАТ ХРОМА,
АЦЕТАТ АЛЮМИНИЯ в качестве протравы
при крашении тканей;
АЦЕТАТ СВИНЦА – для изготовления
свинцовых белил;
АЦЕТАТ МЕДИ ( II ) – для борьбы
с вредителями сельского хозяйства.

УКСУСНАЯ КИСЛОТА
красителей, сложных эфиров,
ацетатного шелка, негорючей фото – и
кинопленки;
- широко используют соли уксусной
кислоты:
АЦЕТАТ ЖЕЛЕЗА, АЦЕТАТ ХРОМА,
АЦЕТАТ АЛЮМИНИЯ в качестве протравы
при крашении тканей;
АЦЕТАТ СВИНЦА – для изготовления
свинцовых белил;
АЦЕТАТ МЕДИ ( II ) – для борьбы
с вредителями сельского хозяйства.

ЩАВЕЛЕВАЯ КИСЛОТА
- для отбеливания тканей;
- в производстве красителей;
- в кожевенной и деревообрабатывающей
промышленности;
- для удаления ржавчины и накипи;
- в пищевой промышленности
(как пищевая добавка)

ЩАВЕЛЕВАЯ КИСЛОТА
- для отбеливания тканей;
- в производстве красителей;
- в кожевенной и деревообрабатывающей
промышленности;
- для удаления ржавчины и накипи;
- в пищевой промышленности
(как пищевая добавка)

ДОМАШНЕЕ ЗАДАНИЕ
- Упр. 16, 17 (письменно) – стр. 190
Относительная молекулярная масса некоторой
предельной одноосновной карбоновой кислоты
составляет 102. Определите кислоту, составьте
формулы всех возможных изомеров, включая
межклассовые. Дайте название всем веществам.

























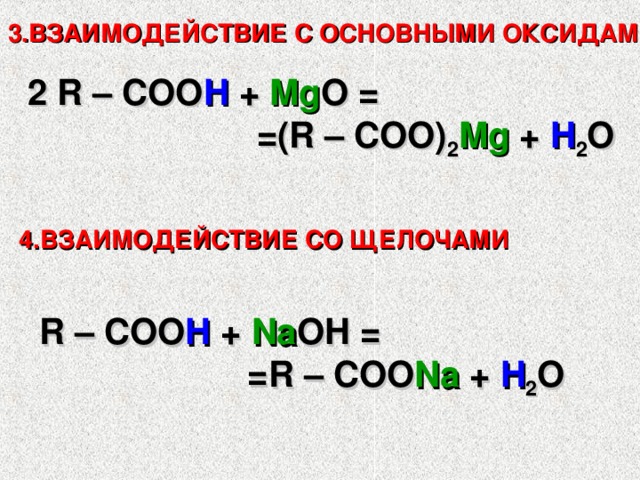

 " width="640"
" width="640"












![СПОСОБЫ ПОЛУЧЕНИЯ ОКИСЛЕНИЕ ПЕРВИЧНЫХ СПИРТОВ И АЛЬДЕГИДОВ [ О ] СН 3 – СН 2 – ОН - Н 2 О ПЕРВИЧНЫЙ СПИРТ [ О ] СН 3 – СООН СН 3 – СОН - Н 2 О КАРБОНОВАЯ КИСЛОТА АЛЬДЕГИД](https://fsd.multiurok.ru/html/2017/02/16/s_58a5508000a4c/img36.jpg)



























