Просмотр содержимого документа
«Исследование приготовление раствора сахара и определение массовой доли его в растворе»
Конспект урока по химии в 8 классе
Практическая работа №5 «Исследование приготовление раствора сахара и определение массовой доли его в растворе»
| Тип урока | Урок комплексного применения ЗУН учащихся. Дидактические цели: урок применения знаний и умений. Способ проведения: лабораторная работа |
| Авторы УМК | Габриелян О.С..,11-издание, 2012г. |
| Цели урока | Систематизировать знания по теме: соединения химических элементов. Научиться взвешивать на лабораторных весах, определять объем жидкости с помощью мерного цилиндра, приготовлять раствор с определенной массовой долей вещества. |
| Задачи урока | Общеучебные: - повторить понятие массовая доля и массы вещества, исследовать зависимость массы вещества от массовой доли растворенного вещества. Обучающие: - применить знания о способах исследования зависимости зависимость массы вещества от массовой доли растворенного вещества во время проведения лабораторной работы. - продолжить работу над формированием умений анализировать и обобщить знания о массовой доле. Развивающие: - развить познавательные интересы, интеллектуальные и творческие способности. - развить умения использовать полученные знания в повседневной жизни; |
| Метод обучения: | Проблемно-поисковый с применением элементов технологий дифференцированного обучения и здоровье сбережения. Системно – деятельностный подход. |
|
|
|
| Оборудование: | Интерактивная доска, штатив лабораторный с лапкой и муфтой, реактивы, и химическая посуда (химический стакан, палочка для перемешивания, мерный цилиндр, лабораторные весы, разновесы; сахар, вода). |
|
|
|
Оборудование и реактивы: химический стакан, палочка для перемешивания, мерный цилиндр, лабораторные весы, разновесы; сахар, вода.
Техника безопасности:
--Работать за столом аккуратно.
--Не делать резких движений.
--Взвешивание на весах всегда проводят с использованием тары (кусочка бумаги). --Химические вещества никогда нельзя помещать на чашку весов
--Взвешиваемый предмет помещают на левую чашку весов, а разновес - на правую
--Вначале взвешивают пустую тару, потом - тару с веществом и по разности определяют массу вещества
--Когда масса гирь начнет приближаться к массе предмета, наблюдают за качанием стрелки, до её совпадения с нулевым уровнем
--Когда равновесие достигнуто, записывают массу и убирают разновесы в футляр
--Рабочее место держать в порядке, предметы не разбрасывать.
--После выполнения работы, привести в порядок рабочее место.
Ход работы:
Выполнение лабораторной работы № 5 в тетради.
Порядок выполнения работы
Рассчитайте массу сахара и массу воды, необходимые для приготовления необходимого вам раствора используя формул:
m(вещества) = m(раствора) · ω(вещества)
m(H2O) = m(раствора) - m(вещества)
Расчеты приведите в отчете о практической работе.
Определите объем воды, соответствующий вычисленной массе, используя формулу: V = m · ρ.Помните, что для воды ρ = 1 г/мл.
Расчет приведите в отчете о практической работе.
С помощью мерного цилиндра отмерьте вычисленный объем воды. Перелейте воду в химический стакан.
На лабораторных весах взвесьте вычисленную массу сахара. Всыпьте сахар стакан с водой.
Перемешайте содержимое химического стакана до полного растворения сахара.
Сделайте вывод о том, что необходимо для приготовления раствора с определенной массовой долей растворенного вещества.
Отмерьте мерным цилиндром 50 мл дистиллированной воды и влейте ее в коническую колбочку емкостью 100 мл.
Чайную ложку сахарного песка (или два кусочка) взвесьте на лабораторных весах, затем поместите его в колбочку с водой и перемешивайте стеклянной палочкой до полного растворения.
Теперь приступайте к расчетной части. Вначале рассчитайте массовую долю сахара в растворе. Необходимые данные у вас есть: масса сахара, объем воды, плотность воды примите равной 1 г/мл.
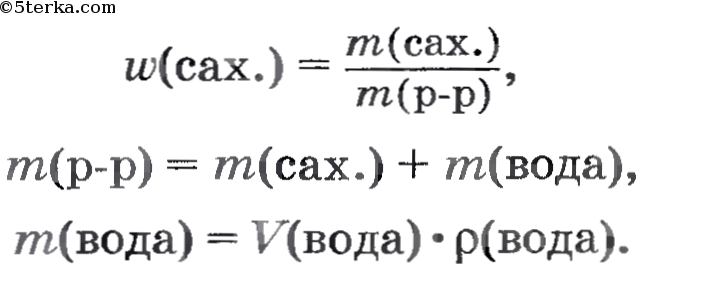
Вы также сможете рассчитать, сколько молекул сахара содержится в полученном растворе, используя известные вам соотношения:

Задача. Рассчитайте массовую долю сахара в растворе. Например:
Дано: Решение:
V(Н2О)=50мл 1) m(Н2О) = V(Н2О) · ρ(Н2О) = 50мл · 1г/мл = 50г
ρ(Н2О)=1г/мл 2) m(р-р) = m(Н2О) + m(сах.)= 50г + 3,5г = 53,5г
m(сах.)=3,5г 3) ω(сах.) = m(сах.):m(р-р) = 3,5г:53,5г = 0,065 (6,5%)
ω(сах.)=?
Ответ ω(сах.) = 0,065 (6,5%)
Выполните дополнительное задание. Найти количество вещества и число молекул в растворе.
Рефлексия: учащиеся научились приготовить раствор с определенной массовой долей. Я думаю, что дети с этим справились
Итог урока.
Сегодня мы на уроке систематизировали, расширили и углубили знания, умения и навыки по теме «Массовая доля растворенного вещества», выяснили зависимость концентрации вещества от массы .
Домашняя работа: повторить § 25-26, упражнение 24(2,4)
Приложение 1. Фото с урока