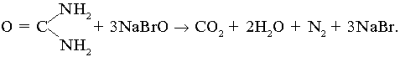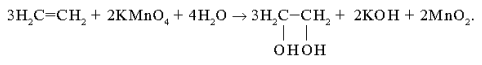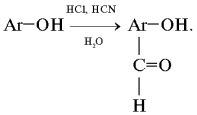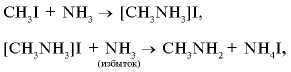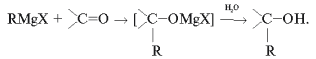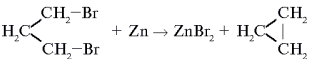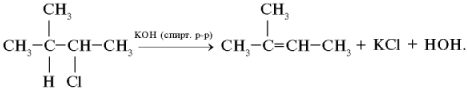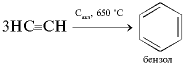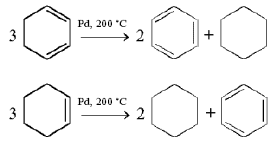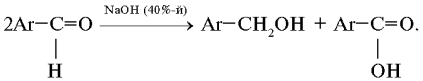ИПолучение
1. Реакция Вюрца: действие металлического натрия на моногалогенопроизводные углеводородов. Происходит удвоение углеродного скелета. Реакция подходит для получения симметричных алканов.
2CH3–CH2Br + 2Na = CH3–CH2–CH2–CH3 +2NaBr
2. Реакция Дюма: декарбоксилирование солей карбоновых кислот — сплавление со щелочами.
CH3COONa (тв.) + NaOH(тв.) = CH4 + Na2CO3
3. Реакция Кольбе: электролиз растворов солей карбоновых кислот:
CH3COONa + 2H2O =[эл.ток]= 2СО2 + Н2 + С2Н6 + 2NaOH
4. Синтез Густавсона: отщепление двух атомов галогена от дигалогеналканов:
СlCH2-CH2-CH2-CH2Cl + Zn = C4H8 (циклобутан) + ZnCl2
Вместо магния может использоваться цинк.
5. Синтез Лебедева: получение бутадиена из этанола.
2C2H5OH = Н2 + 2Н2O + CH2=CH-CH=CH2
Химические свойства
1. Реакция Коновалова – нитрование алканов разбавленной (10%-ной) азотной кислотой:
C2H6 + HNO3 = C2H5NO2 + Н2O
Избирательность нитрования:
третичный атом вторичный атом первичный атом углерода.
2. Эффект Хараша: присоединение бромоводорода в присутствии перекиси. Реакция протекает против правила Марковникова:
СН3-СН=СН2 + HBr =[Н2О2]= СН3-СН2-СН2Br
3. Реакция Вагнера: реакция с холодным водным раствором перманганата калия – мягкое окисление алкенов (образуется диол)
3СН3-СН=СН2 + 2KMnO4 + 4H2O = 2MnO2 + 2KOH + 3СН3 -СН(OH)-СН2(OH)
4. Реакция Кучерова: гидратация алкинов. Присоединение воды происходит в присутствии солей ртути (II) и идет через образование неустойчивого енола, который изомеризуется в альдегид или кетон. Гидратация ацетилена дает альдегид, других алкинов – кетон.
C2H2 + H2O = CH3CHO
5. Реакция Зелинского: тримеризация ацетилена над активированным углем. Образуется бензол.
3C2H2 = C6H6
6. Реакция Зинина: восстановление нитросоединений в растворе в щелочной и нейтральной среде:
R-NO2 + 3(NH4)2S = R-NH2 + 3S + 6NH3 +2H2O
ТО, ЧТО НАС ОБЬЕДИНЯЕТ...
Реакция Арбузова (перегруппировка Арбузова, изомеризация Арбузова) Каталитическая изомеризация эфиров фосфористой кислоты в эфиры алкилфосфиновых кислот (1904).
Правило Бейльштейна Если оба заместителя в ароматическом кольце принадлежат к одному и тому же типу, то преобладающее направление замещения определяется тем из них, влияние которого сильнее (1866).
Проба Бейльштейна Открытие галогенов в органических соединениях путем прокаливания на окисленной медной проволоке (1872). Вещество в смеси с CuO наносят на медную (или платиновую) проволоку и вносят в пламя; образующиеся при этом летучие галогениды меди окрашивают пламя в зеленый или голубовато-зеленый цвет.
Реактив Бенедикта (проба Бенедикта) [Benedict's reagent, Benedict's test]. Обнаружение алифатических альдегидов действием на них водного раствора, содержащего сульфат меди(II) CuSO4, карбонат натрия Na2CO3 и цитрат натрия. При нагревании образуются красные, желтые, зеленые осадки.
Реакция Бородина Разложение карбамида: 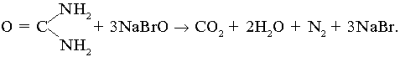
Реакция Бутлерова-Лермонтовой-Эльтекова Получение углеводородов изостроения каталитическим алкилированием низших олефинов алкилгалогенидами (1878).
Реакция Вагнера (окисление по Вагнеру, перманганатная проба).Окисление органических соединений, содержащих двойную связь, действием 1-3%-го раствора перманганата калия (1887) в цис-a-гликоли в щелочной среде (считается положительной, если раствор перманганата быстро обесцвечивается в кислой среде или буреет в щелочной и нейтральной): 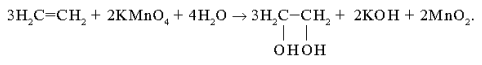
Реакция Вёлера Взаимодействие карбида кальция с водой (1862). Практическое значение реакция приобрела после того, как А.Муассан и Т.Вильсон разработали способ дешевого получения карбида кальция в электропечи в результате сплавления кокса и извести (1892). 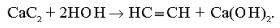
Реакция Вильямсона (метод Вильямсона) [Williamson's synthesis]. Получение простых эфиров из алкилгалогенида и алкоголята натрия (или калия): 
Реакция Вюрца. [Wurtz reaction]. Синтез алканов действием металлического натрия в инертном растворителе на алкилгалогениды (1855):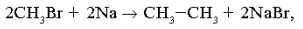
в общем виде:

Реакция Вюрца-Фиттига. [Wurtz-Fittig reaction]. Получение алкилбензолов из смеси алифатических и ароматических галогенидов действием металлического натрия в инертном растворителе (1864):
Реакция Гарриеса. (1866-1923), профессор (Германия). Основные исследования посвящены химии каучука. Президент Немецкого химического общества (1920-1922). Образование озонидов.
Реакция Гаттермана. Получение ароматического альдегида при взаимодействии фенола с хлороводородом и циановодородом в присутствии катализаторов (кислот Льюиса) с последующим гидролизом продукта (1898):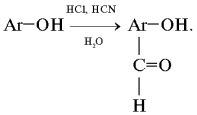
Правила ориентации Голлемана Ориентанты (заместители) первого рода (CH3, C2H5, галогены, аминогруппа, гидроксил) повышают реакционную способность ароматического ядра и направляют реагенты в орто- и параположения.
2. Ориентанты (заместители) второго рода (нитро- и сульфогруппы, карбоксильная и карбонильная группы) уменьшают реакционную способность ароматического ядра и направляют реагенты в метаположение (1895). (В настоящее время эти эффекты объясняются на основе электронных представлений: мезомерные и индукционные эффекты, 1920 г.).
Реакция Гофмана. Получение алифатических аминов из алкилгалогенидов: 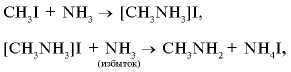
и так далее до образования третичного амина (CH3)3N.
Реактив Гриньяра. [Grignard reagent] Синтез органических веществ из алкилгалогенидов и магния в эфире. Реакция открыта П.Барбье в 1899 г. и подробно изучена В.Гриньяром в 1900 г.: 
Реактив Гриньяра RMgX используется для присоединения по кратным связям 
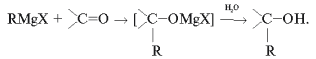
Реакция Густавсона. Получение циклоалканов из дигалогенпроизводных (1887). 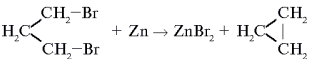
Реакция Дильса-Альдера (диеновый синтез) Присоединение ненасыщенного соединения, кратная связь которого активирована соседней группой (такое соединение имеет название "диенофил": акролеин, малоновый ангидрид, кротоновый альдегид), к ненасыщенному углеводороду (диену), имеющему сопряженные двойные связи (бутадиен, циклогексадиен, антрацен, фуран) (1928).
Правило Зайцева. Отщепление галогеноводородных кислот от алкилгалогенидов или воды от спиртов преимущественно происходит так, что с галогеном или гидроксилом уходит водород от наименее гидрогенизованного соседнего атома углерода (1875): 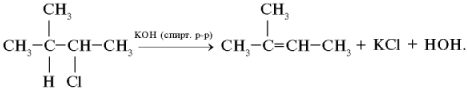
Реакция Зелинского-Казанского (метод Зелинского-Казанского). Тримеризация ацетилена (полимеризация ацетилена) на активированном угле при нагревании (1924): 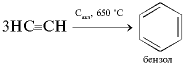
Реакция Зелинского (необратимый катализ, катализ Зелинского)Каталитическое диспропорционирование циклогексадиена и циклогексена (1911): 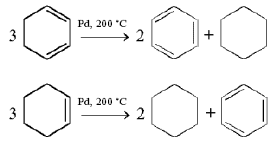
Реакция Зинина. Восстановление ароматических нитросоединений (1842): 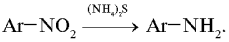
Реакция Канниццаро [Cannizzaro reaction]. Окислительно-восстановительное диспропорционирование двух молекул ароматического альдегида в щелочной среде, приводящее к образованию спирта и кислоты (1853): 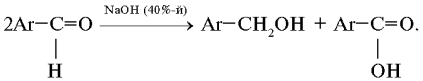
Реакция Кирхгофа. Получение глюкозы гидролизом крахмала при его нагревании с катализатором - разбавленной серной кислотой (1811): 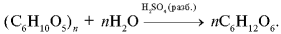
Реакция Клемменсена (восстановление по Клемменсену). Восстановление альдегидов и кетонов в гомологи бензола водородом в момент его выделения (восстановление карбонильной группы до метиленовой) (1913):![]()
Реакция Кольбе-Шмитта. Получение ароматических оксикислот карбоксилированием фенолятов щелочных металлов (1860): 
Реакция Кольбе (электрохимическая). Получение алканов с четным числом атомов углерода электролизом растворов солей щелочных металлов и карбоновых кислот с неразветвленной углеродной цепью (1849): 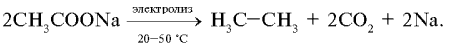
Реакция Коновалова. Получение нитроалканов (1888): 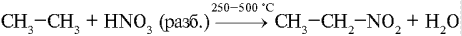
Реакция Кучерова (гидратация по Кучерову). Каталитическая гидратация ацетиленовых углеводородов с образованием карбонилсодержащих соединений (1881):
![]()
Реакция Лебедева. Получение бутадиена пиролизом этанола (1926): 
Реакция Львова-Шешукова. Хлорирование олефинов в a-положение к двойной связи, сопровождающееся аллильным сдвигом двойной связи (1883):
Правило Марковникова. В случае присоединения водородсодержащих соединений (протонных кислот или воды) к несимметричному алкену атом водорода преимущественно присоединяется к наиболее гидрогенизованному атому углерода, стоящему при двойной связи (1869):
Реакция Настюкова (формалитовая реакция). Взаимодействие ароматических углеводородов с формальдегидом (определение ароматических углеводородов) в присутствии концентрированной серной кислоты (1904):
Образование красно-коричневой смолы подтверждает наличие бензола и его гомологов. Реакции мешает присутствие непредельных циклических соединений.
Правило Несмеянова-Борисова. Электрофильные и радикальные замещения у углеродного атома, связанного двойной углерод-углеродной связью, происходят с сохранением геометрической конфигурации молекулы вещества.
Реакция Раймера-Тимана. Получение ароматических о-оксиальдегидов взаимодействием фенола с хлороформом в растворе щелочи. Реакция приводит к введению альдегидной группы в бензольное кольцо (замещение обычно происходит в ортоположение):
Реакция Розенмунда. Получение ароматических альдегидов из хлорангидридов кислот в среде бензола, толуола и других ароматических углеводородов:
Реакция открыта М.М.Зайцевым в 1872 г. и подробно изучена К.В.Розенмундом в 1918 г.
Реакция Сабатье-Сандерана. Жидкофазное гидрирование этилена до этана в присутствии мелкораздробленного никеля как катализатора (1899): 
Реакция Савича. Получение алкинов из дигалогенпроизводных алканов (1861):
Проба Селиванова. Качественное открытие фруктозы (1887) (кетозы при нагревании с резорцином и соляной кислотой дают вишнево-красное окрашивание; альдозы в этих же условиях взаимодействуют медленнее и дают бледно-розовую окраску):
(Можно использовать раствор, состоящий из 0,05 г резорцина в 50 мл воды и нескольких капель концентрированной соляной кислоты плотностью 1,19 г/мл.)
Реакция Тищенко. Диспропорционирование альдегида - получение сложного эфира из альдегида - в присутствии алкоголята алюминия (1906):
Проба Толленса (реакция "серебряного зеркала"). Взаимодействие формальдегида с аммиачным раствором оксида серебра (реактив Толленса):
Реакция Ульмана. Получение высших ароматических гомологов из арилгалогенидов действием порошкообразной меди: 
Реакция Фаворского. Конденсация карбонильных соединений с алкинами с образованием ацетиленовых спиртов:
Синтез Фишера-Тропша. Получение алканов при каталитическом гидрировании (взаимодействие с водородом) монооксида углерода под давлением (1923).
Реакция Фокина. Гидрогенизация жиров (1902): ![]()
Реакция Фриделя-Крафтса. Алкилирование или ацилирование ароматических соединений соответственно алкил- или ацилгалогенидами (получение гомологов бензола) в присутствии безводного катализатора (AlCl3, BF3, ZnCl2 и др.) (1877):
Реакция Чугаева (ксантогеновая реакция). Превращение спиртов в алкены термическим разложением ксантогеновых эфиров, получаемых из этих спиртов (1902).
Крекинг по Шухову. Высокотемпературная переработка нефтяного сырья для получения продуктов меньшей молекулярной массы - расщепление углеводородов нефти (1891).
Правило Эльтекова (перегруппировка Эльтекова). Соединения, в которых гидроксильная группа находится при углеродном атоме, образующем углерод-углеродную кратную связь (енолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения - альдегиды или кетоны (1877):
Реакция Юрьева. Взаимные превращения 5-членных гетероциклических соединений, содержащих один гетероатом (1936).