
Электролитическая диссоциация
Барбашина Любовь Викторовна
Воронежский Государственный Профессионально-педагогический колледж

20 Октябрь, 2022
Электролитическая диссоциация

Электролитическая диссоциация
- Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией.
(1887г)
Сванте Аррениус (1859-1927)
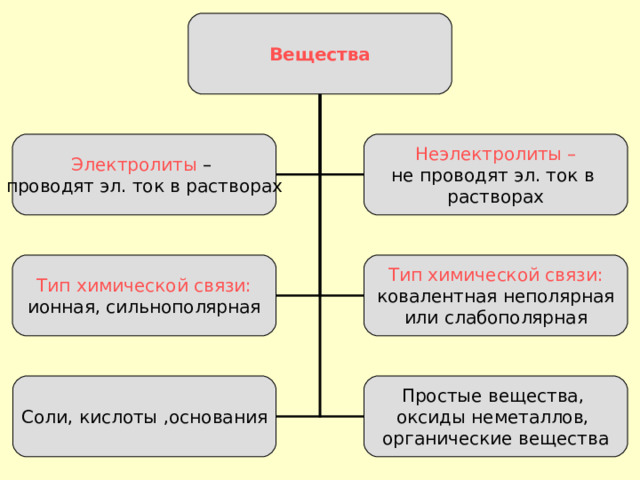
Вещества
Неэлектролиты –
Электролиты –
проводят эл. ток в растворах
не проводят эл. ток в
растворах
Тип химической связи:
Тип химической связи:
ионная, сильнополярная
ковалентная неполярная
или слабополярная
Соли, кислоты ,основания
Простые вещества,
оксиды неметаллов,
органические вещества
Коллекция учебных динамических слайдов по химии 8 класс.
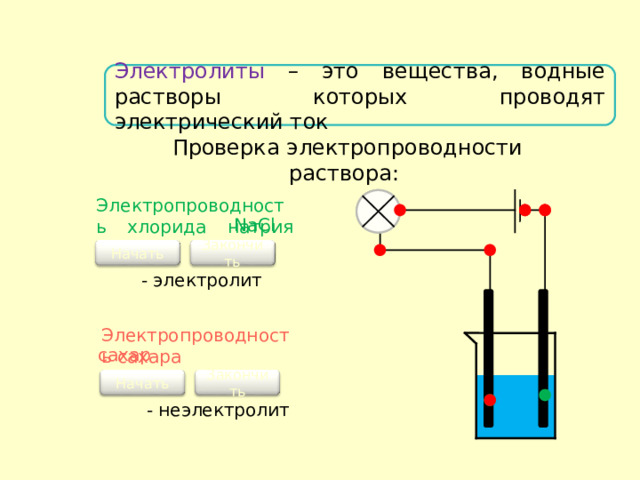
Электролиты – это вещества, водные растворы которых проводят электрический ток
Проверка электропроводности раствора:
Электропроводность хлорида натрия ( NaCl)
NaCl
Начать
Закончить
- электролит
Электропроводность сахара
сахар
Начать
Закончить
- неэлектролит
5
5
Баженов Алексей Анатольевич

20 Октябрь, 2022
Убери лишнее. (Найдите неэлектролиты)
Ошибка
Ca(OH) 2
Ошибка
H 2 O
О 2
NaOH
Mg(NO 3 ) 2
Ошибка
Al(NO 3 ) 3
Ошибка
NaCl
Ошибка
Ошибка
Na 2 CO 3
Ошибка
CuCl 2
CaSO 4
CO 2
Ошибка
K 2 SO 4
CaCO 3
Ошибка
FeCl 3
Ошибка
NaNO 3
BaSO 4
S О 3
K 2 S
Ошибка
Cu(OH) 2
H 2 SO 4
Ошибка
5
5
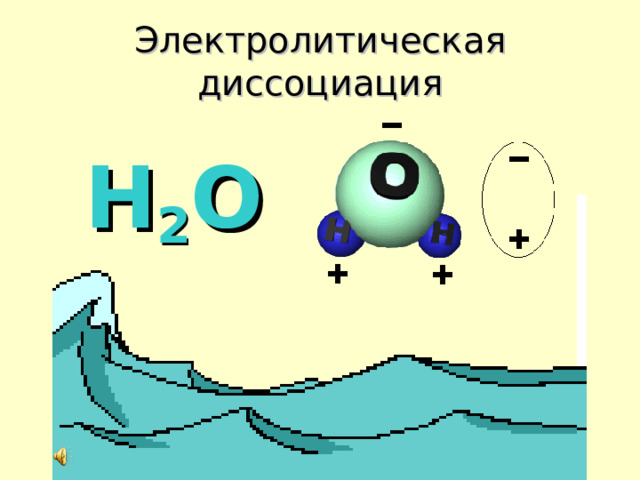
Электролитическая диссоциация
H 2 O

-
+
-
+
-
+
+
-
+
-
=
+
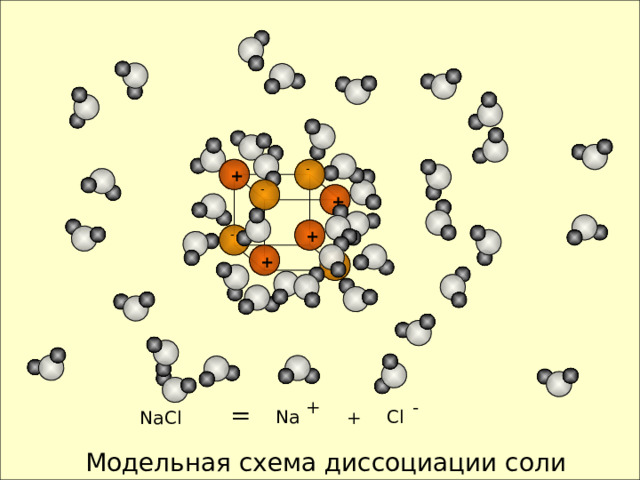
NaCl
Cl
Na
Модельная схема диссоциации соли
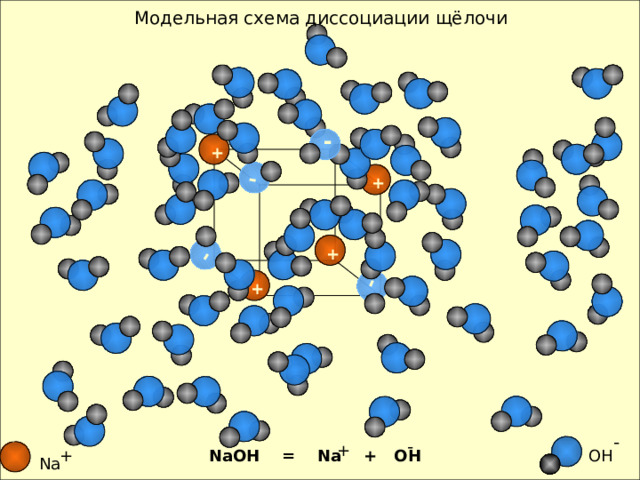
Модельная схема диссоциации щёлочи
-
-
-
-
+
+
+
+
_
-
-
+
+
+
OH
NaOH = Na + OH
Na
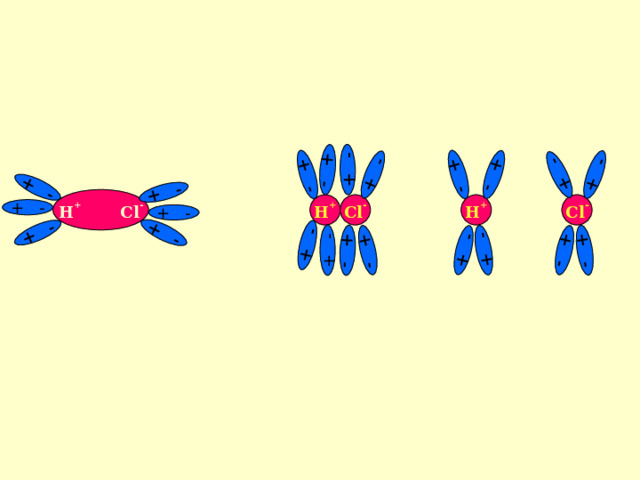
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
H + Cl -
H +
Cl -
H +
Cl -
+ -
+ -
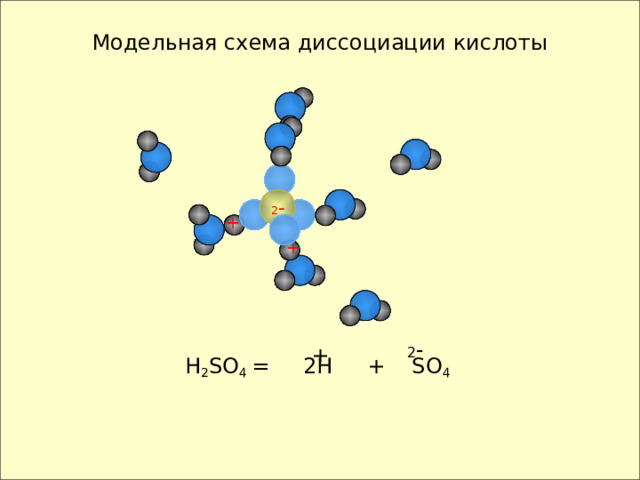
Модельная схема диссоциации кислоты
2 -
+
+
2 -
+
H 2 SO 4 = 2H + SO 4
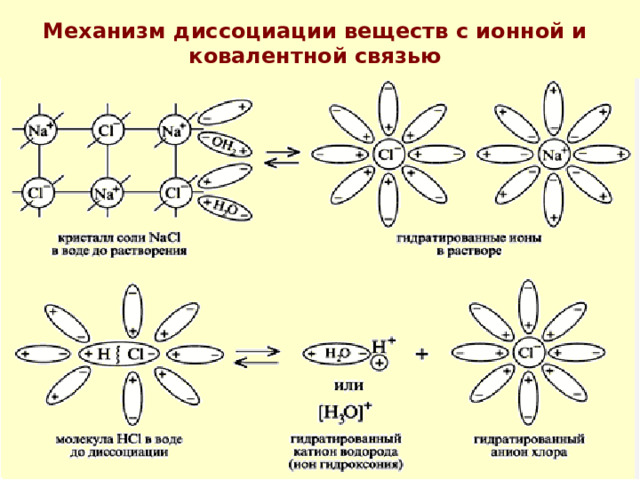
Механизм диссоциации веществ с ионной и ковалентной связью

Электролитическая диссоциация
Степень диссоциации -
это отношение числа частиц, распавшихся на ионы ( n ), к общему числу растворённых частиц ( N ).
 3% " width="640"
3% " width="640"
Электролитическая диссоциация
электролиты
сильные
слабые
средние
30%
3%
30% 3%

Электролитическая диссоциация
Степень диссоциации зависит от:

Задание 1 .
Впишите недостающие слова:
- Все вещества по их способности проводить электрический ток в растворах делятся на ______________ и ________________ .
Процесс распада электролита на ионы называется __________________ ______________.
В растворах электролиты диссоциируют на _______________ и ______________ ионы.
По степени электролитической диссоциации электролиты делятся на _________ и _______ .
2) Все соли – электролиты, CuSO 4 – ___________ .
Все растворимые основания – сильные электролиты,
NaOH – ___________________ .
электролиты
неэлектролиты
электролитической диссоциацией
положительные
отрицательные
сильные
слабые
электролит
сильный электролит
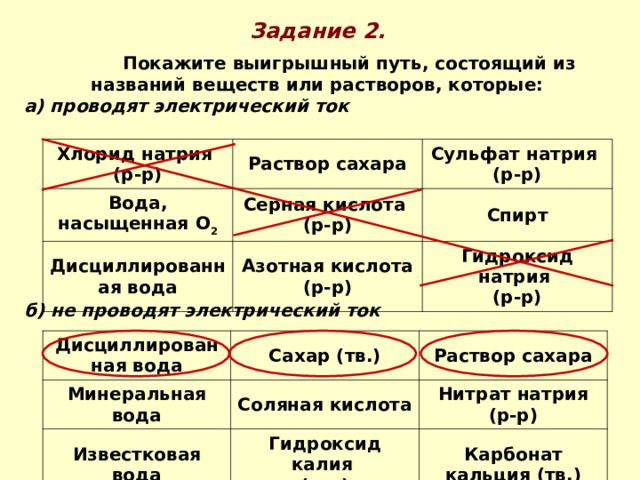
Задание 2.
Покажите выигрышный путь, состоящий из названий веществ или растворов, которые:
а) проводят электрический ток
Хлорид натрия
(р-р)
Раствор сахара
Вода, насыщенная O 2
Серная кислота
(р-р)
Дисциллированная вода
Сульфат натрия
(р-р)
Азотная кислота
(р-р)
Спирт
Гидроксид натрия
(р-р)
б) не проводят электрический ток
Дисциллированная вода
Минеральная вода
Сахар (тв.)
Раствор сахара
Известковая вода
Соляная кислота
Нитрат натрия (р-р)
Гидроксид калия
(р-р)
Карбонат кальция (тв.)

в) являются сильными электролитами
Раствор аммиака в воде
Сахар (тв.)
Гидроксид калия
(р-р)
Серная кислота
(р-р)
Соляная кислота
Угольная кислота
Дисциллированная вода
Нитрат натрия (р-р)
Карбонат кальция (тв.)

Задание 3.
Соотнесите:
1.
А) Электролиты 1) Кислоты
Б) Неэлектролиты 2) Оксиды
3) Простые вещества
4) Соли
5) Основания
2.
А) Сильные электролиты 1) Азотная кислот
Б) Слабые электролиты 2) Вода
3) Гидроксид натрия
4) Соляная кислота
5) Гидроксид алюминия
3.
Электролиты: Ионы в растворе электролита:
А) NaCl
Б) KOH
В) HNO 3
+
1) OH¯ 4) K
+
2) H 5) NO 3 ¯
–
+
3) Na 6)Cl
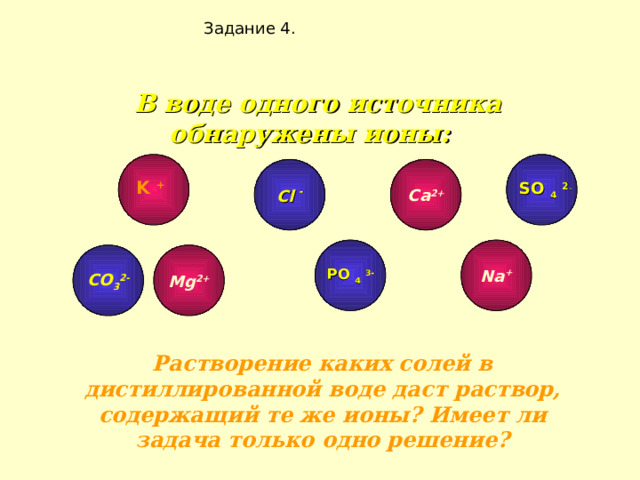
Задание 4.
В воде одного источника обнаружены ионы:
Cl -
Ca 2+
K +
SO 4 2 -
Na +
Mg 2+
C О 3 2-
PO 4 3-
Растворение каких солей в дистиллированной воде даст раствор, содержащий те же ионы? Имеет ли задача только одно решение?

Коллекция учебных динамических слайдов по химии 8 класс.
Реакции ионного обмена.
20 Октябрь, 2022
РИО ( реакции ионного обмена ) – это реакции протекающие между электролитами .
Пример: Взаимодействие хлорида бария с сульфатом натрия.
Порядок действий:
2. Расставить коэффициенты.
3. По таблице растворимости, определить нерастворимые вещества. Обозначить их стрелкой вниз.
4. Составить полное ионное уравнение (растворимые вещества расписать на ионы.
6. Составить сокращенное ионное уравнение.
5. Сократить одинаковые ионы в левой и правой части полного ионного уравнения.
1. Записать уравнение реакции в молекулярном виде.
2
SO 4 2-
2Na +
Ba 2+
BaSO 4
2Na +
BaCl 2 + Na 2 SO 4 BaSO 4 + NaCl
2Cl -
2Cl -
+
BaSO 4
SO 4 2-
Ba 2+
+
+
+
+
+
Баженов Алексей Анатольевич

Коллекция учебных динамических слайдов по химии 8 класс.
Тема: Условия протекания реакций ионного обмена.
20 Октябрь, 2022
I . Если образуется осадок.
II . Если образуется газ.
H 2 O
H 2 O
SO 4 2-
2H +
CO 3 2-
2Na +
2Na +
Na 2 CO 3 + H 2 SO 4 Na 2 SO 4 + H 2 CO 3
SO 4 2-
2Cl -
BaCl 2 + Na 2 SO 4 BaSO 4 + NaCl
Ba 2+
2Cl -
2Na +
SO 4 2-
2Na +
BaSO 4
2
CO 2
CO 2
CO 2
H 2 O
2H +
CO 3 2-
+
+
+
+
+
+
Ba 2+
SO 4 2-
+
BaSO 4
+
+
+
+
+
+
+
III . Если образуется вода.
2NO 3 -
Mg(NO 3 ) 2 + Na 2 CO 3 MgCO 3 + NaNO 3
2Na +
2Na +
MgCO 3
2
Mg 2+
CO 3 2-
2NO 3 -
2Na +
2Na +
2H +
2OH -
SO 4 2-
2H 2 O
2 NaOH + H 2 SO 4 Na 2 SO 4 + 2H 2 O
SO 4 2-
Mg 2+
CO 3 2-
+
MgCO 3
+
+
+
+
2H 2 O
2OH -
2H +
+
+
+
+
+
+
H +
+
H 2 O
OH -
+
23
23
Баженов Алексей Анатольевич

















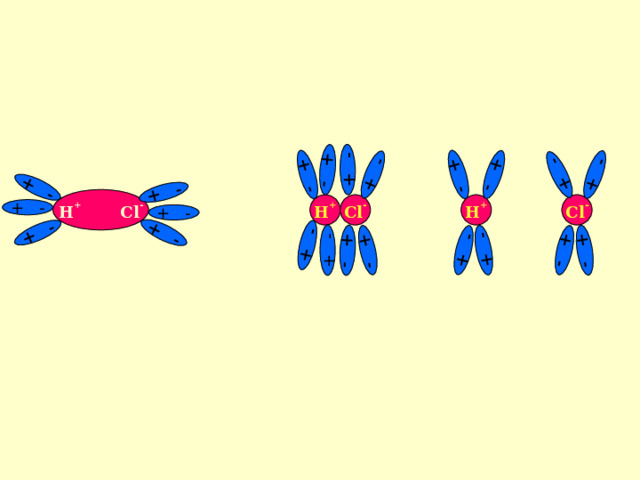



 3% " width="640"
3% " width="640"

























