
Окислительно-восстановительные реакции.
Классификация ОВР

К концу XVIII в. широкое распространение в химии получила кислородная теория окисления.
Окисление – это процесс соединения вещества с кислородом, а восстановление – это процесс отнятия у него кислорода.
Согласно теории в химических реакциях, протекающих с изменением степеней окисления атомов, происходит передача электронов от одних частиц к другим.


Классификация реакций
По признаку изменения
степени окисления
Окислительно-
восстановительные
Без изменения
степени окисления
Mg 0 – 2ē = Mg +2
O 2 + 4ē = 2O -2
-2
+1
0
+1
+1
+6
-2
+1
-2
+1
-2
+6
0
-2
+2
t
H 2 SO 4 + 2KOH = K 2 SO 4 + 2H 2 O
2Mg + O 2 = 2MgO

-1
0
0
+3
t
2Fe + 3Cl 2 = 2FeCl 3

-1
0
+3
-1
0
0
+3
0
t
2Fe + 3Cl 2 = 2FeCl 3
2Al + 3I 2 = 2AlI 3
+7
-1
0
+2
t
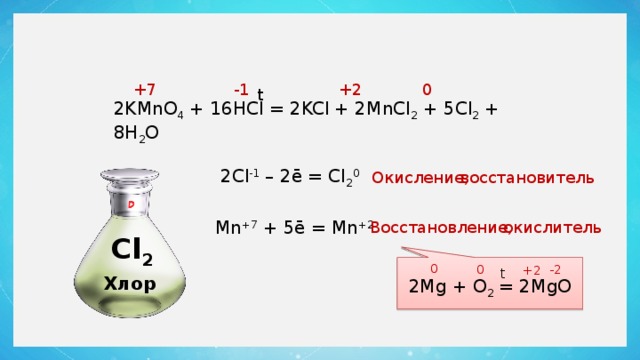
2KMnO 4 + 16HCl = 2KCl + 2MnCl 2 + 5Cl 2 + 8H 2 O
2Cl -1 – 2ē = Cl 2 0
восстановитель
Окисление,
Mn +7 + 5ē = Mn +2
окислитель
Восстановление,
Cl 2
0
0
-2
+2
t
Хлор
2Mg + O 2 = 2MgO
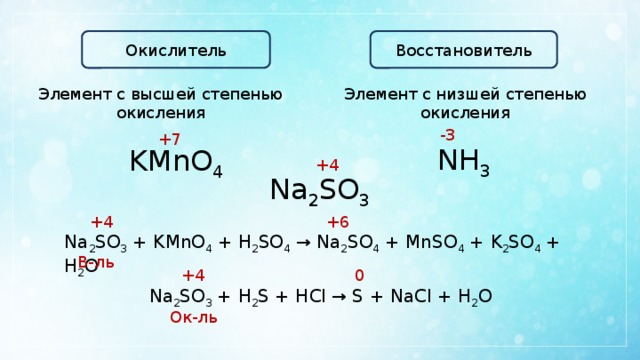
Окислитель
Восстановитель
Элемент с высшей степенью окисления
Элемент с низшей степенью окисления
-3
+7
NH 3
KMnO 4
+4
Na 2 SO 3
+4
+6
Na 2 SO 3 + KMnO 4 + H 2 SO 4 → Na 2 SO 4 + MnSO 4 + K 2 SO 4 + H 2 O
В-ль
+4
0
Na 2 SO 3 + H 2 S + HCl → S + NaCl + H 2 O
Ок-ль

Важнейшие окислители и восстановители
Важнейшие
восстановители
Важнейшие
окислители
Вещества-неметаллы:
O 2 .
F 2 ,
Сложные вещества:
KMnO 4 ,
K 2 Cr 2 O 7 ,
HNO 3 и её соли,
H 2 SO 4 конц.,
PbO 2 ,
HСlO 4 и её соли.

Отбеливание тканей, бумаги

PbS + 4H 2 O 2 = PbSO 4 + 4H 2 O

Важнейшие окислители и восстановители
Важнейшие
восстановители
Важнейшие
окислители
Вещества-неметаллы:
Вещества-металлы:
O 2 .
F 2 ,
щелочные и щелочноземельные металлы,
Сложные вещества:
Zn.
Al,
Mg,
KMnO 4 ,
K 2 Cr 2 O 7 ,
Сложные вещества:
H 2 SO 4 конц.,
HNO 3 и её соли,
CH 4 ,
Na 3 N,
PH 3 ,
SiH 4 ,
NH 3 ,
HСlO 4 и её соли.
PbO 2 ,
Ca 3 P 2 ,
H 2 S,
сульфиды металлов,
CaH 2 .
HBr,
HCl,
HI,
NaH,
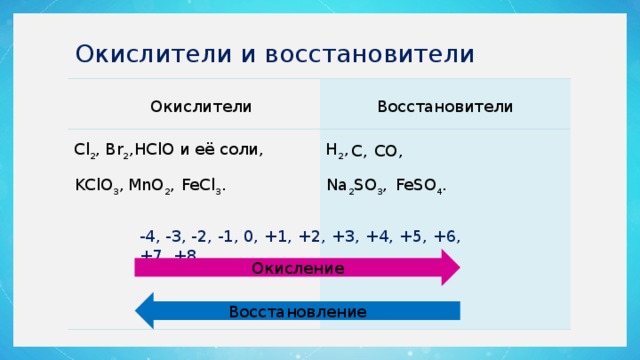
Окислители и восстановители
Окислители
Восстановители
Br 2 ,
HСlO и её соли,
H 2 ,
Cl 2 ,
C,
CO,
FeCl 3 .
FeSO 4 .
Na 2 SO 3 ,
MnO 2 ,
KСlO 3 ,
-4, -3, -2, -1, 0, +1, +2, +3, +4, +5, +6, +7, +8
Окисление
Восстановление

Классификация ОВР
Межмолекулярные окислительно-восстановительные реакции – реакции, в которых окислитель и восстановитель входят в состав различных веществ.
+3
+2
-1
0
FeCl 3 + KI → FeCl 2 + I 2 + KCl
Fe – окислитель
I – восстановитель

Классификация ОВР
Внутримолекулярные окислительно-восстановительные реакции – это реакции, в которых окислитель и восстановитель входят в состав одного вещества.
0
+6
-3
+3
(NH 4 ) 2 Cr 2 O 7 → N 2 + Cr 2 O 3 + H 2 O
N – восстановитель
Cr – окислитель
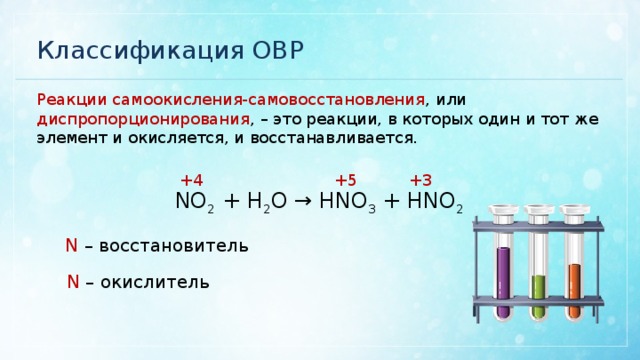
Классификация ОВР
Реакции самоокисления-самовосстановления , или диспропорционирования , – это реакции, в которых один и тот же элемент и окисляется, и восстанавливается.
+3
+5
+4
NO 2 + H 2 O → HNO 3 + HNO 2
N – восстановитель
N – окислитель

Составление ОВР:
1) записать схему химической реакции;
2) расставить степени окисления атомов элементов, выделить элементы, которые изменили свои степени окисления, определить окислитель и восстановитель;
3) определить число отданных и принятых электронов, составить электронный баланс;
4) подобрать коэффициенты в уравнении реакции.

Составление ОВР
-2
+4
0
-2
H 2 S + O 2 → SO 2 + H 2 O
2
3
2
2
6
2
восстановитель
S -2 – 6ē = S +4
12
окислитель
4
3
O 2 0 + 2 ∙ 2ē = 2O -2
2 H 2 S + 3 O 2 = 2 SO 2 + 2 H 2 O
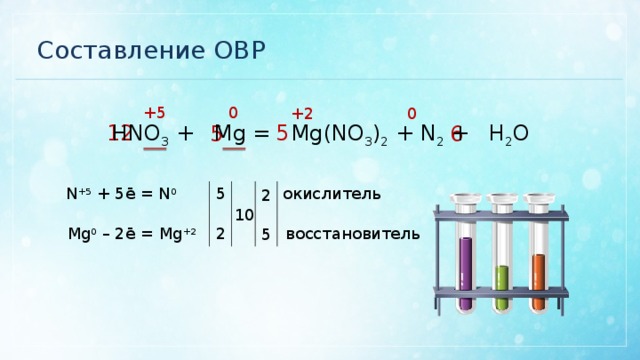
Составление ОВР
0
+5
0
+2
HNO 3 + Mg = Mg(NO 3 ) 2 + N 2 + H 2 O
12
5
6
5
5
N +5 + 5ē = N 0
окислитель
2
10
2
восстановитель
Mg 0 – 2ē = Mg +2
5
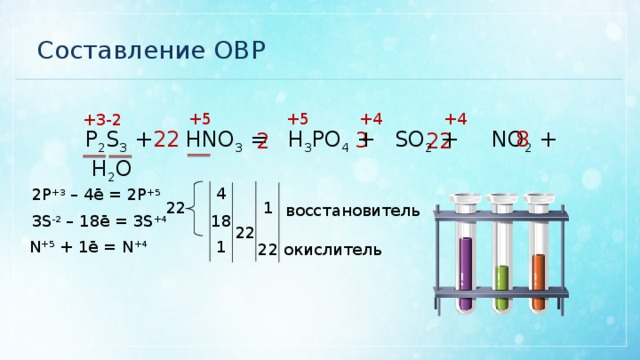
Составление ОВР
+4
+5
+4
+5
+3
-2
22
8
P 2 S 3 + HNO 3 = H 3 PO 4 + SO 2 + NO 2 + H 2 O
3
22
2
4
2P +3 – 4ē = 2P +5
1
22
восстановитель
3S -2 – 18ē = 3S +4
18
22
1
N +5 + 1ē = N +4
22
окислитель

Составление ОВР
+7
+2
2KMnO 4 + 5Na 2 SO 3 + 3 H 2 SO 4 = 2MnSO 4 + 5Na 2 SO 4 + K 2 SO 4 + 3H 2 O
+7
+4
2KMnO 4 + 3Na 2 SO 3 + H 2 O = 2MnO 2 + 3Na 2 SO 4 + 2KOH
+7
+6
2KMnO 4 + Na 2 SO 3 + 2 KOH = 2K 2 MnSO 4 + Na 2 SO 4 + H 2 O
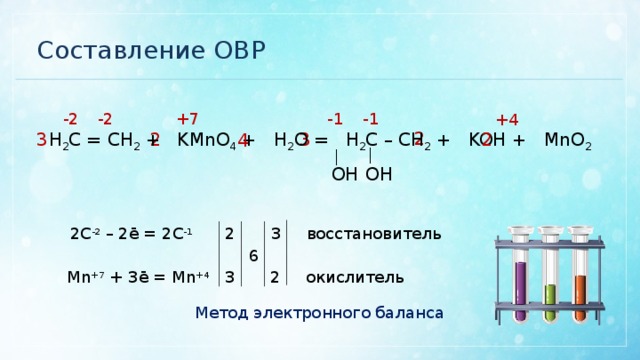
Составление ОВР
-1
+7
-1
-2
-2
+4
2
2
H 2 C = CH 2 + KMnO 4 + H 2 O = H 2 C – CH 2 + KOH + MnO 2
3
3
2
4
|
|
OH
OH
3
2
восстановитель
2C -2 – 2ē = 2C -1
6
окислитель
3
2
Mn +7 + 3ē = Mn +4
Метод электронного баланса
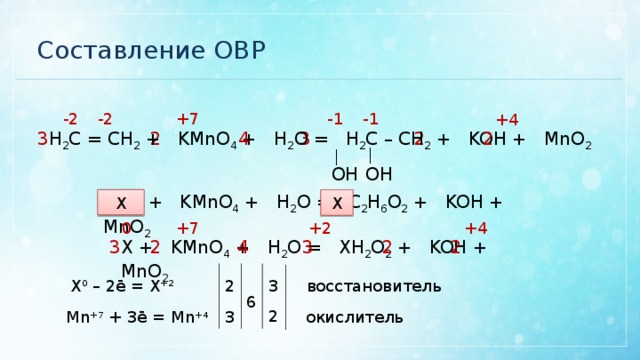
Составление ОВР
-1
-1
-2
-2
+7
+4
3
2
4
H 2 C = CH 2 + KMnO 4 + H 2 O = H 2 C – CH 2 + KOH + MnO 2
2
2
3
|
|
OH
OH
С 2 H 4 + KMnO 4 + H 2 O = C 2 H 6 O 2 + KOH + MnO 2
Х
Х
+4
0
+2
+7
2
2
3
2
3
X + KMnO 4 + H 2 O = XH 2 O 2 + KOH + MnO 2
4
Х 0 – 2ē = Х +2
2
3
восстановитель
6
2
окислитель
Mn +7 + 3ē = Mn +4
3
Обмен веществ
Дыхание
Фотосинтез

Гниение
Брожение

Получение аммиака
Получение металлов
Получение кислот

Получение фотографий

Горение природного газа
Ржавление железа
Потемнение серебра

Окислительно-восстановительные реакции.
Важнейшие окислители и восстановители.
Метод электронного баланса при расстановке коэффициентов в уравнениях химических реакций.
Роль окислительно-восстановительных процессов в природе и на производстве.






















































