Ферменты

Содержание
- Определение ферментов
- Значение ферментов
- Историческая справка
- Строение ферментов
- Каталитический центр
- Субстратный центр
- Аллостерический центр
- Уровни организации молекул ферментов: первичная структура
- Вторичная структура
- Третичная структура
- Четвертичная структура
- Зависимость активности ферментов от температуры
- Зависимость активности ферментов от рН – среды
- Классификация ферментов
- Свойства ферментов
- Механизм действия ферментов
- Применение ферментов
- Тест «Ферменты»

Определение ферментов
Ферме́нты или энзи́мы
(от лат. fermentum , греч. ζύμη, ἔνζυμον — дрожжи , закваска) — обычно белковые молекулы или молекулы РНК
( рибозимы ) или их комплексы,
ускоряющие
( катализирующие )
химические реакции в живых системах

Значение ферментов
- В каждой клетке имеются сотни различных ферментов
- С их помощью осуществляются многочисленные химические реакции, которые могут с большой скоростью идти при температурах, подходящих для данного организма, то есть в пределах от 5 о до 40 о
- Ферменты – это биологические катализаторы, то есть вещества, которые ускоряют биохимические реакции
- Они абсолютно необходимы, потому что без них реакции в клетке протекали бы слишком медленно

Из истории
- Термин фермент предложен в XVII веке химиком ван Гельмонтом при обсуждении механизмов пищеварения
- В кон. ХVIII — нач. XIX вв. уже было известно, что мясо переваривается желудочным соком , а крахмал превращается в сахар под действием слюны
- Однако механизм этих явлений был неизвестен
- В XIX в. Луи Пастер , изучая превращение углеводов в этиловый спирт под действием дрожжей , пришел к выводу, что этот процесс ( брожение ) катализируется некой жизненной силой, находящейся в дрожжевых клетках

Наука о ферментах
- Термины «фермент» и «энзим» давно используют как синонимы (первый в основном в русской и немецкой научной литературе, второй — в англо- и франкоязычной) Наука о ферментах называется энзимологией , а не ферментологией
Строение ферментов
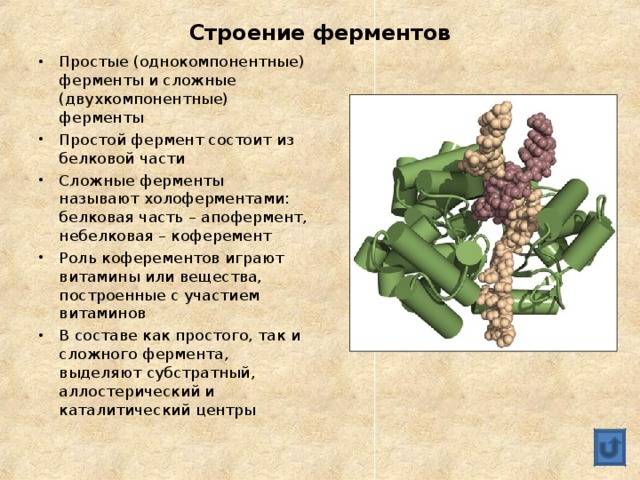
- Простые (однокомпонентные) ферменты и сложные (двухкомпонентные) ферменты
- Простой фермент состоит из белковой части
- Сложные ферменты называют холоферментами: белковая часть – апофермент, небелковая – коферемент
- Роль коферементов играют витамины или вещества, построенные с участием витаминов
- В составе как простого, так и сложного фермента, выделяют субстратный, аллостерический и каталитический центры
Каталитический центр
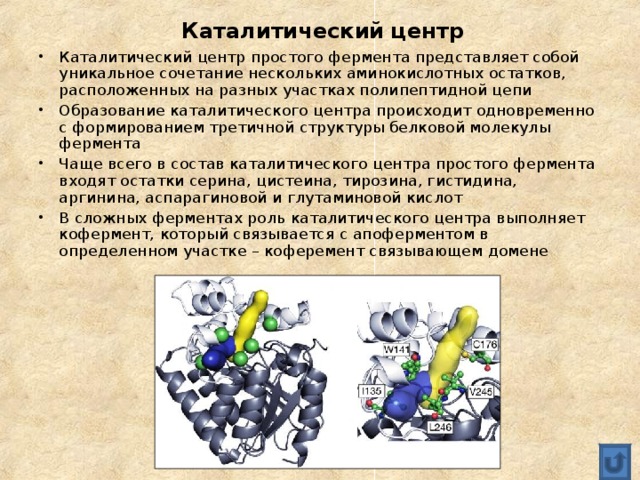
- Каталитический центр простого фермента представляет собой уникальное сочетание нескольких аминокислотных остатков, расположенных на разных участках полипептидной цепи
- Образование каталитического центра происходит одновременно с формированием третичной структуры белковой молекулы фермента
- Чаще всего в состав каталитического центра простого фермента входят остатки серина, цистеина, тирозина, гистидина, аргинина, аспарагиновой и глутаминовой кислот
- В сложных ферментах роль каталитического центра выполняет кофермент, который связывается с апоферментом в определенном участке – коферемент связывающем домене
Субстратный центр
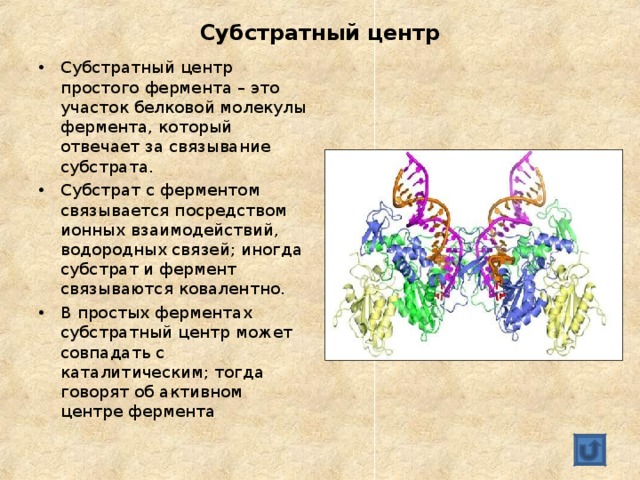
- Субстратный центр простого фермента – это участок белковой молекулы фермента, который отвечает за связывание субстрата.
- Субстрат с ферментом связывается посредством ионных взаимодействий, водородных связей; иногда субстрат и фермент связываются ковалентно.
- В простых ферментах субстратный центр может совпадать с каталитическим; тогда говорят об активном центре фермента
Аллостерический центр
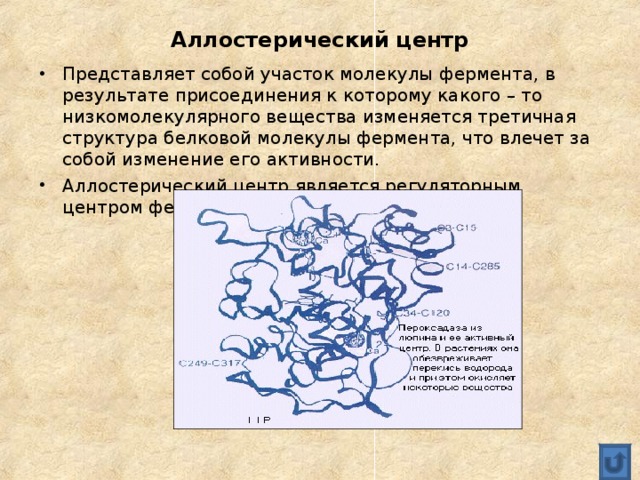
- Представляет собой участок молекулы фермента, в результате присоединения к которому какого – то низкомолекулярного вещества изменяется третичная структура белковой молекулы фермента, что влечет за собой изменение его активности.
- Аллостерический центр является регуляторным центром фермента
Уровни организации молекул ферментов Первичная структура
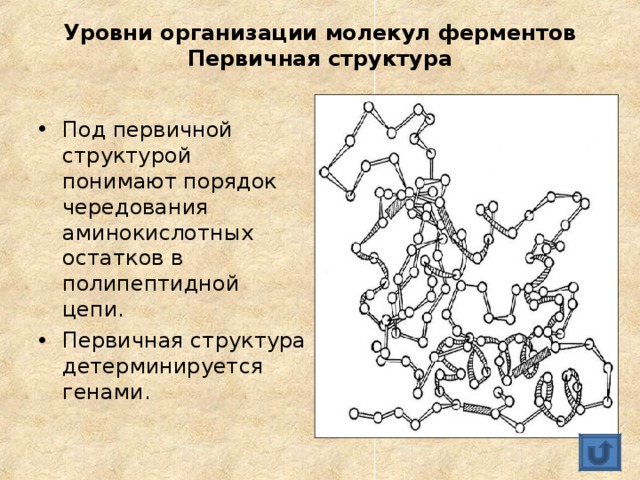
- Под первичной структурой понимают порядок чередования аминокислотных остатков в полипептидной цепи.
- Первичная структура детерминируется генами.
Вторичная структура
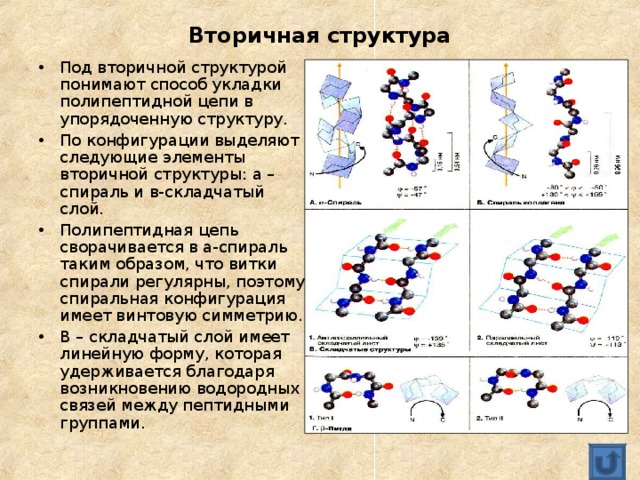
- Под вторичной структурой понимают способ укладки полипептидной цепи в упорядоченную структуру.
- По конфигурации выделяют следующие элементы вторичной структуры: а – спираль и в-складчатый слой.
- Полипептидная цепь сворачивается в а-спираль таким образом, что витки спирали регулярны, поэтому спиральная конфигурация имеет винтовую симметрию.
- В – складчатый слой имеет линейную форму, которая удерживается благодаря возникновению водородных связей между пептидными группами.
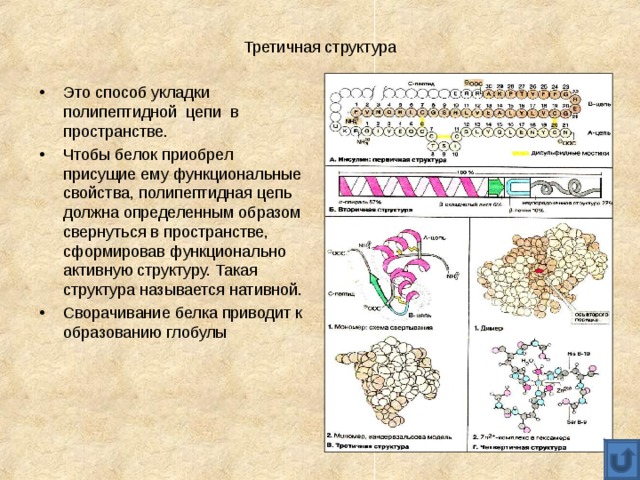
Третичная структура
- Это способ укладки полипептидной цепи в пространстве.
- Чтобы белок приобрел присущие ему функциональные свойства, полипептидная цепь должна определенным образом свернуться в пространстве, сформировав функционально активную структуру. Такая структура называется нативной.
- Сворачивание белка приводит к образованию глобулы
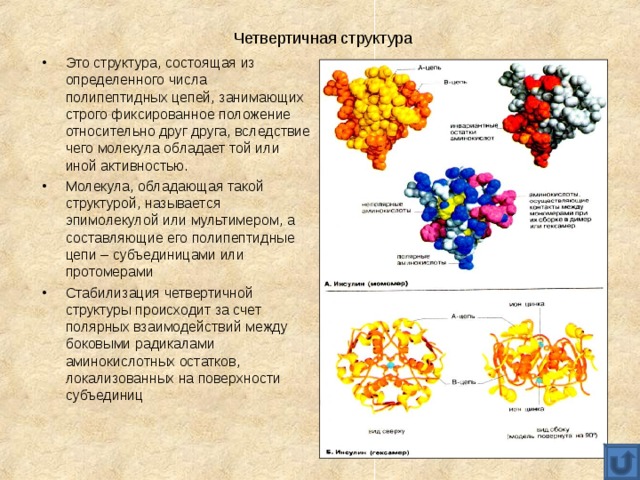
Четвертичная структура
- Это структура, состоящая из определенного числа полипептидных цепей, занимающих строго фиксированное положение относительно друг друга, вследствие чего молекула обладает той или иной активностью.
- Молекула, обладающая такой структурой, называется эпимолекулой или мультимером, а составляющие его полипептидные цепи – субъединицами или протомерами
- Стабилизация четвертичной структуры происходит за счет полярных взаимодействий между боковыми радикалами аминокислотных остатков, локализованных на поверхности субъединиц
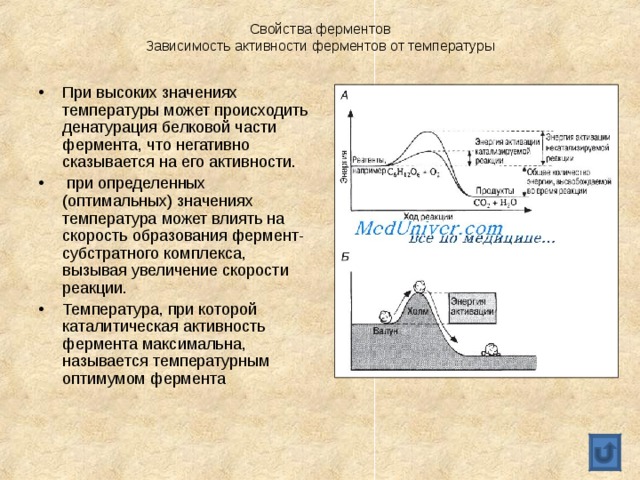
Свойства ферментов Зависимость активности ферментов от температуры
- При высоких значениях температуры может происходить денатурация белковой части фермента, что негативно сказывается на его активности.
- при определенных (оптимальных) значениях температура может влиять на скорость образования фермент-субстратного комплекса, вызывая увеличение скорости реакции.
- Температура, при которой каталитическая активность фермента максимальна, называется температурным оптимумом фермента

Зависимость активности фермента от рН-среды
СРЕДА
Значение
рН
ЖЕЛУДОЧНЫЙ СОК
ОТКЛОНЕНИЯ
1,7
Желчь печеночная
0,9 – 2,0
Желчь пузырная
7,4
Кровь (плазма)
6,2 – 8,5
6,8
5,6 – 8,0
7,4
Моча
Пот
7,25 – 7,44
5,8
Слезная жидкость
5,0 – 6,5
7,4
7,7
слюна
4,2 – 7,8
Спинномозговая жидкость
7,6 – 7,8
6,8
Сок поджелудочной железы
7,6
5,6 – 7,9
7,4 – 7,8
8,8
Сок тонкого кишечника
8,6 – 9,0
6,5
5,1 – 7,1
- Большинство ферментов проявляет максимальную активность при значениях рН, близких к нейтральным. Лишь отдельные ферменты «работают» в сильно кислой или сильно щелочной среде.
- Изменение оптимального для данного фермента значения рН-среды может привести к изменению третичной структуры фермента, что скажется на его активности.
- При изменении рН может измениться ионизация субстрата, что повлияет на образование фермент- субстратного комплекса

Классификация ферментов
- В 1961 году специальной комиссией международного биохимического союза была предложена систематическая номенклатура ферментов.
- Ферменты были подразделены на 6 групп в соответствии с общим типом реакции, которую они катализируют.
- Каждый фермент получил систематическое наименование, точно описывающее катализируемую им реакцию.
- Однако, поскольку многие из этих систематических названий оказались очень длинными и сложными, каждому ферменту было присвоено рабочее название для повседневного употребления.
- Рабочее название складывалось из названия субстрата, типа катализируемой реакции и окончания –аза.
Например:
Лактат + дегидрогенизация + аза = лактатдегидрогеназа
- Но для давно известных ферментов оставлены следующие названия, т.е. прежние названия пепсин, трипсин.

Классификация ферментов
Группа
Катализируемая реакция
Оксидоредуктазы. 480 ферментов, большая роль в энергетических процессах
Катализирует реакции окисления – восстановления, перенос атомов H и O или электронов от одного к другому.
Трансферазы
Перенос определенных группы атомов от одного вещества к другому
Гидролазы. 460 ферментов, к ним относятся пищеварительные ферменты, входящие в состав лизосом и других органоидов, где они способствуют распаду более крупных биомолекул на простые
Реакции гидролиза, при которых из субстрата образуются два продукта.
Лиазы. 230 ферментов, участвующих в регуляциях синтеза и распада промежуточных продуктов обмена
Ферменты, катализируемые реакции разрыва связей, в субстрате без присоединения воды или окисления.
Изомеразы. 80 ферментов
Ферменты, катализирующие превращения в пределах одной молекулы, они вызывают внутримолекулярные перестройки.
Лигазы (синтетазы) (около 80 ферментов)
Катализируемое соединение 2-х молекул с использованием энергии фосфатной связи, сопряжено с распадом АТФ.

Свойства ферментов
Рассмотрим действие ферментов как биокатализаторов на примере реакции, знакомой всем владельцам кошек. Речь идет о разложении мочевины, содержащейся в кошачьей моче, на диоксид углерода и аммиак. (Именно аммиаком пахнет кошачий ящик с песком, если песок в нем долго не менять.) Эта реакция катализируется ферментом уреазой . В присутствии уреазы скорость реакции превосходит нормальную во много триллионов раз:

- Одна молекула уреазы за 1 секунду расщепляет до 30 000 молекул мочевины. Не будь катализатора, на расщепление потребовалось бы примерно 30 млн лет. Ферментам свойственна высокая активность, но она меняется в зависимости от рН (концентрации ионов водорода), температуры, давления. Специфичность ферментов состоит в том, что каждый из них действует только на одну реакцию (например, уреаза расщепляет только мочевину). Фермент обладает способностью различать среди множества молекул именно те, которые должны вступать в реакцию, – эти молекулы называют субстратом (S). В контакт с субстратом вступает лишь очень небольшая часть молекулы фермента (3–5 аминокислотных остатков). Эта часть – активный центр фермента (рис. 1).
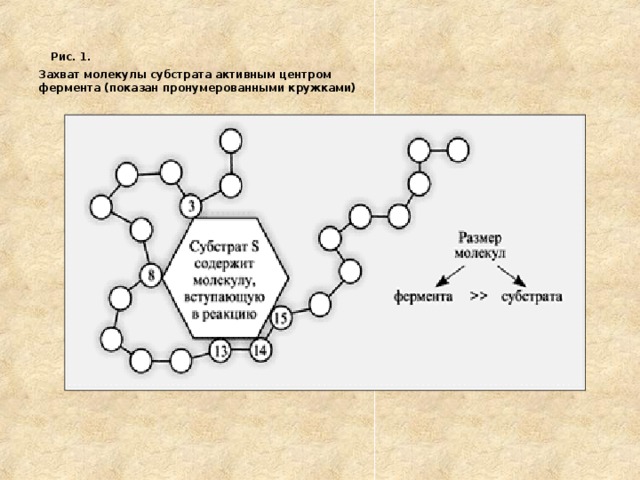
Рис. 1. Захват молекулы субстрата активным центром фермента (показан пронумерованными кружками)

Свойства ферментов
- Не расходуются в процессе катализа
- Избирательное действие на вещества – специфичны
- Высокая каталитическая активность
- Проявляют активность при определенных условиях среды
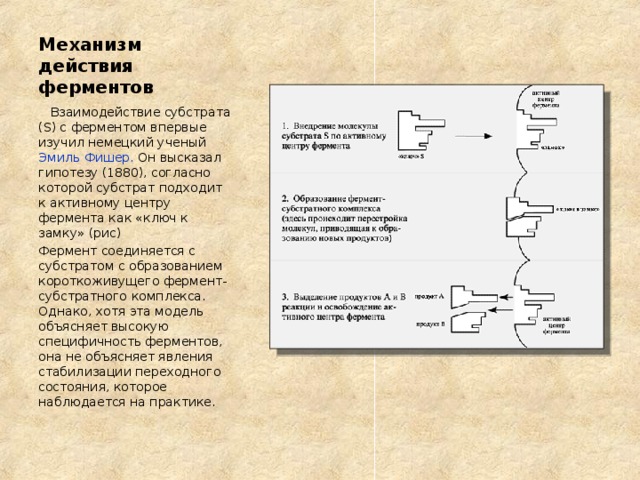
Механизм действия ферментов
Взаимодействие субстрата (S) c ферментом впервые изучил немецкий ученый Эмиль Фишер. Он высказал гипотезу (1880), согласно которой субстрат подходит к активному центру фермента как «ключ к замку» (рис)
Фермент соединяется с субстратом с образованием короткоживущего фермент-субстратного комплекса. Однако, хотя эта модель объясняет высокую специфичность ферментов, она не объясняет явления стабилизации переходного состояния, которое наблюдается на практике.
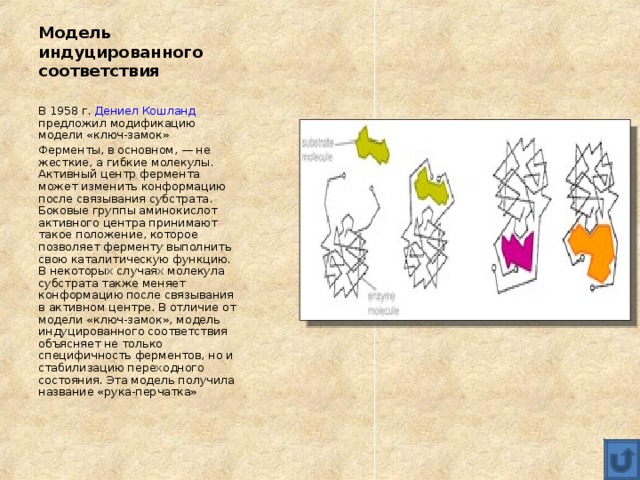
Модель индуцированного соответствия
В 1958 г. Дениел Кошланд предложил модификацию модели «ключ-замок»
Ферменты, в основном, — не жесткие, а гибкие молекулы. Активный центр фермента может изменить конформацию после связывания субстрата. Боковые группы аминокислот активного центра принимают такое положение, которое позволяет ферменту выполнить свою каталитическую функцию. В некоторых случаях молекула субстрата также меняет конформацию после связывания в активном центре. В отличие от модели «ключ-замок», модель индуцированного соответствия объясняет не только специфичность ферментов, но и стабилизацию переходного состояния. Эта модель получила название «рука-перчатка»
Применение ферментов
Ферменты получили широкое применение в легкой, пищевой и химической промышленности, а также в медицинской практике
- В пищевой промышленности ферменты используют при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей В животноводстве ферменты используют при приготовлении кормов Ферменты используют при изготовлении фотоматериалов Ферменты используют при обработке овса и конопли Ферменты используют для смягчения кожи в кожевенной промышленности Ферменты входят в состав стиральных порошков, зубных паст В медицине ферменты имеют диагностическое значение – определение отдельных ферментов в клетке помогает распознаванию природы заболевания (например вирусный гепатит – по активности фермента в плазме крови) их используют для замещения недостающего фермента в организме
- В пищевой промышленности ферменты используют при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей
- В животноводстве ферменты используют при приготовлении кормов
- Ферменты используют при изготовлении фотоматериалов
- Ферменты используют при обработке овса и конопли
- Ферменты используют для смягчения кожи в кожевенной промышленности
- Ферменты входят в состав стиральных порошков, зубных паст
- В медицине ферменты имеют диагностическое значение – определение отдельных ферментов в клетке помогает распознаванию природы заболевания (например вирусный гепатит – по активности фермента в плазме крови) их используют для замещения недостающего фермента в организме

Тест «Ферменты»

1. Что такое фермент:
- А) вещества, замедляющие скорость протекания химических реакций
- Б) вещества, увеличивающие скорость протекания химических реакций
- В) питательные вещества клетки

2. Почему при низких температурах ферменты теряют свою активность:
- А) в клетке накапливаются ядовитые вещества
- Б) изменяется пространственная структура молекул
- В) уменьшается содержание ферментов в клетке

3. К какой группе веществ относится липаза, ускоряющая реакцию расщепления жиров:
- А) к ферментам
- Б) к аминокислотам
- В) к гормонам

4. Почему под влиянием высоких температур ферменты теряют свою активность:
- А) изменяется активность субстрата
- Б) изменяется пространственная структура молекул
- В) уменьшается содержание ферментов в клетке

5. Какую функцию выполняют ферменты, содержащиеся в клетках всех организмов:
- А) обеспечивают клетке строительный материал
- Б) служат энергетическим веществом клетки
- В) ускоряют химические реакции в клетке

6. Что собой представляет каталаза, увеличивающая скорость разложения пероксида водорода:
- А) гормон
- Б) полисахарид
- В) фермент

7. При какой температуре наступает оптимальная активность ферментов у животных:
- А) 40 – 50 о С
- Б) 30 – 40 о С
- В) 50 о С

8. Что происходит с ферментом при его взаимодействии с субстратом:
- А) фермент не изменяется
- Б) фермент превращается в новое вещество
- В) фермент мутирует

ОШИБКА …

ОТЛИЧНО!

Выводы
- Ферменты – это биологические катализаторы, то есть вещества, которые ускоряют биохимические реакции
- Не расходуются в процессе катализа
- Специфичны – избирательно действуют на вещества
- Высокая каталитическая активность
- Проявляют активность при определенных условиях среды