
Белки. Нуклеиновые кислоты.
Белки–полимеры, структурная единица которых аминокислота.
Аминокислоты соединены между собой пептидной связью.

Классификация АК
По химическому строению
1) Алифатические – глицин (Гли), аланин (Ала), валин (Вал), лейцин (Лей), изолейцин (Илей);
2) Оксикислоты – серин (Сер), треанин (Тре);
3) Дикарбоновые – аспарагин (Асп), глутамин (Глу), аспарагиновая кислота (Аск), глутаминовая кислота (Глк);
4) Двуосновные – лизин (Лиз), гистидин (Гис), аргинин (Арг);
5) Ароматические – фениналанин (Фен), тирозин (Тир), триптофан (Три);
6) Серосодержащие – цистеин (Цис), метионин (Мет).

По биохимической роли:
1) глюкогенные – через ряд химических превращений поступают на путь гликолиза (окисления глюкозы) – Гли, Ала, Тре, Вал, Аск, Глк, Арг, Гис, Мет.
2) кетогенные – участвуют в образовании кетоновых тел - Лей, Илей, Тир, Фен.
По заменимости:
1) Незаменимые – не синтезируются в организме – Гис, Иле, Лей, Лиз, Мет, Фен, Тре, Три, Вал, а у молодняка Арг, Гис.
2) Заменимые – остальные.
Первичная структура белка
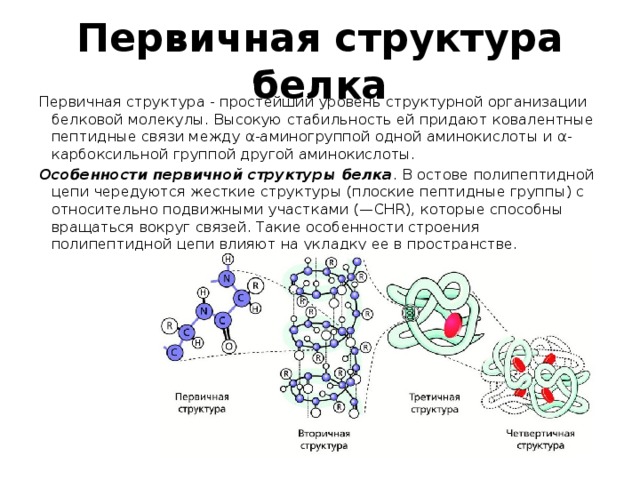
Первичная структура - простейший уровень структурной организации белковой молекулы. Высокую стабильность ей придают ковалентные пептидные связи между α-аминогруппой одной аминокислоты и α-карбоксильной группой другой аминокислоты.
Особенности первичной структуры белка . В остове полипептидной цепи чередуются жесткие структуры (плоские пептидные группы) с относительно подвижными участками (—СНR), которые способны вращаться вокруг связей. Такие особенности строения полипептидной цепи влияют на укладку ее в пространстве.
Вторичная структура белка
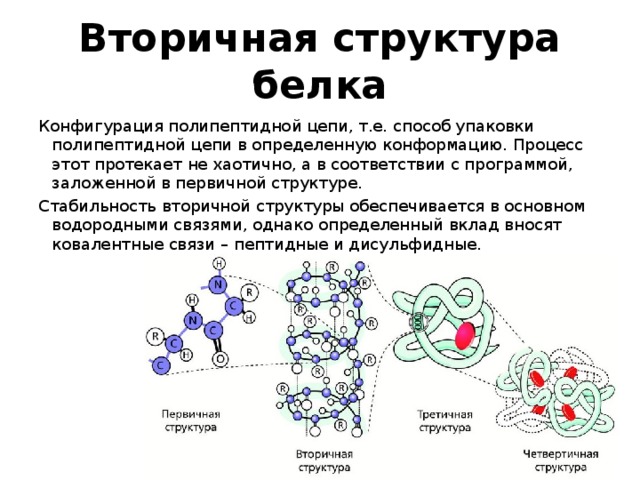
Конфигурация полипептидной цепи, т.е. способ упаковки полипептидной цепи в определенную конформацию. Процесс этот протекает не хаотично, а в соответствии с программой, заложенной в первичной структуре.
Стабильность вторичной структуры обеспечивается в основном водородными связями, однако определенный вклад вносят ковалентные связи – пептидные и дисульфидные.
Третичная структура белка
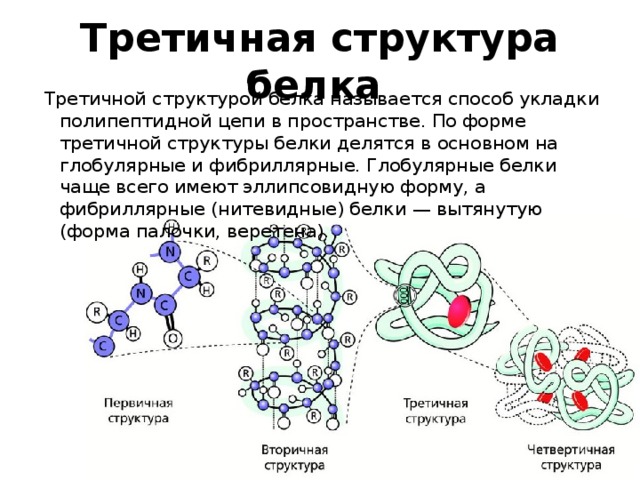
Третичной структурой белка называется способ укладки полипептидной цепи в пространстве. По форме третичной структуры белки делятся в основном на глобулярные и фибриллярные. Глобулярные белки чаще всего имеют эллипсовидную форму, а фибриллярные (нитевидные) белки — вытянутую (форма палочки, веретена).
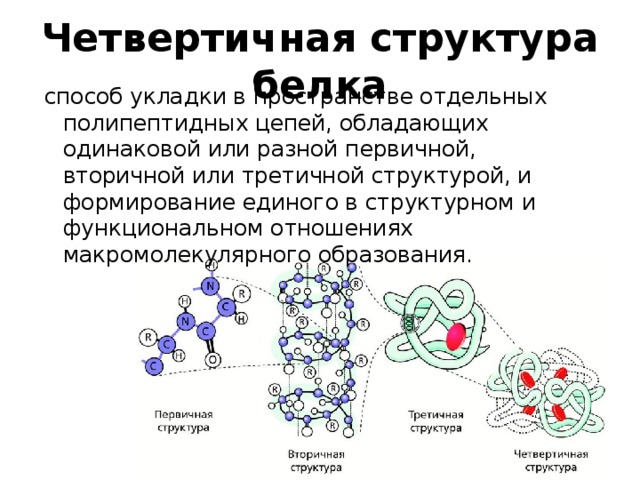
Четвертичная структура белка
способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой или разной первичной, вторичной или третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярного образования.


Функции белков
Структурная – белками образованы многие клеточные компоненты, а в комплексе с липидами они входят в состав клеточных мембран.
Каталитическая – все биологические катализаторы.
Транспортная – белок гемоглобин транспортирует кислород, ряд других белков образуя комплекс с липидами транспортируют их по крови и лимфе (пример: миоглобин, сывороточный альбумин).
Регуляторная – ряд гормонов и других биологически активных веществ имеют белковую природу (пр.: инсулин).
Защитная – антитела (иммуноглобулины) являются белками, кроме того основу кожи составляет белок коллаген, а волос – креатин.
Опорная – сухожилия, поверхности суставов соединения костей образованы в значительной степени белковыми веществами (пр.: коллаген, эластин).
Энергетическая – аминокислоты белков могут поступать на путь гликолиза, который обеспечивает клетку энергией.
Рецепторная – многие белки участвуют в процессах избирательного узнавания (рецепторы).

Нуклеиновые кислоты – биополимеры, состоящие из пуринового или пиримидинового основания, углеводов (рибозы и дезоксирибозы) и фосфатных групп.
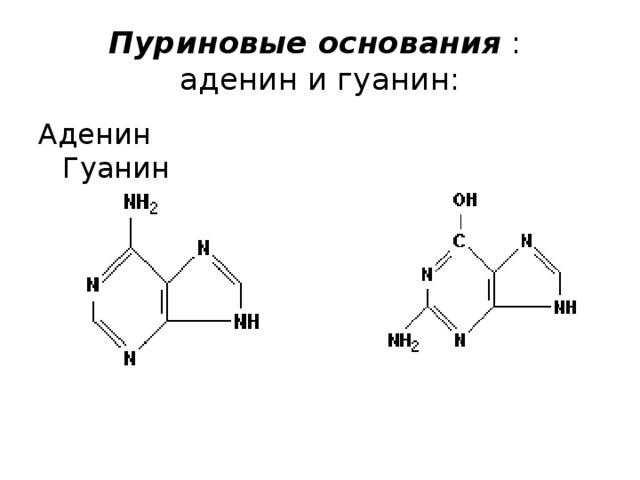
Пуриновые основания : аденин и гуанин:
Аденин Гуанин
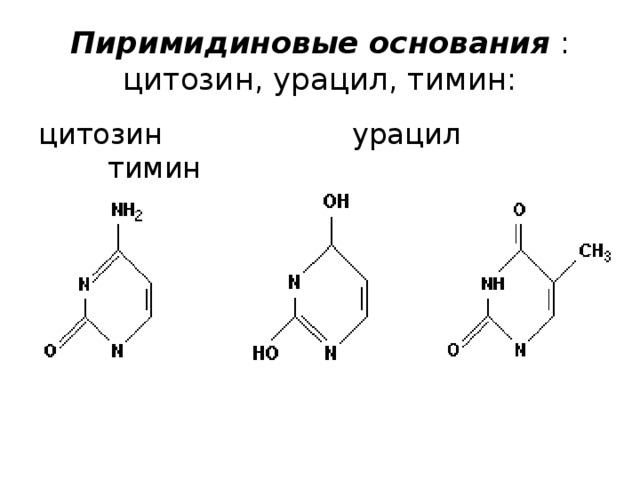
Пиримидиновые основания : цитозин, урацил, тимин:
цитозин урацил тимин
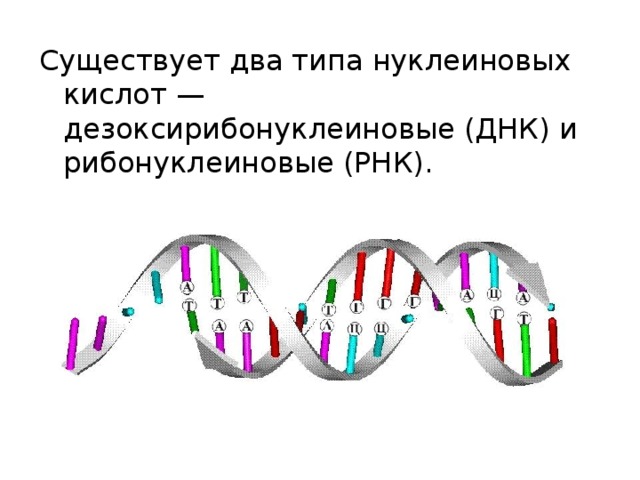
Существует два типа нуклеиновых кислот — дезоксирибонуклеиновые (ДНК) и рибонуклеиновые (РНК).

В ДНК входят четыре вида нуклеотидов, отличающихся по азотистому основанию в их составе: аденин (А), гуанин (Г), цитозин (Ц) и тимин (Т).
В молекуле РНК также имеется 4 вида нуклеотидов с одним из азотистых оснований-аденином, гуанином, цитозином и урацилом (У).
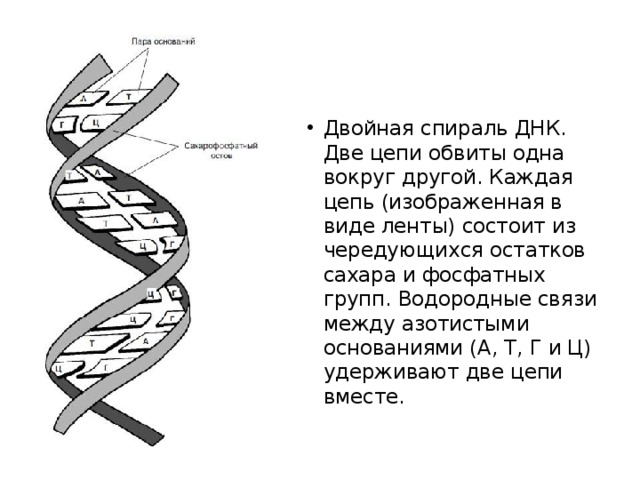
- Двойная спираль ДНК. Две цепи обвиты одна вокруг другой. Каждая цепь (изображенная в виде ленты) состоит из чередующихся остатков сахара и фосфатных групп. Водородные связи между азотистыми основаниями (А, Т, Г и Ц) удерживают две цепи вместе.
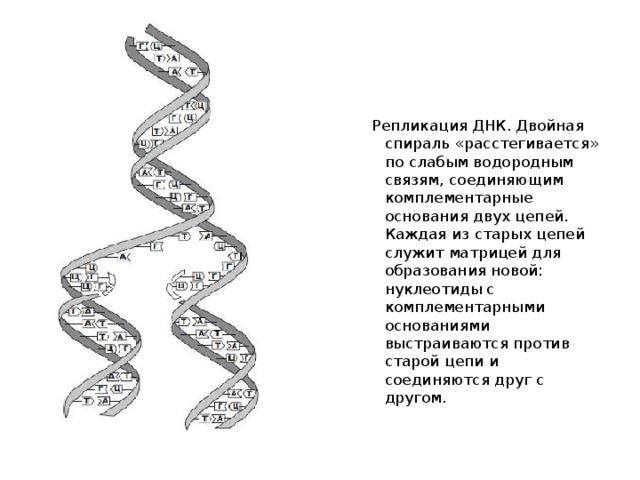
Репликация ДНК. Двойная спираль «расстегивается» по слабым водородным связям, соединяющим комплементарные основания двух цепей. Каждая из старых цепей служит матрицей для образования новой: нуклеотиды с комплементарными основаниями выстраиваются против старой цепи и соединяются друг с другом.

Молекулы РНК, как правило, одноцепочечные (в отличие от ДНК) и содержат значительно меньшее число нуклеотидов.
Выделяют три вида РНК, различающиеся по величине молекул и выполняемым функциям, — информационную (иРНК), рибосомальную (рРНК) и транспортную (тРНК).


Информационная РНК (и-РНК) располагается в ядре и цитоплазме клетки, имеет самую длинную полинуклеотидную цепь среди РНК и выполняет функцию переноса наследственной информации из ядра в цитоплазму клетки.
Транспортная РНК (т-РНК) также содержится в ядре и цитоплазме клет-ки, ее цепь имеет наиболее сложную структуру, а также является самой короткой (75 нуклеотидов). Т-РНК доставляет аминокислоты к рибосомам в процессе трансляции — биосинтеза белка.

Рибосомальная РНК (р-РНК) содержится в ядрышке и рибосомах клетки, имеет цепь средней длины. Все виды РНК образуются в процессе транскрипции соответствующих генов ДНК.
Матричная РНК (м-РНК) содержащая информацию о первичной структуре белков. мРНК синтезируется на основе ДНК в ходе транскрипции, после чего, в свою очередь, используется в ходе трансляции как матрица для синтеза белков.













































