Просмотр содержимого документа
«Алкены для 10го класса на узбекском языке»
Тўйинмаган углеводородлар Этилен углеводородлари (алкенлар, олефинлар)
Тўйинмаган углеводородлар
АЛКЕНЛАР АЛКИНЛАР АЛКАДИЕНЛАР
С n H 2n С n H 2n - 2

- Тўйинмаган углеводородлар деб углерод сони алкан ларникига тенг бўлиб, водород сони алкан ларникидан 2,4,6 … га кам бўлган углеводородларга айтилади.
- Тўйинмаган углеводородлар битта қўшбоғли – этилен, иккита қўшбоғли – диен ва уч боғли – ацетилен углеводородларига бўлинадилар.

Маъруза режаси:
- Изомерияси ва номланиши
- Олиниш усуллари
- Физик ва кимёвий хоссалари
- Алкенларнинг полимерланиш реакциялари
- Айрим вакиллари
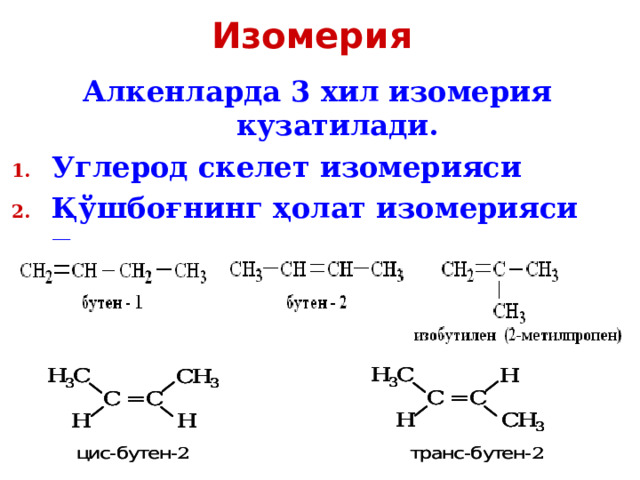
Изомерия
Алкенларда 3 хил изомерия кузатилади.
- Углерод скелет изомерияси
- Қўшбоғнинг ҳолат изомерияси
- Геометрик изомерия

Номенклатура
- Эмпирик номенклатура – алкандаги –ан қўшимчасини –илен қўшимчасига алмаштириб ҳосил қилинади:
СН 2 = СН 2 - этилен
СН 3 – СН = СН 2 - пропилен
- Рационал номенклатура – этиленни асос қилиб олинади ва унинг гомологлари этеленнинг ҳосилалари деб қаралади:
СН 3 – СН = СН 2 - метилэтилен

- Систематик номенклатура бўйича алкенлар номи тегишли алканлар номи охиридаги –ан қўшимчасини –ен қўшимчасига алмаштириб ҳосил қилинади. Радикалларнинг номи ва ҳолати рақамлар билан кўрсатилади.
Т ўйинмаган бир валентли радикаллар:
- СН 2 =СН – винил (этенил),
- СН 2 =СН–СН 2 – аллил (1-пропенил),
- СН 2 = С – СН2- изопропенил (1-пропенил-2).
–
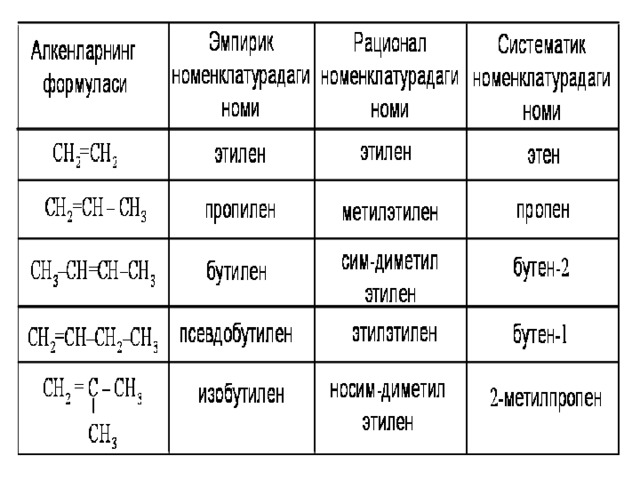
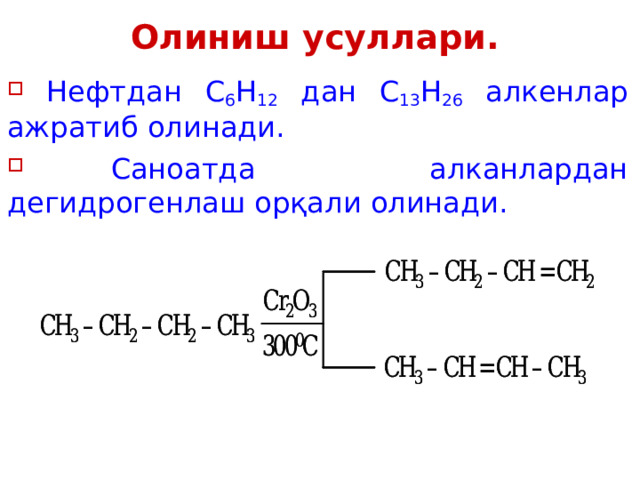
Олиниш усуллари.
- Нефтдан С 6 Н 12 дан С 13 Н 26 алкенлар ажратиб олинади.
- Саноатда алканлардан дегидрогенлаш орқали олинади.

Лаборатория шароитида олиш
- Тўйинган бир атомли спиртларни дегидратлаш (к атализатор - сульфат ва фосфат кислоталар, калий бисульфат, фосфор-(V)-оксид).
Зайцев қоидаси : В одород энг кам водород тутган углерод атомидан ажралади .

2. Дегидрогалогенлаш реакцияси
- Г алоид водородни тортиб олувчи восита сифатида қуруқ ишқорнинг спиртдаги эритмаси, учламчи амин, хинолиндан фойдаланилади.
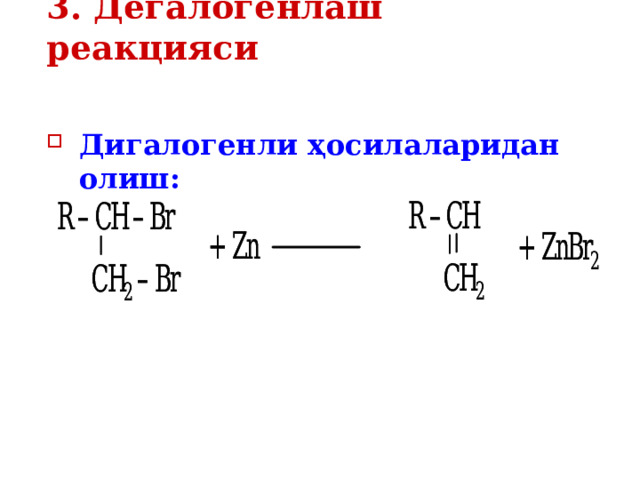
3 . Дегалогенлаш реакцияси
- Ди галогенли ҳосилаларидан олиш:

4. Ацетилен СНларни палладий катализаторлигида гидрогенлаш

Физик хоссалари.
- Д астлабки тўрт вакили газсимон, С 5 Н 10 дан С 12 Н 24 гача суюқлик, қолганлари қаттиқ моддалар.
- Тўғри занжирлилар тармоқланган занжирли изомерларига қараганда, Цис-изомерлари транс-изомерларига нисбатан юқори ҳароратда қайнайди.
- Олефинларнинг зичлиги бирдан кичик, лекин тегишли парафинларникидан катта.
- Олефинлар сувда оз эрийди.
- ИҚ спектрда винил гуруҳидаги қўшбоғнинг валент тебранишлари 1050 см -1 да С – Н – боғланишнинг деформация тебраниши 920 ва 980 см -1 да намоён бўлади.
- УБ нурларни 190-200 нм ютади.
- ЯМР спектрда 4,5-6,0 м.д. да намоён бўлади.

Кимёвий ҳусусиятлари.
- Алкенлар бирикиш, алмашиниш, изомерланиш, полимерланиш, оксидланиш реакцияларига киришади. Алмашиниш қўшбоғга нисбатан -ҳолатда жойлашган углероддаги водородлар ҳисобига боради:
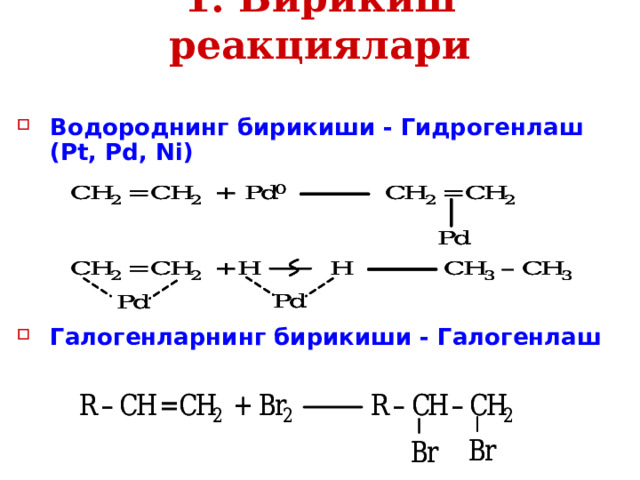
1. Бирикиш реакциялари
- Водороднинг бирикиши - Гидрогенлаш (Pt, Pd, Ni)
- Галогенларнинг бирикиши - Галогенлаш
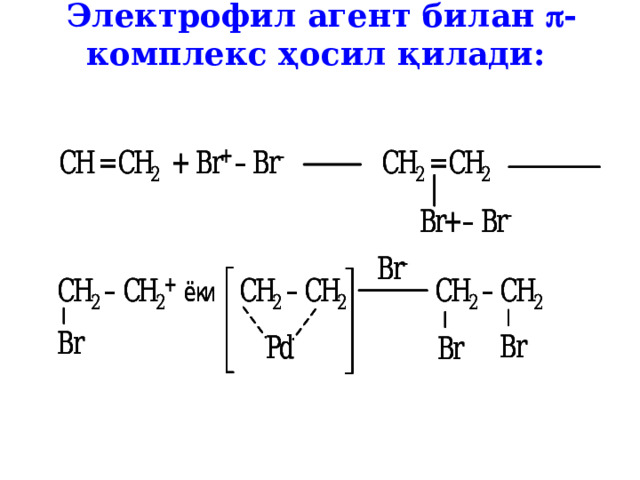
Э лектрофил агент билан -комплекс ҳосил қилади:
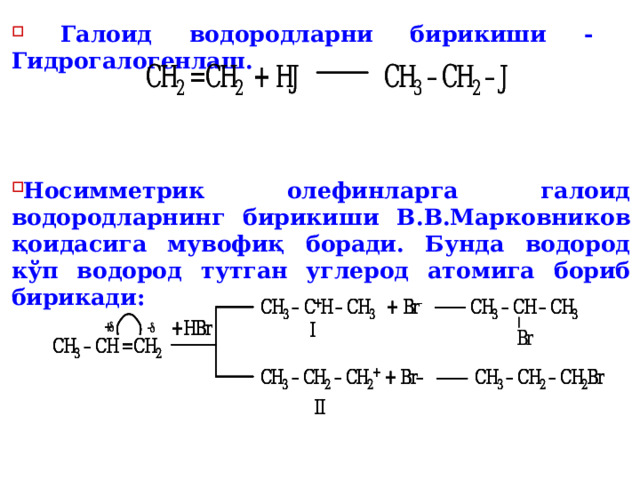
- Г алоид водородларни бирикиши - Гидрогалогенлаш.
- Носимметрик олефинларга галоид водородларнинг бирикиши В.В.Марковников қоидасига мувофиқ боради. Бунда водород кўп водород тутган углерод атомига бориб бирикади:
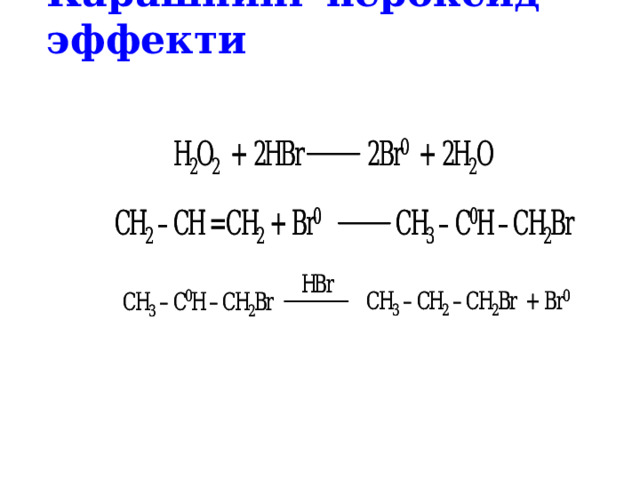
Карашнинг пероксид эффекти

Гипогалогенлаш - Марковников қоидасига асосан боради:
Сувнинг бирикиши – Гидратлаш (жараён карбокатионли механизм бўйича боради).
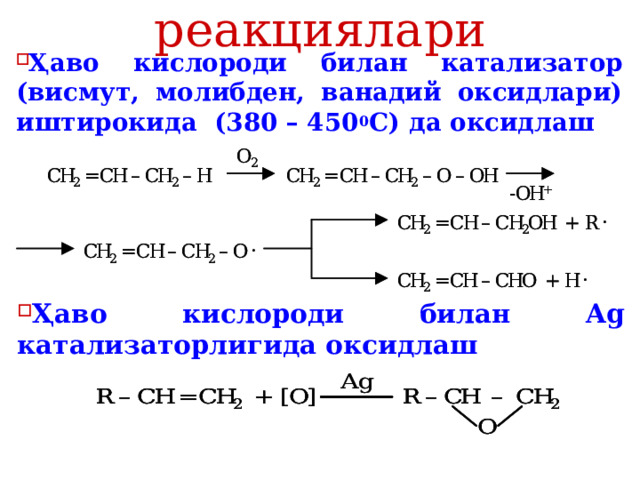
Оксидланиш реакциялари
- Ҳаво кислороди билан катализатор (висмут, молибден, ванадий оксидлари) иштирокида (380 – 450 0 С) да оксидлаш
- Ҳаво кислороди билан Ag катализаторлигида оксидлаш
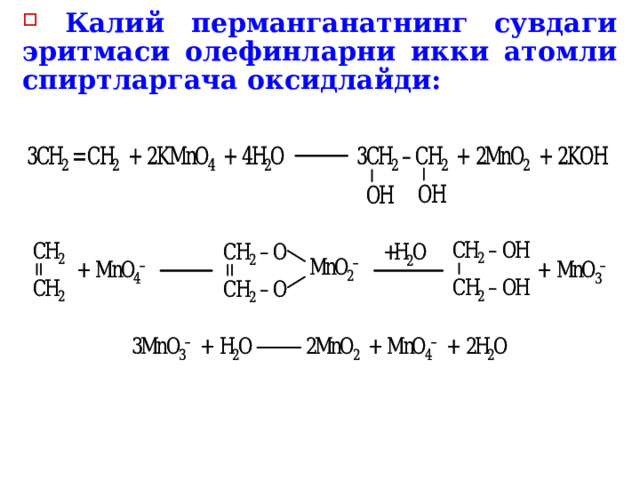
- Калий перманганатнинг сувдаги эритмаси олефинларни икки атомли спиртларгача оксидлайди:
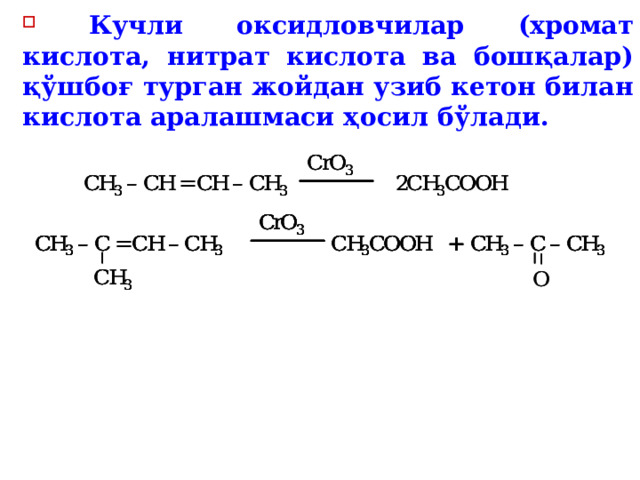
- Кучли оксидловчилар (хромат кислота, нитрат кислота ва бошқалар) қўшбоғ турган жойдан узиб кетон билан кислота аралашмаси ҳосил бўлади.
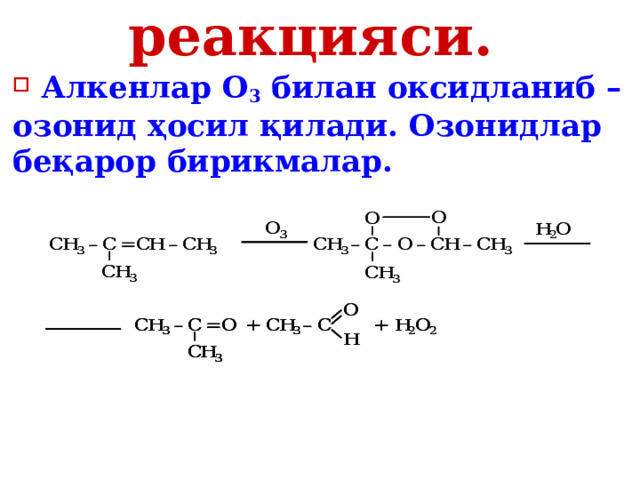
Озонлаш реакцияси.
- Алкенлар О 3 билан оксидланиб – озонид ҳосил қилади. Озонидлар беқарор бирикмалар.
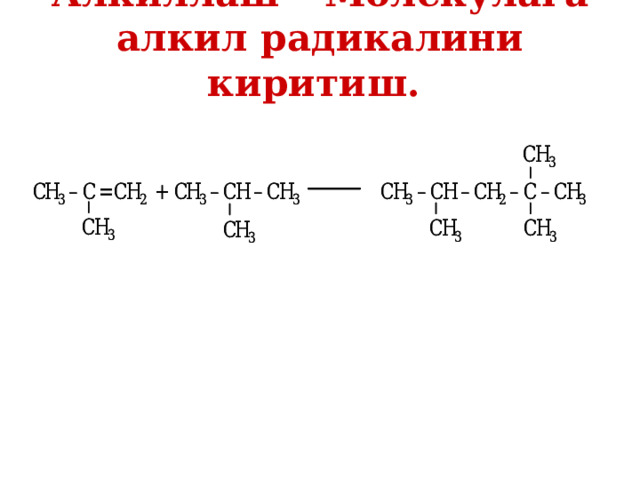
Алкиллаш – Молекулага алкил радикалини киритиш.

Қайта гуруҳланиш.

Полимерланиш.
- Полимерланиш – Молекулаларнинг ўзаро бирикиб, юқори молекуляр бирикма ҳосил қилиши.
- Гомополимерланиш – Бир хил молекулаларни бирикиши.
- Сополимерланиш (кополимерланиш) – Ҳар хил молекулаларни бирикиши.

Полимерланиш жараёни радикал ёки ионли (каталитик) механизм билан содир бўлиши мумкин.
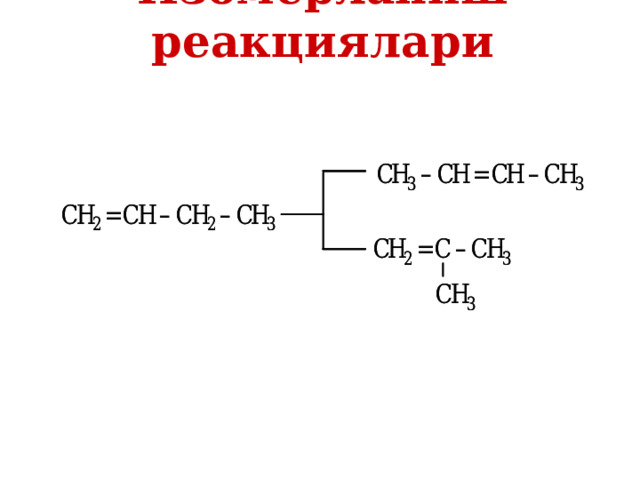
Изомерланиш реакциялари

Алмашиниш реакциялари.
Саноатда бу жараёндан глицерин ишлаб чиқаришда фойдаланилади.

- Оксосинтез. Олефинларнинг энг қимматли ҳусусиятларидан бири СО ва Н 2 (100 – 500 атм, 100 – 500 0 С кобальт карбонили катализатор) билан бирикиши.

- Олефинлар орасида катта аҳамиятга эга бўлганлари этилен ва пропилен.
- Эритувчилар, полимерлар, спиртлар, альдегидлар, кетонлар ва бошқалар олинади.

























































