Конкурсное испытание «Урок»
Тема: Кислород: нахождение в природе и способы получения
или «Пока дышу, надеюсь»
Цель: расширить знания учащихся о химическом элементе кислороде и простых веществах — кислороде и озоне, их нахождение в природе; усвоение понятий “аллотропия” и “аллотропные модификации”; знакомство с историей открытия простого вещества — кислород и способы его получения и собирания.
Задачи урока
Образовательные: познакомить учащихся с общей характеристикой элемента и простого вещества, рассмотреть распространенность кислорода в природе, изучить основные способы получения кислорода.
Воспитательные: формирование у учащихся таких черт характера, как трудолюбие, дисциплинированность, ответственность, аккуратность, положительное отношение к учёбе, воспитывать культуру общения через работу в парах «ученик-ученик», «ученик-учитель».
Развивающие: развитие у учащихся умения анализировать, сравнивать, обобщать учебный материал; развитие познавательных умений - слушать, выделять главное, составлять план, наблюдать, ставить проблемы и решать их.
Планируемые результаты
Предметные: уметь сопоставлять характеристики кислорода как химического элемента и простого вещества, знать основные способы получения кислорода в промышленности и лаборатории, распространенность в природе.
Личностные: проявлять интерес к самостоятельной учебной деятельности, навыкам сотрудничества в совместной работе, творческого отношения к процессу обучения; осознания здорового и безопасного образа жизни; понимания необходимости соблюдения экологической культуры.
Метапредметные:
Познавательные. Умение: находить способы решения проблем поискового характера; развивать исследовательское мышление, способность оригинально мыслить и самостоятельно решать поставленные задачи, обобщать полученную информацию, вести наблюдение прогнозировать ситуацию.
Регулятивные. Умение: выполнять учебное задание в соответствие с целью, выполнять учебное действие в соответствии с заданием, контролировать, оценивать свои действия.
Коммуникативные. Умение: развивать коммуникативное мышление в условиях метапредметного обучения. Формулировать высказывания, сравнивать, анализировать, обобщать и переносить информацию с одного вида деятельности на другой, накапливать знания, слушать собеседника и вести диалог.
Тип урока: изучение нового материла (комбинированный)
Методы: объяснительно – иллюстративные
Формы: фронтальная, групповая
Оборудование: компьютер, проектор, экран, ресурсы сети «Интернет», презентация, рабочие листы
План урока
1. Организационный момент (1 мин)
2. Актуализация знаний. Целеполагание (3-5 мин)
3. Изучение нового материала (20 мин)
4. Проверка усвоения материала (3-5 мин)
5. Домашнее задание (2 мин)
6. Рефлексия (1 мин)
7. Итоги (1 мин)
Ребята заходят в класс. Делятся на три группы. Делятся выбирая кружочек (кружочки трех разных цветов).
Ребята, прежде, чем вы сядете, выберите пожалуйста один из цветных кружочков и займите места согласно цвету кружочка.
Ход урока
1. Организационный момент (1 мин) (слайд 1)
Ребята, прежде, чем вы сядете, выберите пожалуйста один из цветных кружочков и займите места согласно цвету кружочка.
Добрый день! Меня зовут Лейла Бийсолтановна. Я рада приветствовать вас и надеюсь, что мы с вами сегодня испытаем самые наилучшие эмоции на нашем уроке. Как ваше настроение? У вас на столе лежат карточки, откройте и подпишите их. В конце урока мы вернемся к ним.
2. Актуализация знаний. Целеполагание (3 – 5 мин) (слайд 2)
Сегодняшний наш урок хочу начать с латинской пословицы «Пока дышу, надеюсь». Как вы думаете, о чем мы с вами будем сегодня говорить?
Задание «Кроссворд» с ключевым словом «Кислород»
|
|
| 1 э |
К |
с |
п |
е |
р |
и |
м |
е |
н |
т |
|
| 2 с |
п |
И |
р |
т |
о |
в |
к |
а |
|
|
|
| 3 С | м | е | с | ь |
|
|
| 4 в | а | Л | е | н | т | н | о | с | т | ь |
|
|
| 5 а | т | О | м |
|
|
|
|
|
|
|
|
|
| 6 б | е | Р | ц | е | л | и | у | с |
|
|
| 7 м | О | л | е | к | у | л | а |
|
| 8с | о | е | Д | и | н | е | н | и | е |
|
|
|
Вопросы:
1. Метод исследования какого – либо явления в определенных условиях.
2. Горелка для жидкого топлива.
3. Вещество, не имеющее постоянного состава.
4. Свойство атома ХЭ присоединять определенное число атомов другого элемента.
5. Мельчайшая химическая неделимая частица вещества.
6. Шведский химик, определивший атомные массы 45 химических элементов.
7. Мельчайшие химически делимые частица, состоящие из атомов.
8. Процесс образования сложных веществ.
Абсолютно верно, тема нашего сегодняшнего урока «Кислород: нахождение в природе и способы получения» (слайд 3)
Как вы думаете, почему кислород – это первый химический элемент, с которого мы начинаем изучение?
3. Изучение нового материла
1. Нахождение в природе. (слайд 4)
(- Кислород самый распространённый химический элемент на Земле).
Вспомните, из курса географии, где находится кислород в природе (атмосфера, гидросфера, литосфера).
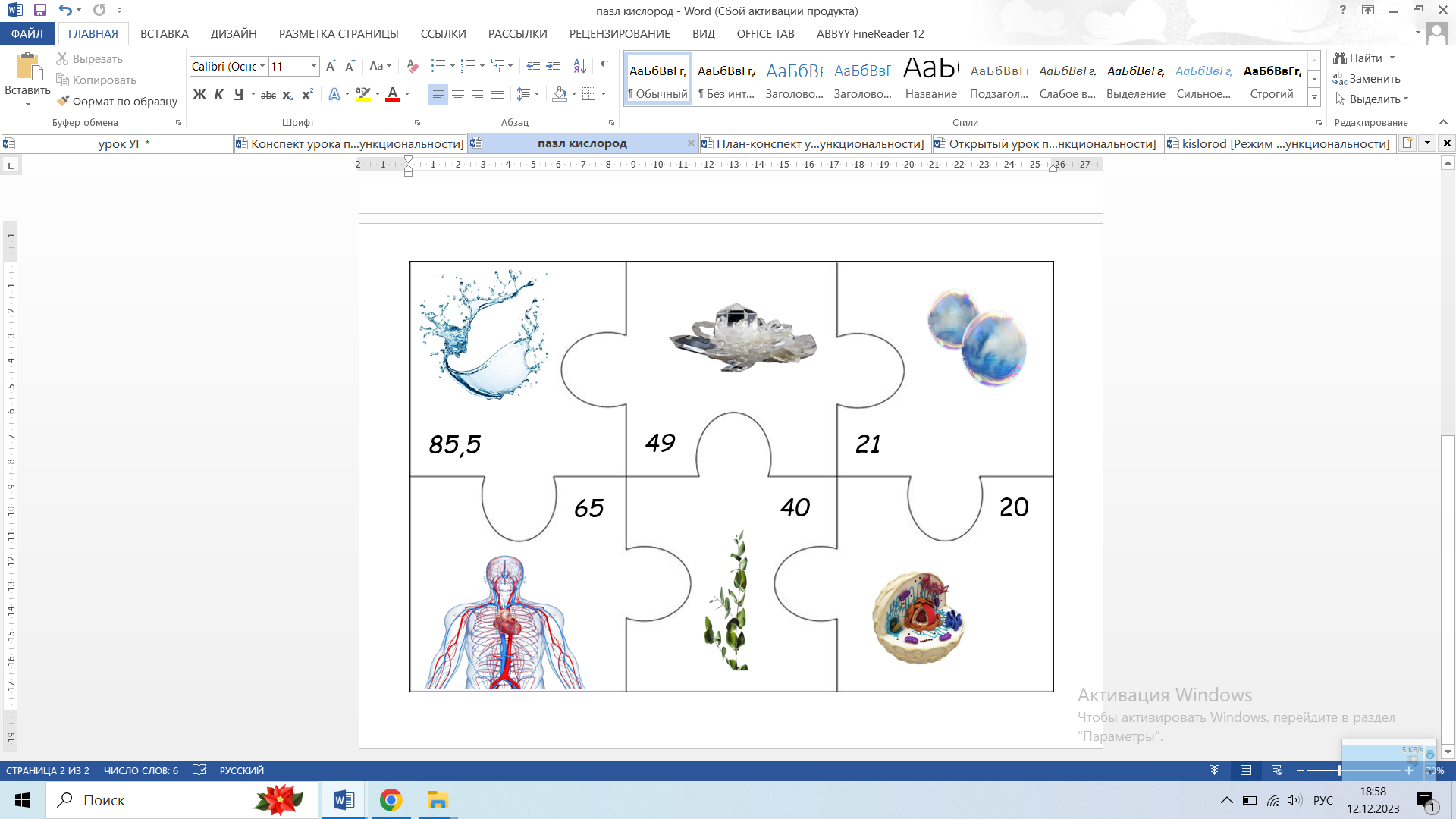
Морские и пресные воды содержат огромное количество связанного кислорода – 85,5%, в атмосфере содержание свободного кислорода составляет 21% по объему и 23% по массе. Более 1500 соединений земной коры в своем составе содержат кислород. Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет около 20%. Для химического элемента кислорода характерны две разные аллотропные модификации – озон и молекулярный кислород. (слайд 5)
Если какой – либо элемент образует два или несколько простых веществ, то такие вещества называются аллотропными модификациями. Само это явление называется аллотропией.
2. Общая характеристика элемента
На доске план характеристика (выделенное жирным будет распечатано)
Символ – О
Положение в ПСХЭ - VI Гр (А), 2 период, порядковый номер – 8
Химическая природа – неметалл
Относительная атомная масса – Ar = 16
Валентность – II
Химический элемент кислород образует простое вещество кислород.
Молекула кислорода – О2
Относительная молекулярная масса = 32
3. История открытия
“1 августа 1774 г. Я попытался извлечь воздух из ртутной окалины (оксида ртути) и нашел, что воздух легко может быть изгнан из нее посредством линзы. Этот воздух не поглощался водой. Каково же было мое изумление, когда я обнаружил, что свеча горит в этом воздухе необычайно ярким пламенем. Тщетно пытался я найти объяснение этому явлению”. (слайд 6)
Открытие кислорода является одним из важнейших событий в истории, и связано с именами учёных Д. Пристли, К .Шееле и А. Лавуазье (слайд 7)
Каким образом ученые получали кислород?
4. Способы получения кислорода (слайд 8)
Получение в промышленности
 Электролиз воды: 2H2O эл.ток 2H2↑ + O2↑
Электролиз воды: 2H2O эл.ток 2H2↑ + O2↑
Сжижение воздуха под давлением: Воздух = p, t=- 183°C= О2 (голубая жидкость)
Получение в лаборатории
Разложение перманганата калия (марганцовка):
 2KMnO4 t,°C K2MnO4+MnO2+O2↑
2KMnO4 t,°C K2MnO4+MnO2+O2↑
Разложение перекиси водорода:
 2H2O2 катализатор 2H2O + O2↑
2H2O2 катализатор 2H2O + O2↑
Разложение бертолетовой соли:
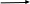 2KClO3 катализатор, t, 0C 2KCl + 3O2↑
2KClO3 катализатор, t, 0C 2KCl + 3O2↑
Более подробно мы рассмотрим получение кислорода разложением перманганата калия. Практическая работа. Получение кислорода методом вытеснения воздуха.
В лабораториях небольшие количества кислорода можно получать нагреванием перманганата калия (марганцовка) KMnO4. Кислород мало растворим в воде и тяжелее воздуха, поэтому его можно получать двумя способами:
1. вытеснением воды;
2. вытеснением воздуха (кислород будет собираться на дне сосуда). (слайд 9)
4. Проверка усвоения материала. Каждая группа получает творческое задание.
1 группа. Смарт карточки «Кислород»
2 группа. Игра «Ассоциации»
3 группа. Создай свою сказку.

6. Домашнее задание (слайд 10)
Ребята, у вас на столах лежат листочки со штрих кодами, вам нужно будет отсканировать этот код и пройти тестирование. Ваши результаты я увижу у себя в личном кабинете и отправлю вашему учителю.

7. Рефлексия
Возвращаемся к карточкам, подписанным в начале урока. Ребята, проанализируйте свою работу на уроке – все ли вам было понятно, можно ли будет применять полученные знания в дальнейшем? Оцените свои знания, используя эталонную шкалу рН, где кислая среда – материал не понятен, щелочная среда – в материале разобрался и могу применять. Укажите выбранную кислотность, написав в специальном поле соответствующую цифру.

8. Итоги.
Дорогие ребята, спасибо вам за сегодняшнее занятие. Без вас это событие не состоялось бы. Вы большие молодцы! Очень активно себя проявили. Спасибо вам еще раз.







 Электролиз воды: 2H2O эл.ток 2H2↑ + O2↑
Электролиз воды: 2H2O эл.ток 2H2↑ + O2↑ 2KClO3 катализатор, t, 0C 2KCl + 3O2↑
2KClO3 катализатор, t, 0C 2KCl + 3O2↑






















