МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«ЗОРКИНСКАЯ СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА – ДЕТСКИЙ САД»
НИЖНЕГОРСКОГО РАЙОНА РЕСПУБЛИКИ КРЫМ
| РАССМОТРЕНО на заседании методического объединения учителей естественно- математического цикла Руководитель МО: ________ Суфан С.В. Протокол №_____от_______
|
|
|
ФОНД
ОЦЕНОЧНЫХ СРЕДСТВ
по химии
для 8 класса
Учитель-составитель Турчин Дмитрий Викторович
с. Зоркино
2021 год
Паспорт
фонда оценочных средств
по химии в 8 классе
| № п/п | Контролируемые разделы (темы) дисциплины* | Наименование оценочного средства
|
| 1 | Первоначальные химические понятия | Контрольная работа №1 |
| 2 | Кислород. Водород. Вода. Растворы | Контрольная работа № 2 |
| 3 | Количественные отношения в химии. Основные классы неорганических соединений | Контрольная работа № 3
|
| 4 | Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение вещества. Химическая связь. | Контрольная работа № 4 |
Контрольная работа №1
Вариант 1
1.1. Из представленных ниже рисунков выберите тот, на котором изображено протекание химической реакции.

Протекание химической реакции изображено на рисунке:________
Объясните сделанный вами выбор: _________________________
________________________________________________________________________________________________
1.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:_____________________________________ ________________________
И
2.1. Укажите, какой из приведённых ниже процессов является химической реакцией.
1. Распространение аромата цветов в комнате.
2. Движение маятника в механических часах.
3. Образование накипи в чайнике при кипячении водопроводной воды.
Напишите номер выбранного процесса:____________
Объясните сделанный вами выбор: _________________________
________________________________________________________________________________________________
2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:____________________________________ _______________________________________
Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами в быту. В ответе запишите цифры, под которыми они указаны. (В задании может быть несколько верных суждений.)
1) Углекислый газ способствует появлению «парникового эффекта», что представляет угрозу для окружающей среды и здоровья человека. 2) Запрещается нагревать герметично закрытую колбу с жидкостью. 3) Вещества, находящиеся в лаборатории, можно пробовать на вкус. 4) Средства бытовой химии допускается хранить вместе с продуктами питания.
Ответ: __________________________.
Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами. В ответе запишите цифры, под которыми они указаны. (В задании может быть несколько верных суждений.)
1) В химическом кабинете разрешается пробовать вещества на вкус. 2) Для получения разбавленных растворов H2SO4 концентрированную серную кислоту осторожно приливают к дистиллированной воде. 3) Если на лабораторном столе случайно загорелась тетрадка, то, чтобы потушить пламя, необходимо ограничить доступ воздуха к очагу возгорания, например, накрыв тетрадь плотной тканью (полотенцем или тряпкой). 4) Если нет шпателя (ложечки), твёрдые реактивы можно брать руками.
Ответ: __________________________.
Вариант 2.
Внимательно рассмотрите предложенные рисунки. Укажите номер рисунка, на котором изображён объект, содержащий индивидуальное химическое вещество.

Индивидуальное химическое вещество содержится в объекте, изображённом на рисунке:_______________
1.2. Какие вещества содержатся в объектах, изображённых на остальных рисунках? Приведите по ОДНОМУ примеру.
Для каждого вещества укажите его химическое название и формулу.
Рис. 1: _____________________(название) ______________(формула).
Рис. 2: _____________________(название) ______________(формула).
Рис. 3: _____________________(название) ______________(формула).
И
2.1. Укажите, в ходе какого из приведённых ниже процессов протекает химическая реакция.
1. Движение шара по дорожке при игре в боулинг.
2. Горение бенгальских огней.
3. Таяние мороженого.
Напишите номер выбранного процесса:____________
Объясните сделанный Вами выбор: _______________________________________
2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:__________________________________________________________________________
Из приведённого списка выберите верные суждения о правилах поведения в химической
лаборатории и обращения с химическими веществами в быту. В ответе запишите цифры, под которыми они указаны. (В задании может быть несколько верных суждений.)
1) При работе с раствором пищевой соды необходимо использовать резиновые перчатки.
2) Повышенное содержание в замкнутом пространстве оксида углерода(II) не является
угрожающим фактором для здоровья человека.
3) Хлор в лаборатории получают в вытяжном шкафу.
4) Внесение в почву избыточного количества минеральных удобрений вредит окружающей среде.
Ответ: __________________________.
Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами в быту. В ответе запишите цифры, под
которыми они указаны. (В задании может быть несколько верных суждений.)
1) Легковоспламеняющиеся жидкости следует хранить вдали от нагревательных приборов. 2) Раствор медного купороса, используемый для опрыскивания садовых деревьев, не
следует хранить в оцинкованном ведре. 3) В школьной лаборатории для нагревания пробирок запрещается использовать спиртовки. 4) Кислород в лаборатории необходимо получать в вытяжном шкафу.
Ответ: __________________________
Вариант 3
1.1. Внимательно рассмотрите предложенные рисунки. Укажите номер рисунка, на котором изображён объект, содержащий индивидуальное химическое вещество.

Индивидуальное химическое вещество
содержится в объекте, изображённом на рисунке:_______________
1.2. Какие вещества содержатся в объектах, изображённых на остальных рисунках? Приведите по ОДНОМУ примеру.
Для каждого вещества укажите его химическое название и формулу.
Рис. 1: _____________________(название) ______________(формула).
Рис. 2: _____________________(название) ______________(формула).
Рис. 3: _____________________(название) ______________(формула).
И
2.1. Из представленных ниже рисунков выберите тот, на котором изображено протекание химической реакции.

Протекание химической реакции изображено на рисунке:_________ Объясните сделанный Вами выбор: _________________________ ___________________________________________________
2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:__________________ __________________________________
3. Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами в быту. В ответе запишите цифры, под которыми они указаны. (В задании может быть несколько верных суждений.)
1) Продукты неполного сгорания топлива в автомобильном двигателе отрицательно влияют на состояние окружающей среды.
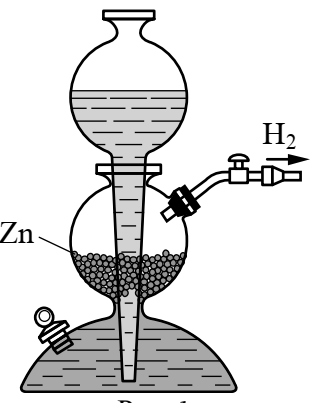
2) Делительная воронка используется в лаборатории для разделения двух несмешивающихся жидкостей.
3) Для перемешивания приготовленного раствора допустимо использовать имеющиеся на столе канцелярские принадлежности (карандаш, ручку, линейку). 4) Загоревшийся бензин тушат водой.
Ответ: __________________________.
4. Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами в быту. В ответе запишите цифры, под которыми они указаны. (В задании может быть несколько верных суждений.)
1) При работе с раствором поваренной соли необходимо использовать защитные очки.
2) Полиэтиленовые пакеты легко разрушаются под действием атмосферных явлений и не представляют угрозы для окружающей среды.
3) Красками, содержащими ионы свинца, не рекомендуется красить детские игрушки и посуду.
4) Получаемый в химической лаборатории газообразный хлор нельзя определять по запаху.
Ответ: __________________________.
Контрольная работа № 2
Вариант 1.
1. (задание из ВПР)


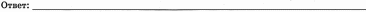
2 (из ГИА)
Из приборов, изображённых на рисунках, выберите тот, с помощью которого можно
получить газообразный водород по реакции .
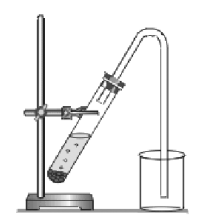
| 
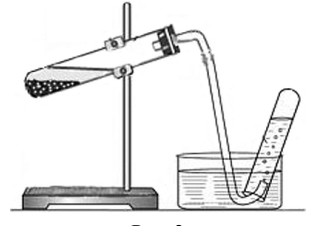
| 
|
| Рис. 1 | Рис. 2 |
Водород можно получить с помощью прибора, изображённого на рисунке:_______
Каким методом – вытеснения воды или вытеснения воздуха – получают водород в этом
приборе?
Ответ: методом вытеснения __________________________.
Почему прибор, изображённый на другом рисунке, не может быть использован для
получения водорода?
Объяснение:_____________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Вариант 2.
(задание из ВПР)
В таблице приведены названия и химические формулы некоторых газообразных веществ.
| № | Название вещества | Формула | Молярная масса,
г/моль |
| Водород | H2 |
|
| Сероводород | H2S |
|
| Сернистый газ | SО2 |
|
Используя предложенные Вам справочные материалы, вычислите молярные массы
каждого из газов и запишите полученные данные в таблицу.
Какой из приведённых в таблице газов имеет при заданных условиях такую же
плотность, как и газ фосфин РH3, молярная масса которого равна 34 г/моль? Укажите номер
вещества. Ответ:________
Объясните свой выбор:_____________________________________________________________
_________________________________________________________________________________
(задание из ВПР)
Превращение одних веществ в другие называется химической реакцией.
Из представленных ниже рисунков выберите тот, на котором изображено протекание
химической реакции.
Протекание химической реакции изображено на рисунке:
Объясните сделанный Вами выбор: _________________________________________________
________________________________________________________________________________
2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:
________________________________________________________________________________
Критерии оценивания.
Задание 1
| Ответ | Кол.баллов |
Записано краткое дано. | 1 |
Записана формула для расчета | 1 |
Есть запись расчетов по алгоритму, ответ | 1 |
| Всего: | 3 |
Задание 2
| Ответ | Кол. баллов |
Указаны методы разделения | 1 |
Указаны номера рисунков | 1 |
| Всего: | 2 |
Шкала оценки образовательных достижений (для всех заданий)
| Процент результативности (баллов) | Оценка уровня подготовки балл (отметка) вербальный аналог |
| 5 | «5»-отлично |
| 4 | «4»- хорошо |
| 3-4 | «3»- удовлетворительно |
| менее 3 | «2»- неудовлетворительно |
Контрольная работа № 3
Вариант 1
(задание из ВПР)
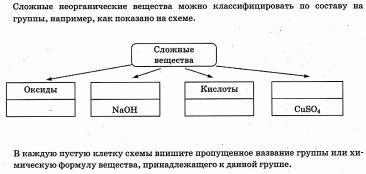
(задание из ВПР)

Вычислите массу 0,25 моль оксида серы(IV).
Решение:______________________________________________________________________
______________________________________________________________________________
Ответ: __________________________
Вариант 2
(задание из ВПР)

(задание из ВПР)

Вычислите массу 0,45 моль железа.
Решение:______________________________________________________________________
_______________________________________________________________________________
Ответ: __________________________
Критерии оценивания.
Задание 1
| Ответ | Кол. баллов |
Записаны названия классов | 1 |
Приведены формулы характерных веществ | 1 |
| Всего: | 2 |
Задание 2
| Ответ | Кол. баллов |
Записаны три правильных ответа | 1 |
Записаны все ответы правильно | 1 |
| Всего: | 2 |
Задание 3
| Ответ | Кол. баллов |
Записано краткое дано. | 1 |
Записано уравнение реакции | 1 |
Есть запись расчетов по алгоритму, ответ | 1 |
| Всего: | 3 |
Шкала оценки образовательных достижений (для всех заданий)
| Процент результативности (баллов) | Оценка уровня подготовки балл (отметка) вербальный аналог |
| 7 | «5»-отлично |
| 5-6 | «4»- хорошо |
| 3-4 | «3»- удовлетворительно |
| менее 3 | «2»- неудовлетворительно |
Контрольная работа № 4
Вариант 1
(задание из ВПР)
В Периодической системе химических элементов Д.И. Менделеева систематизирована информация о химических элементах, их свойствах и свойствах их соединений, о закономерностях изменения этих свойств.
Прочитайте предложение и впишите пропущенные слова: уменьшается, увеличивается, не изменяется.
Слова в ответе могут повторяться.
С увеличением заряда ядра атома химического элемента в периодах Электроотрицательность ___________________, а в группах ___________________.
Учитывая закономерности, сформулированные в составленном выше предложении, расположите в порядке увеличения электроотрицательности химические элементы: иод, хлор, фтор, бром.
Запишите символы указанных химических элементов в нужной последовательности.
Ответ:_________________________________________________________________
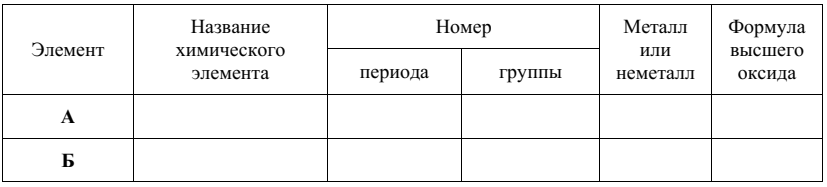
(задание из ВПР)
Даны два химических элемента: А и Б. Известно, что в атоме элемента А содержится
12 протонов, а в атоме элемента Б – 15 электронов.
Используя Периодическую систему химических элементов Д.И. Менделеева, определите
химические элементы А и Б.
Укажите номер периода и номер группы в Периодической системе химических элементов
Д.И. Менделеева, в которых расположен каждый элемент.
Установите, металлом или неметаллом являются простые вещества, образованные этими
химическими элементами.
Составьте формулы высших оксидов, которые образуют элементы А и Б.
Ответы запишите в таблицу.
Контрольная работа № 4
Вариант 2
(задание из ВПР)
В Периодической системе химических элементов Д.И. Менделеева систематизирована информация о химических элементах, их свойствах и свойствах их соединений, о закономерностях изменения этих свойств.
Прочитайте предложение и впишите пропущенные слова: уменьшается, увеличивается, не изменяется.
Слова в ответе могут повторяться.
С увеличением заряда ядра атома химического элемента в периодах радиус атомов _________________________________, а в группах ___________________________.
Учитывая закономерности, сформулированные в составленном выше предложении, расположите в порядке увеличения радиуса химические элементы: алюминий, кремний, магний, натрий.
Запишите символы указанных химических элементов в нужной последовательности.
Ответ:__________________________________________________________________.
(задание из ВПР)
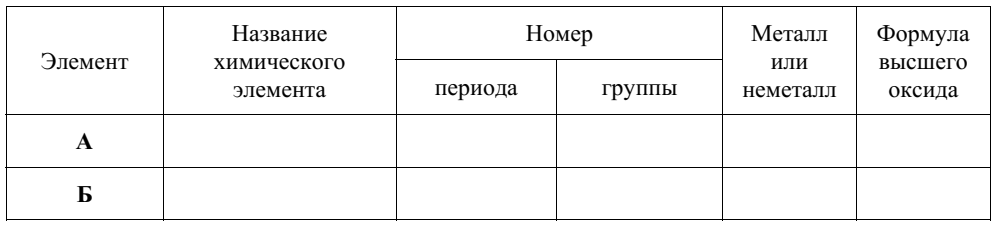
Даны два химических элемента: А и Б. Известно, что в атоме элемента А суммарно
содержится 20 протонов и электронов, а в атоме элемента Б – 13 электронов.
Используя Периодическую систему химических элементов Д.И. Менделеева, определите
химические элементы А и Б.
Укажите номер периода и номер группы в Периодической системе химических элементов
Д.И. Менделеева, в которых расположен каждый элемент.
Установите, металлом или неметаллом являются простые вещества, образованные этими
химическими элементами.
Составьте формулы высших оксидов, которые образуют элементы А и Б.
Ответы запишите в таблицу.
Критерии оценивания.
Задание 1
| Ответ | Кол.баллов |
Верно указаны символ химического элемента | 1 |
Определены период и группа | 1 |
Верно определена формула простого вещества или оксида | 1 |
| Всего: | 3 |
Задание 2
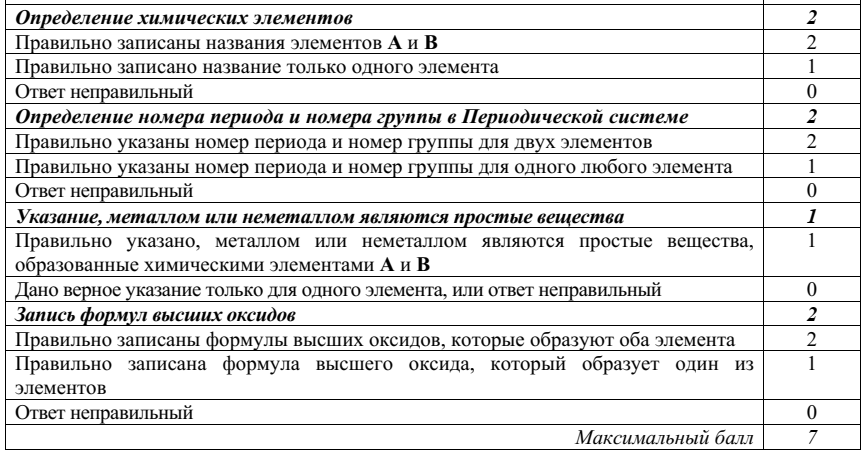
Шкала оценки образовательных достижений (для всех заданий)
| Процент результативности (баллов) | Оценка уровня подготовки балл (отметка) вербальный аналог |
| 10-11 | «5»-отлично |
| 7-9 | «4»- хорошо |
| 5-6 | «3»- удовлетворительно |
| 4 и менее | «2»- неудовлетворительно |
Паспорт
фонда оценочных средств (практические работы)
по химии в 8 классе
| № п/п | Темы | Наименование оценочного средства |
| 1 | Первоначальные химические понятия | Практическая работа № 1. Правила поведения в кабинете химии. Приемы безопасной работы с оборудованием и веществами.
Практическая работа № 2 Очистка загрязненной поваренной соли. |
| 2 | Кислород. Водород. Вода. Растворы | Практическая работа № 3 Получение кислорода и изучение его свойств Практическая работа № 4 Получение водорода и изучение его свойств Практическая работа №5 Приготовление растворов солей с определённой массовой долей растворённого вещества. |
| 3 | Основные классы неорганических соединений | Практическая работа № 6: Решение экспериментальных задач по теме «Основные классы неорганических соединений» |
Практическая работа № 1.
Тема: Правила поведения в кабинете химии. Приемы безопасной работы с оборудованием и веществами.
Цель: ______________________________________________________________________________
_______________________________________________________________________
_______________________________________________________________________
Оборудование. Лабораторный штатив, спиртовка, спички, набор химической посуды.
Внимание! Никогда не приступайте к работе с химическими реактивами без изучения инструкции.
Задание 1. Изучите правила техники безопасности, которые необходимо соблюдать при работе в химической лаборатории.
С правилами техники безопасности ознакомлен __________________
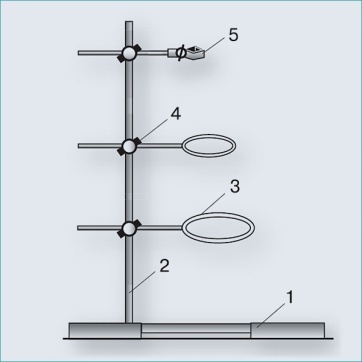
Задание 2. Изучи те устройство лабораторного штатива. Научитесь разбирать и собирать штатив. Подготовьте лабораторный штатив к работе: закрепите в лапке штатива пробирку, разместите на штативе химический стакан и фарфоровую чашку.
| Рисунок | Строение | Назначение прибора |
| 
| 1. |
|
| 2. |
| 3. |
| 4. |
| 5. |
Как правильно закрепляют пробирку в штативе?__________________
____________________________________________________________
Почему, закрепляя пробирку в штативе, нельзя туго закручивать винт лапки?______________________________________________________
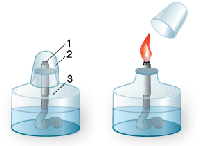
Задание 3. Изучите строение спиртовки и пламени.
| Рисунок | Строение | Назначение прибора |
| 
| 1. |
|
| 2. |
| 3. |
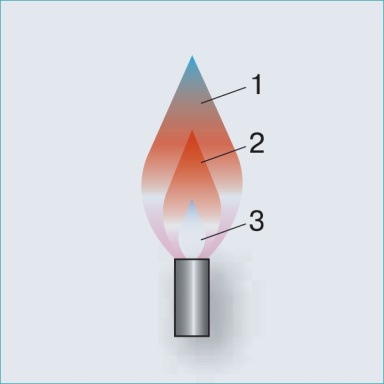
Научитесь работать со спиртовкой, соблюдая правила безопасного обращения с ней. Укажите строение пламени.
| Рисунок | Строение | Как нужно нагревать пробирку. |
| 
| 1.
|
|
| 2.
|
| 3.
|
Вывод: о способах обращения с лабораторным штативом и спиртовкой______________________________________________________________________________________________________________________________________________________________________________________________________
Практическая работа № 2
Тема: Очистка загрязнённой соли от примесей
Цель: _______________________________________________________________________________
________________________________________________________________________________________________________________________________________________
Оборудование и реактивы: загрязнённая поваренная соль, химический стакан с водой, стеклянная палочка, воронка, пробирка, бумажный фильтр, фарфоровая чашка, лабораторный штатив с кольцом, спиртовка, спички.
| 
| С правилами техники безопасности ознакомлен(а) и обязуюсь их выполнять ______________________ подпись
|
РЕКОМЕНДАЦИИ ПО ИЗМЕРЕНИЮ ОБЪЕМА ВОДЫ
| 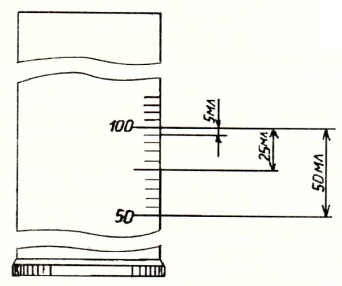 Определение цены деления мерного цилиндра Определение цены деления мерного цилиндра
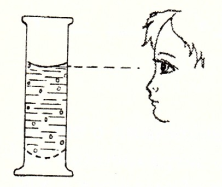 Измерение объема жидкости мерным цилиндром Измерение объема жидкости мерным цилиндром
| Возьмите мерный цилиндр, внимательно рассмотрите шкалу. Установите цену деления (то есть определите, скольким миллилитрам соответствует каждое деление), для этого: — найдите разницу между двумя делениями й (100-50 = 50); — посчитайте число мелких отрезков между ними (10); — разделите разницу между делениями на число мелких отрезков (50 : 10 = 5). В данном случае цена деления — 5 мл. Налейте в мерный цилиндр столько воды, чтобы нижний мениск жидкости достиг нужного деления мерной посуды. При определении уровня мениска глаз наблюдателя должен быть в одной горизонтальной плоскости с соответствующим делением.
|
Ход работы
| Что делаем | Что наблюдаю | Выводы |
| 1.Растворение
загрязнённой поваренной
соли.
В стакан с загрязнённой
поваренной солью
прилейте 50 мл воды.
Осторожно перемешайте
содержимое стеклянной палочкой. | Поваренная соль ______ __________ в воде, песок ________ _______
в воде. Через некоторое время он______________ _________ | Твёрдые и нерастворимые в воде вещества отделяют
от раствора ________________________
______________________
_______________________ |
| 2.Фильтрование
полученного раствора.
Для изготовления фильтра
листок фильтровальной
бумаги сложили на 4 части.
Согнули края так, чтобы
получился конус.
Поместили фильтр в
воронку. Вставили воронку
в пробирку и аккуратно
наливаем мутный раствор
по стеклянной палочке. | Частицы песка
______________ на фильтре, в пробирке собирается
_________________
(фильтрат) | Фильтрованием отделяют
________________ частицы
вещества от жидкости. |
| 3.Выпаривание раствора
соли ( фильтрата).
Полученный фильтрат
вылили в фарфоровую
чашку и поставили её на
кольцо штатива. Нагревали
в пламени спиртовки, до
полного испарения воды.
Полученную соль сравнили
с исходной. | По мере испарения воды на стенках чашки появляется __________________________________________________________________________________________
(вид, цвет, название вещества) | Выпариванием разделяют
___________________
___________________
вещества и растворитель
(воду) |
Вывод:__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Практическая работа № 3
Тема: Получение кислорода и изучение его свойств.
Цель: _______________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
Оборудование и реактивы: раствор перекиси водорода, катализатор, шпатель, 2 пробирки в подставке, зажим для пробирок, спички, древесная лучинка
Т

 Б:
Б:
| 
| С правилами техники безопасности ознакомлен(а) и обязуюсь их выполнять ______________________ подпись
|
Задание 1
1. Приготовьте катализатор, смешайте раствор медного купороса и раствора аммиака. Пролейте в пробирку 2 мл раствора пероксида водорода.
2. Какие изменения происходят с пероксидом водорода?
Что ещё вы наблюдаете? ____________________________________________________________
3. Как доказать, что выделяющийся газ - кислород? _________________ _____________________________________________________________________________________
4. Каким способом можно собрать газообразный кислород?
____________________________________________________________________________________________
| 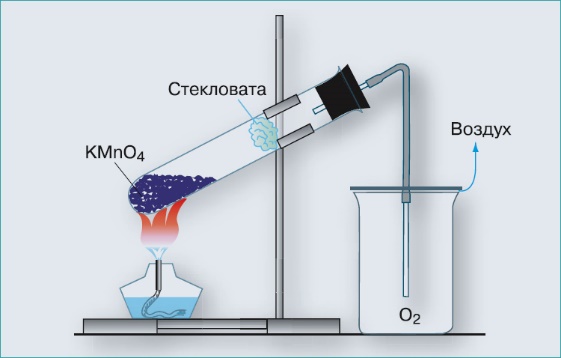
| На рисунке схематическая установка для получения и сбора кислорода. Как он называется? ______________________________
|
| 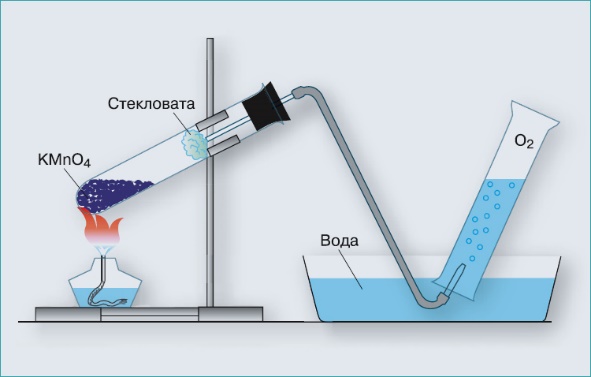
| На рисунке схематическая установка для получения и сбора кислорода. Как он называется? ____________________________ |
5. Запишите уравнения происходящих химических реакций:
t
H2O2→ ___________+___________; С + О2→______________
Задание 2.
1 1. Какую роль играет катализатор в процессе разложения пероксида водорода?____________________________________________________
2.Как работает катализатор? _______________________________ _____________________________________________________________________________________
Вывод:
Кислород собирают двумя способами: ______
1 - _______________________________ пробирка поставлена __________________________________________________________
2 - ______________________________ пробирка поставлена ___________________________________________________________
Кислород распознают _______________________________________
Кислород обладает следующими свойствами: ______________________
_____________________________________________________________
______________________________________________________________
Практическая работа № 4
Тема: Получение водорода и изучение его свойств
Цель: _______________________________________________________________________________
_____________________________________________________________________________________
Оборудование и реактивы: цинк (гранулы), раствор соляной кислоты, пробирка с газоотводной трубкой, сухая пробирка (сборник), спиртовка, спички, лабораторный штатив с лапкой.
ТБ:

С правилами ТБ ознакомлен (а)________________
Ход работы:
Задание: Каким способом можно собрать газообразный кислород?
| 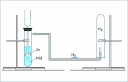
| На рисунке схематическая установка для получения и сбора водорода. Как он называется? _________________________________________ |
| 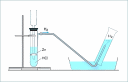
| На рисунке схематическая установка для получения и сбора водорода. Как он называется? ____________________________ |
Соберите прибор
| Что делаем | Что наблюдаем | Уравнения реакций. |
| 1.В пробирку поместите
2-3 кусочка цинка и
прилейте к 3-4 мл
раствора соляной
кислоты. Закройте
пробирку пробкой с
газоотводной трубкой.
Подведите конец трубки
к горлышку пробирки
перевёрнутой вверх
дном. Соберите водород
в пробирку.
2.Заполненную водородом пробирку поднесите к
пламени спиртовки. | _____________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
________________
При поднесении
пробирки с водород
пламени
спиртовки
слышен…
________________ | 1.Составьте уравнение реакции получения водорода:
Zn + HCl →__________ + ___________
К какому типу относится данная
реакция?____________________
___________________________
Почему водород собирают в
перевёрнутую пробирку?
___________________________
__________________________
2.Составьте уравнение реакции горения
водорода:
H2 + O2→____________
К какому типу относится данная
реакция?___________________ |
Вывод: _____________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
Практическая работа №5
Тема: Приготовление растворов солей с определённой массовой долей растворённого вещества.
| Цель: | __________________________________________________________
__________________________________________________________ __________________________________________________________ __________________________________________________________ |
| Оборудование: | химический стакан или колба для раствора с этикеткой, на которой обозначены массовая доля растворенного вещества и масса раствора согласно варианту, мерный цилиндр, стеклянная палочка с резиновым наконечником.
|
| Реактивы: | дистиллированная вода, растворы солей: 8%-й раствор хлорида калия, 6%-й раствор нитрата натрия, 15%-й раствор карбоната натрия и 20% -й раствор хлорида натрия.
|
| Ход работы: | Вычислить объемы данного раствора и воды, необходимые для приготовления раствора с заданными концентрацией и массой в соответствии с вариантом, предложенным учителем.
|
| 
| С правилами техники безопасности ознакомлен(а) и обязуюсь их выполнять |
___________________ подпись |
Задача. Вычисляю объем данного раствора* и объем воды, необходимые для приготовления раствора заданной концентрации.
| Дано: | Решение: |
| m (необх. р-ра) = w (необх. р-ра) = w (данного р-ра) = |
|
|
|
| V (данного р-ра) = ? мл (Н2O) = ? мл | _________________________________________________________
Ответ: ___________________________________________________ |
Отмеряю мерным цилиндром______мл дистиллированной воды, для этого:
—- устанавливаю цену деления;
— наливаю в мерный цилиндр столько воды, чтобы нижний мениск жидкости достиг уровня необходимого деления.
 При установлении уровня мениска мерный цилиндр или мензурку надо разместить на столе так, чтобы глаза наблюдателя находились в одной горизонтальной плоскости с необходимым делением мерной посуды.
При установлении уровня мениска мерный цилиндр или мензурку надо разместить на столе так, чтобы глаза наблюдателя находились в одной горизонтальной плоскости с необходимым делением мерной посуды.
Выливаю дистиллированную воду в подготовленную посуду (стакан или колбу).
Отмеряю мерным цилиндром необходимый (см. ответ задачи) объем данного раствора и выливаю его в посуду с дистиллированной водой. Взбалтываю.
Практическая работа № 6
Тема: Решение экспериментальных задач по теме «Основные классы неорганических соединений»
Цель: ________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
Оборудование: штативы с пробирками, пипетки.
Реактивы: запишите самостоятельно (____________________________________)
Задание: выполните работу согласно заданию предложенному учителем; отчет о работе оформите в виде таблице.
Теоретические вопросы (для всех)
1. Если щелочь попала на тело, то эти участи кожи необходимо промыть холодной водой, а потом 2%-м раствором уксусной кислоты. Затем вновь промыть холодной водой. Как объяснить такую последовательность действий?_________________________________________________
Запишите соответствующие уравнения реакций, используя для примера любую щелочь._________________________________________________________________
2. Приведите химическое название солей:
пищевая сода NаНСО3___________________________________
кальцинированная сода Na2CO3____________________________________
мел, мрамор, известняк СаСО3_____________________________________
поташ К2СО3_______________________________________
калийная селитра КNO3__________________________________
ляпис AgNO3_____________________________
Какие индикаторы используются для определения характера среды
Ход работы
Задача: Определение вещества в пробирках. известно что это __________________
_______________________________________________________________________
Определение веществ
Чтобы определить _______________________, необходимо в пробы исследуемых растворов прилить_____________________________
Чтобы определить _______________________, необходимо в пробы исследуемых растворов прилить_____________________________
Чтобы определить _______________________, необходимо в пробы исследуемых растворов прилить_____________________________
|
| Пробирка №1 | Пробирка №2 | Пробирка №3
|
| Индикатор №1 |
|
|
|
| Индикатор №2 |
|
|
|
Ответ: Пробирка №1___________________
Пробирка №2___________________________
Пробирка №3_________________________
Вывод:
Подведение итогов работы. В ходе практической работы мы научились _________
_______________________________________________________________________
_______________________________________________________________________
Оценка выполнения практических работ
Критерии оценки работы
| № | Вид деятельности | Максимальный
балл |
| 1 | Предварительная подготовка к работе | 1 |
| 2 | Формулировка цели работы | 1 |
| 3 | Сборка прибора и проверка на герметичность | 1 |
| 4 | Пользование нагревательными приборами | ±1 в п. 9 |
| 5 | Соблюдение правил техники безопасности | 1 |
| 6 | Проведение эксперимента в одну стадию | 1 |
| 7 | Умение работать в паре | 1 |
| 8 | Наблюдение и анализ опыта | 1 |
| 9 | Оформление работы (наличие рисунка
установки, вывод) | 1±1 |
| 10 | Поддержка чистоты рабочего места | 1 |
| Количество баллов | Уровень выполнения работы |
| 1-3 | Неудовлетворительный - 2 |
| 3-5 | Удовлетворительный - 3 |
| 6-8 | Оптимальный - 4 |
| 9-10 | Высокий – 5 |














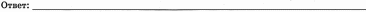












 Определение цены деления мерного цилиндра
Определение цены деления мерного цилиндра Измерение объема жидкости мерным цилиндром
Измерение объема жидкости мерным цилиндром


 Б:
Б: 

























