Просмотр содержимого документа
«Химические свойства солей»


Мотивация
- Что мы знаем о солях?
- Что ещё хотели бы узнать?
- Для чего вам нужны эти знания?

Тема урока: Химические свойства солей
Цели урока:
- изучить основные химические свойства солей на примерах взаимодействия солей с металлами, кислотами, щелочами, солями ;
- определить условия, при которых могут
протекать эти реакции;
- узнать о значении некоторых реакций в повседневной жизни и для дальнейшего изучения химии

Установи соответствие
- Нитрат алюминия - Al(NO 3 ) 3
- Сульфат железа(II) - FeSO 4
- Хлорид натрия - NaCL
- Фосфат калия - K 3 PO 4
- Сульфид железа(II) - FeS
- Гидроксохлорид магния - Mg(OH)CL
- Сульфат бария - BaSO 4

Установи соответствие
- Нитрат алюминия - Al(NO 3 ) 3
- Сульфат железа(II) - FeSO 4
- Хлорид натрия - NaCL
- Фосфат калия - K 3 PO 4
- Сульфид железа(II) - FeS
- Гидроксохлорид магния - Mg(OH)CL

Установи соответствие
- Нитрат алюминия - Al(NO 3 ) 3
- Сульфат железа(II) - FeSO 4
- Хлорид натрия - NaCL
- Фосфат калия - K 3 PO 4
- Сульфид железа(II) - FeS
- Гидроксохлорид магния - Mg(OH)CL
Третий лишний
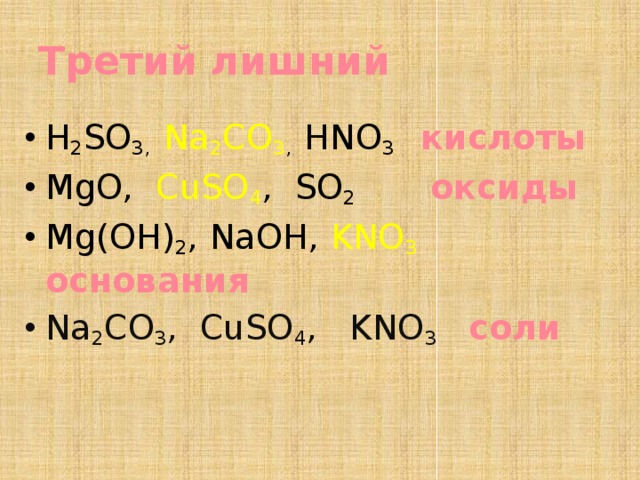
Третий лишний
- H 2 SO 3, Na 2 CO 3 , HNO 3 кислоты
- MgO, CuSO 4 , SO 2 оксиды
- Mg(OH) 2 , NaOH, KNO 3 основания
- Na 2 CO 3 , CuSO 4 , KNO 3 соли

Самооценивание 1 по плану
- Я знаю состав солей, их классификацию, могу находить соли среди других соединений.
- Я умею составлять формулы солей по валентности и давать названия по формулам.
- Я знаю физические свойства и применение солей, умею пользоваться таблицей растворимости.
- Выставь себе оценку: + + + = 5

Методы:
- Химический эксперимент ( Соблюдаем ТБ)
- Сравнение

1. Взаимодествие солей с металлами

1. Взаимодествие солей с металлами
- CuSO 4 + Fe = FeSO 4 + Cu
- Соль 1 + Металл 1 = Соль 2 + Металл 2
- Условие:
- Более активный металл вытесняет менее активный из раствора его соли
Fe, Cu
Активные металлы (Li,Na,K,Ca,Ba) не применяют для таких опытов, т.к. они будут реагировать с водой.

Применение
- Можно ли использовать оцинкованные ведра для хранения раствора медного купороса ?

Почему разрушаются памятники архитектуры?

2. Взаимодействие солей с кислотами

2. Взаимодействие солей с кислотами
Na 2 CO 3 + H 2 SO 4 =

2. Взаимодействие солей с кислотами
- Соль1 + Кислота 1 = Соль 2 + Кислота 2
Условие:
или
2. Выпадение осадка

Применение
- На каких химических свойствах основано применение питьевой соды?
- При ожогах кислотой рекомендуется промыть поражённое место водой, а затем наложить примочку с раствором питьевой соды. Почему?

Применение

Применение

3. Взаимодействие солей с щелочами
CuSO 4 + NaOH =

3. Взаимодействие солей с щелочами
- Соль1 + Щёлочь = Соль 2 + Основание
Условие:
или
2. Выделение газа

4. Взаимодействие солей с солями

4. Взаимодействие солей с солями

4. Взаимодействие солей с солями
- Соль 1 + Соль 2 = Соль 3 + Соль 4
- Условие:
Применение

Самооценивание 2 по плану
- Я могу проводить эксперимент и по признаку реакции делать выводы
- Я умею составлять уравнения реакций солей с металлами, кислотами, щелочами, солями.
- Я знаю значение некоторых реакций в повседневной жизни.

Закрепление
1. Соль 1 + Металл 1 = Соль 2 + Металл 2
2. Соль 1 + Кислота 1 = Соль 2 + Кислота 2
3. Соль1 + Щёлочь = Соль 2 + Основание
4. Соль 1 + Соль 2 = Соль 3 + Соль 4
Условия реакций:
Исключи лишнее:

Закрепление
- Соль 1 + Металл 1 = Соль 2 + Металл 2
2. Соль 1 + Кислота 1 = Соль 2 + Кислота 2
3. Соль1 + Щёлочь = Соль 2 + Основание
4. Соль 1 + Соль 2 = Соль 3 + Соль 4
Исключи лишнее: 1 – реакция замещения
2, 3, 4, - реакции обмена

Выводы

Самооценивание 3 по плану
- Я знаю с какими веществами будут реагировать соли и могу прогнозировать продукты реакции.
- Я знаю условия протекания этих химических реакций.
- Я могу определять типы химических реакций

Домашнее задание
- § 47, упр. 5 письменно – всем
- Упр. 2 письменно – на «4» и «5»




























































