Электрический ток в различных средах

ВОПРОСЫ:
- Электролитическая диссоциация
- Электрический ток в электролитах. Электролиз
- Законы электролиза
- Применение электролиза

Вопрос 1
Электролитическая диссоциация

Электролитическая диссоциация
По электрическим свойствам все жидкости можно разделить на 2 группы:
ЖИДКОСТИ
ПРОВОДЯЩИЕ
НЕПРОВОДЯЩИЕ
Не содержащие свободные заряженные частицы (недиссоциирующие)
Содержащие свободные заряженные частицы (диссоциирующие) - электролиты
К ним относятся дистилированная вода, спирт, минеральное масло…
К ним относятся растворы (чаще всего водные) и расплавы солей, кислот и оснований
Распад нейтральных молекул вещества в растворителе на положительные и отрицательные ионы под действием электрического поля полярных молекул воды называется Э лектролитической диссоциацией


Электролитическая диссоциация
Электролитическая диссоциация поваренной соли
Na Cl
NaCl Na + + Cl -
Диссоциация других веществ:
CuSO 4 Cu 2+ + SO 4 2-
HCl H + + Cl -
H 2 SO 4 H + + H + + SO 4 2-
Cl -
Na +
CaCl 2 Ca 2+ + Cl - + Cl -
При диссоциации ионы металлов и водорода всегда заряжены положительно , а ионы кислотных радикалов и группы ОН - отрицательно

Вопрос 2
Электрический ток в электролитах. Электролиз

Электролиз
Ионы в электролите движутся хаотично, но при создании электрического поля характер движения становится упорядоченным: положительные ионы (катионы) движутся к катоду, отрицательные ионы (анионы) движутся к аноду
- (катод)
+ (анод)
+
-
Электрический ток в электролитах представляет собой упорядоченное движение положительных и отрицательных ионов
+
-
-
+
+
-

Электролиз
Рассмотрим, что происходит, когда ионы достигают электродов (на примере медного купороса)
CuSO 4 Cu 2+ + SO 4 2-
На катоде:
Положительные ионы меди, подходя к катоду, получают два недостающих электрона, восстанавливаясь до металлической меди
- (катод)
Cu 2+ + 2 е Cu 0
+
В процессе протекания тока через электролит на катоде происходит оседание слоя чистой меди – электролиз раствора медного купороса
Cu 2+
+
Cu 2+
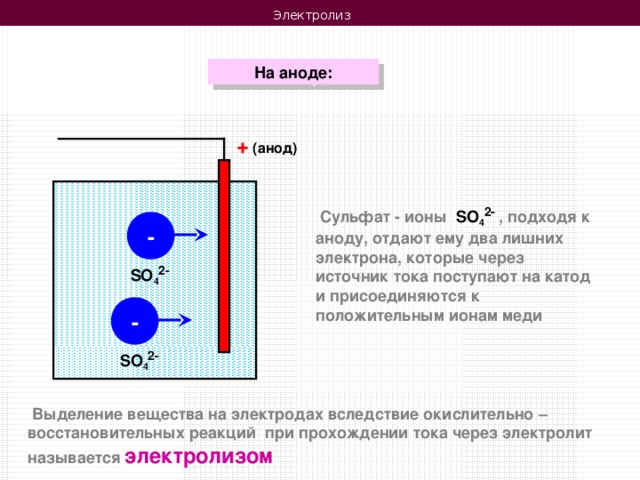
Электролиз
На аноде:
+ (анод)
Сульфат - ионы SO 4 2- , подходя к аноду, отдают ему два лишних электрона, которые через источник тока поступают на катод и присоединяются к положительным ионам меди
-
SO 4 2-
-
SO 4 2-
Выделение вещества на электродах вследствие окислительно – восстановительных реакций при прохождении тока через электролит называется электролизом

Вопрос 3
Законы электролиза

Законы электролиза
Исследовал электролиз и открыл его законы английский физик Майкл Фарадей в 1834 году
Первый закон электролиза
Масса вещества, выделившегося на электродах при электролизе, прямо пропорциональна величине заряда, прошедшего через электролит
k – электрохимический эквивалент вещества
(равен массе вещества, выделившегося при прохождении через электролит заряда 1 Кл)
Майкл Фарадей (1791 – 1867) Открыл явление электромагнитной индукции, законы электролиза, ввел представления об электрическом и магнитном поле
Если учесть, что q = I t , то

Законы электролиза
Второй закон электролиза
При одинаковом количестве электричества (электрическом заряде, прошедшем через электролит) масса вещества, выделившегося при электролизе, пропорциональна отношению молярной массы вещества к валентности
M – масса выделившегося вещества k – электрохимический эквивалент М – молярная масса вещества n – валентность вещества
Заряд, необходимый для выделения 1 моля вещества, одинаков для всех электролитов. Он называется числом Фарадея F
Электрохимический эквивалент и число Фарадея связаны соотношением
Как отсюда экспериментально определить заряд электрона?

Физический смысл электрохимического эквивалента
Отношение массы иона к заряду иона
Как экспериментально определить заряд электрона?

Заряд электрона
1874 г

Зависимость сопротивления электролита от температуры
Температурная зависимость сопротивления электролита объясняется в основном изменением удельного сопротивления. , где альфа - температурный коэффициент сопротивления.
Для электролитов всегда поэтому Сопротивление электролита можно рассчитать по формуле:

Вопрос 4
Применение электролиза

Применение электролиза
ПРИМЕНЕНИЕ ЭЛЕКТРОЛИЗА
Получение химически чистых веществ
Гальваностегия
Гальванопластика

Применение электролиза
Основателем гальванотехники и ее широчайшего применения является Б. С. Якоби , который изобрел в 1836 году гальванопластику
Гальванотехника - это отрасль прикладной электрохимии, смысл которой состоит в получении электролитическим путем металлических копий каких-либо предметов (гальванопластика) или же в нанесении этим же способом металлических покрытий на какие-либо поверхности (гальваностегия). Способ этот в свое время широко использовался в полиграфической промышленности и в определенных случаях применяется и сейчас
Борис Семенович Якоби (1801 – 1874) – русский академик, открывший гальванопластику, создавший первую конструкцию электродвигателя

Применение электролиза
1. Получение химически чистых веществ
Катод – тонкая пластина чистой меди, анод – толстая пластина неочищенной меди
Рафинирование меди
- катод
+ анод
CuSO4
При прохождении тока через электролит на катоде оседает чистая медь, анод расходуется и истощается
Примеси остаются в электролите или оседают на дно
При плотности тока 0,3 А на 1 дм 2 процесс идет несколько дней

Применение электролиза
1. Получение химически чистых веществ
Получение алюминия
Алюминий получают электролитическим способом из глинозема (вспомните – алюминий является одним из самых распространенных химических элементов земной коры и содержится в любой глине)
Осуществив, например, электролиз раствора поваренной соли NaCl , мы можем получить сразу 3 полезных химических вещества:
Газообразные водород и хлор, а также раствор едкого натра NaOH

Применение электролиза
2. Гальваностегия
Гальваностегия – покрытие предметов неокисляющимся металлами для защиты от коррозии
( Ni, Zn, Ag, Au, Cu)
Приведите примеры защитных покрытий в быту и технике

Применение электролиза
3. Гальванопластика
Гальванопластика – получение отслаиваемых копий предмета, полученных путем осаждения металла на поверхности предмета электролитическим способом
Применение:
- Получение рельефных копий барельефов, статуй
- Изготовление клише, полиграфия
- выпуск ценных бумаг, денег

Применение электролиза
Кроме указанных выше, электролиз нашел применение и в других областях: получение оксидных защитных пленок на металлах (анодирование); электрохимическая обработка поверхности металлического изделия (полировка); электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др.); очистка воды - удаление из нее растворимых примесей. В результате получается так называемая мягкая вода (по своим свойствам приближающаяся к дистиллированной); электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т.д.).