Просмотр содержимого документа
«Презентация урока по физике на тему: "Электрический ток в жидкостях"»

«Очень важно не перестать задавать вопросы. Любопытство не случайно дано человеку» (Эйнштейн)
![Проверка Название Буквенное обозначение Время Единица измерения t Электрический заряд Сила тока Основная формула мин / сек q I Напряжение [ Кл ] – Определение q = I*t U [ А ] ––– Сопротивление I = q / t [ В ] ––– Работа электрического тока R U=A/q ––– Мощность A [ Ом ] ––– R=U/I [ Дж ] P A=I*U*t [ Вт ] ––– ––– P=A/t P=I*U –––](https://fsd.multiurok.ru/html/2017/03/02/s_58b801bbddf73/img1.jpg)
Проверка
Название
Буквенное обозначение
Время
Единица измерения
t
Электрический заряд
Сила тока
Основная формула
мин / сек
q
I
Напряжение
[ Кл ]
–
Определение
q = I*t
U
[ А ]
–––
Сопротивление
I = q / t
[ В ]
–––
Работа электрического тока
R
U=A/q
–––
Мощность
A
[ Ом ]
–––
R=U/I
[ Дж ]
P
A=I*U*t
[ Вт ]
–––
–––
P=A/t
P=I*U
–––

24. 02. 2017 г Электрический ток в жидкостях. Законы электролиза

Изучить
Узнать
Усвоить
Повторить
Оценить
Обобщить
Организовать
Продемонстрировать
...
- электролитическая диссоциация;
- рекомбинация;
- электролиз.
2. Явления:
3. Законы:
- закон электролиза Фарадея.


Из жидкостей электрический ток проводят только электролиты – растворы солей, кислот и щелочей.

Жидкий проводник, в котором подвижными носителями зарядов являются только ионы, называют электролитом.
молекула
+ —
CuSO 4
—
+
ионы
Cu 2+
SO 4 2-
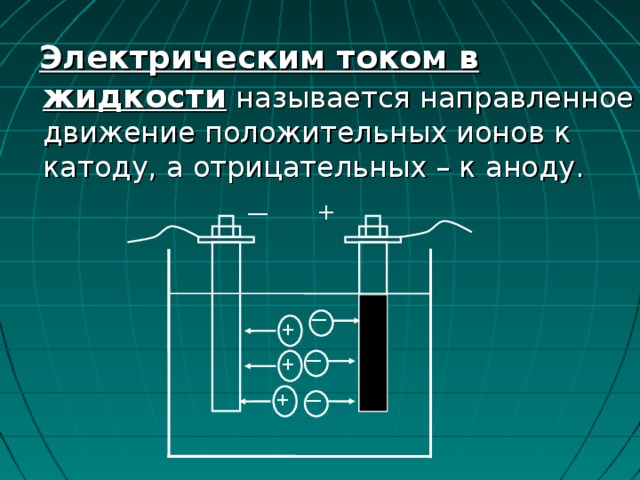
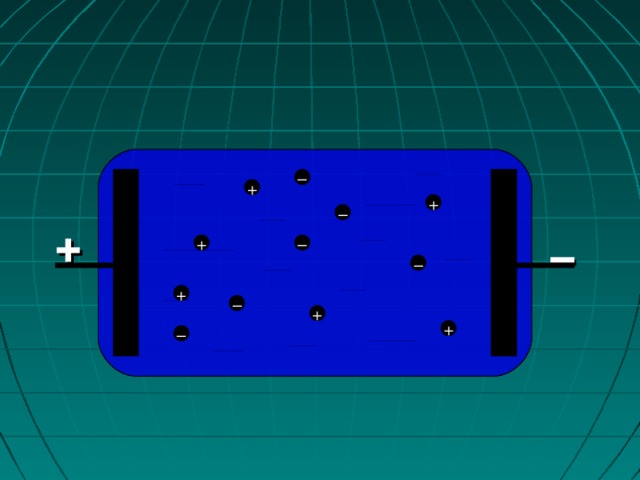
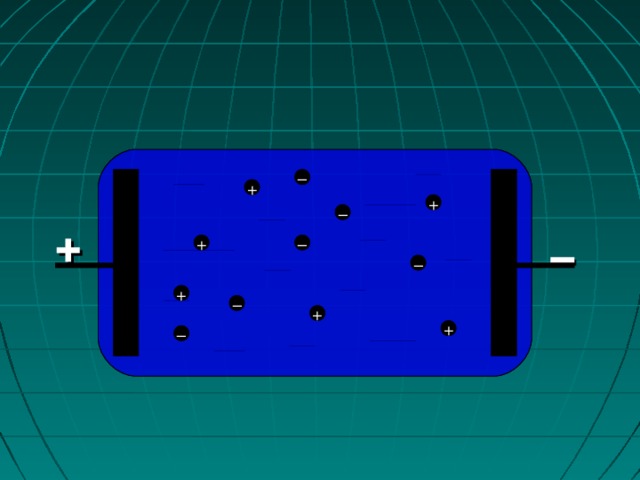
Электрическим током в жидкости называется направленное движение положительных ионов к катоду, а отрицательных – к аноду.
+
—
—
+
—
+
—
+
−
+
+
−
+
−
−
+
−
+
−
+
+
−
−
+
+
−
+
−
−
+
−
+
−
+
+
−

Электролиз это совокупность процессов, протекающих в растворе или расплаве электролита, выделение на катоде вещества, входящего в состав электролита, при пропускании электрического тока.

Закон электролиза
Первый закон Фарадея :
масса вещества ( m ), выделившегося на катоде, прямо пропорциональна заряду ( q ), прошедшему через электролит
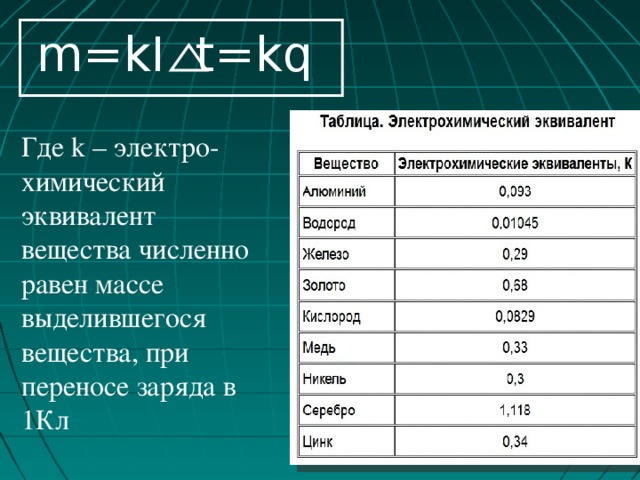
m=kI t=kq
Где k – электро-
химический эквивалент вещества численно равен массе выделившегося вещества, при переносе заряда в 1Кл

Физ.минутка

Гальваностегия – декоративное или антикоррозийное покрытие металлических изделий тонким слоем другого металла (никелирование, хромирование, омеднение, золочение, серебрение)
Гальванопластика – электролитическое изготовление металлических копий, рельефных предметов

Электрометаллургия – получение чистых металлов ( Al , Na , Mg , Be ) при электролизе расплавленных руд
Рафинирование металлов – очистка металлов от примесей с помощью электролиза, когда неочищенный металл является анодом, а на катоде оседает очищенный.

Решение задач
- Задача: При никелировании детали в течении 50 минут сила тока, проходящего через ванну, была равна 2 А. Какова масса, выделившегося вещества на детали, если электрохимический эквивалент никеля k = 3 · 10 в степени – 7 кг/Кл?

Задача 2: В течении 15 минут сила тока, проходящего через ванну, была равна 0,7 А. Какова масса, выделившегося вещества на детали, если электрохимический эквивалент k = 2,077 · 10 в степени – 7 кг/Кл?
Задача 3: Сила тока 120А, как найти массу, выделившегося вещества, за 40 мин, если электрохимический эквивалент k = 1,26 · 10
в степени – 7 кг/Кл?

§49;
упр. 23
(4п,5п,6п)

СПАСИБО ЗА ВНИМАНИЕ







![Проверка Название Буквенное обозначение Время Единица измерения t Электрический заряд Сила тока Основная формула мин / сек q I Напряжение [ Кл ] – Определение q = I*t U [ А ] ––– Сопротивление I = q / t [ В ] ––– Работа электрического тока R U=A/q ––– Мощность A [ Ом ] ––– R=U/I [ Дж ] P A=I*U*t [ Вт ] ––– ––– P=A/t P=I*U –––](https://fsd.multiurok.ru/html/2017/03/02/s_58b801bbddf73/img1.jpg)



































