
Вещества молекулярного и немолекулярного строения
11 класс

ПОНЯТИЯ

ПОНЯТИЯ
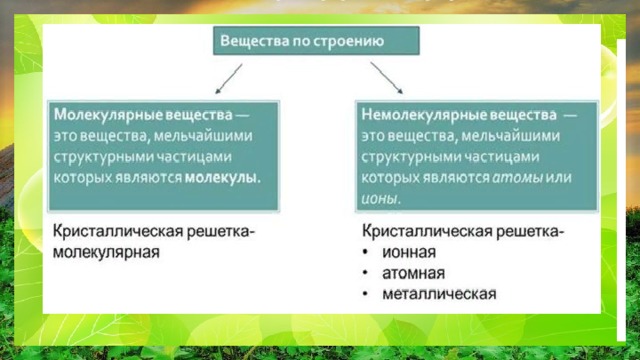

МОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА
Вещества, состоящие из молекул, называются молекулярными веществами. Связи между молекулами в таких веществах очень слабые, намного слабее, чем между атомами внутри молекулы, и уже при сравнительно низких температурах они разрываются — вещество превращается в жидкость и далее в газ (возгонка йода). Температуры плавления и кипения веществ, состоящих из молекул, повышаются с увеличением молекулярной массы. К молекулярным веществам относятся вещества с атомной структурой (C, Si, Li, Na, K, Cu, Fe, W, O 2 , S 8 , P 4 , H 2 , N 2 , Cl 2 , F 2 , Br 2 , I 2 ), среди них есть металлы и неметаллы, соединения неметаллов друг с другом (бинарные и многоэлементные): NH3, CO2, H2SO4.

НЕМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА
К веществам немолекулярного строения относятся ионные соединения . Таким строением обладает большинство соединений металлов с неметаллами: все соли (NaCl, K2SO4, Na2SO4, CuCl2), некоторые гидриды (LiH, NaH) и оксиды (CaO, MgO, FeO, Fe2O3), основания (NaOH, KOH). простые вещества (металлы): Na, Cu, Fe, …;сплавы; неметаллы: бор, кремний, углерод (алмаз), фосфор (чёрный и красный); некоторые бинарные соединения неметаллов: SiC, SiO2.
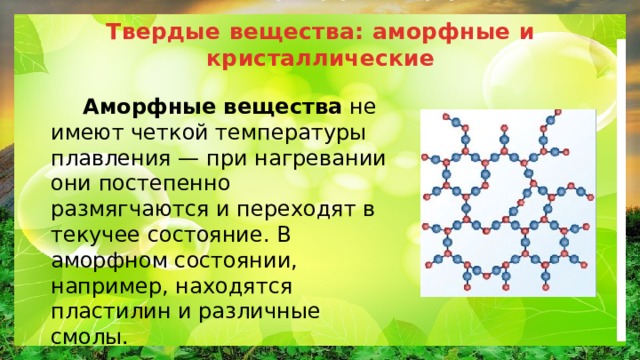
Твердые вещества: аморфные и кристаллические
Аморфные вещества не имеют четкой температуры плавления — при нагревании они постепенно размягчаются и переходят в текучее состояние. В аморфном состоянии, например, находятся пластилин и различные смолы.

Твердые вещества: аморфные и кристаллические
Кристаллические вещества характеризуются правильным расположением тех частиц, из которых они состоят: атомов, молекул и ионов — в строго определенных точках пространства. При соединении этих точек прямыми линиями образуется пространственный каркас, называемый кристаллической решеткой. Точки, в которых размещены частицы кристалла, называют узлами решетки. В зависимости от типа частиц, расположенных в узлах кристаллической решетки, и характера связи между ними, различают четыре типа кристаллических решеток: ионные, атомные, молекулярные и металлические.

Атомные кристаллические решетки
Атомными называют кристаллические решетки, в узлах которых находятся отдельные атомы . В таких решетках атомы соединены между собой очень прочными ковалентными связями. Примером веществ с таким типом кристаллических решеток может служить алмаз — одно из аллотропных видоизменений углерода . Большинство веществ с атомной кристаллической решеткой имеют очень высокие температуры плавления (например, у алмаза она свыше 3500 °С), они прочны и тверды, практически нерастворимы.

Молекулярные кристаллические решетки
Молекулярными называют кристаллические решетки, в узлах которых располагаются молекулы. Химические связи в этих молекулах могут быть и полярными (HCl, H2O), и неполярными (N2, O2). Несмотря на то, что атомы внутри молекул связаны очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому вещества с молекулярными кристаллическими решетками имеют малую твердость, низкие температуры плавления, летучи. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар).


Водородная связь
В молекулах соединениях HF, H2O, NH3 существуют связи водорода с сильно электроотрицательным элементом (Н–F, Н–O, Н–N). Между молекулами таких соединений могут образовываться межмолекулярные водородные связи. В некоторых органических молекулах, содержащих связи Н–O, Н–N, могут возникать внутримолекулярные водородные связи.



































