«Скорость химических реакций. Факторы, влияющие на скорость химической реакции»
Скорость химических реакций -
Это изменение концентрации одного из реагирующих или одного из продуктов реакции в единицу времени.
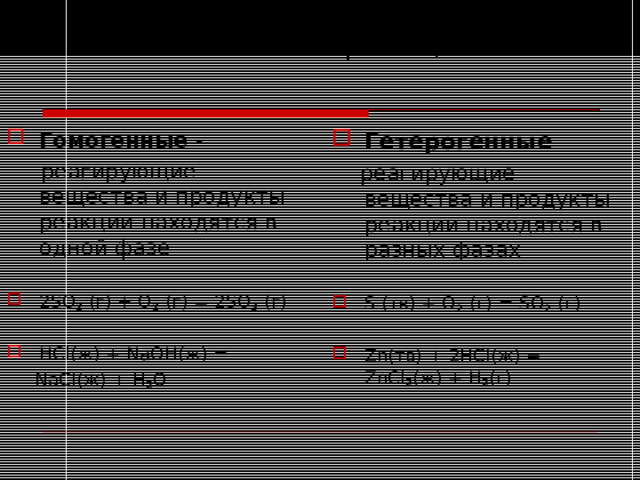
Химические реакции
реагирующие вещества и продукты реакции находятся в одной фазе
реагирующие вещества и продукты реакции находятся в разных фазах
- 2SO 2 (г) + O 2 (г) = 2SO 3 (г)
- HCl(ж) + NaOH(ж) =
- S (тв) + O 2 (г) = SO 2 (г)
- Zn(тв) + 2HCl(ж) = ZnCl 2 (ж) + H 2 (г)
NaCl(ж) + H 2 O
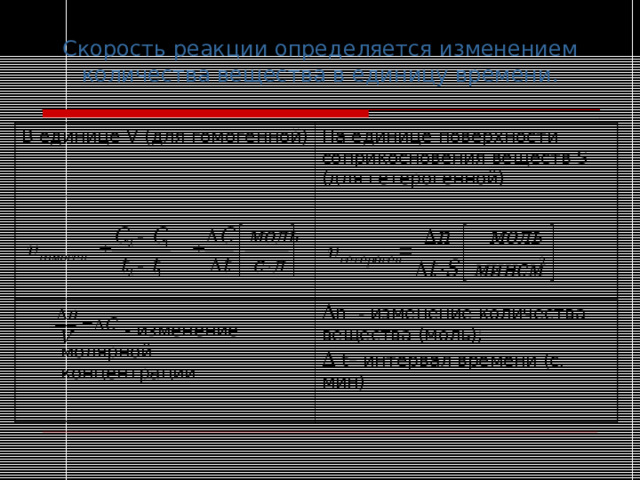
Скорость реакции определяется изменением количества вещества в единицу времени.
В единице V (для гомогенной)
На единице поверхности соприкосновения веществ S (для гетерогенной)
n - изменение количества вещества (моль);
t – интервал времени (с, мин)
- изменение молярной концентрации
Задача на применение знаний по «Скорости химических реакций»
- Химическая реакция протекает в растворе, согласно уравнению: А+В = С. Исходные концентрации: вещества А – 0,80 моль/л, вещества В – 1,00 моль/л. Через 20 минут концентрация вещества А снизилась до 0, 74 моль/л. Определите: а) среднюю скорость реакции за этот промежуток времени;
б) концентрацию вещества В через 20 мин.
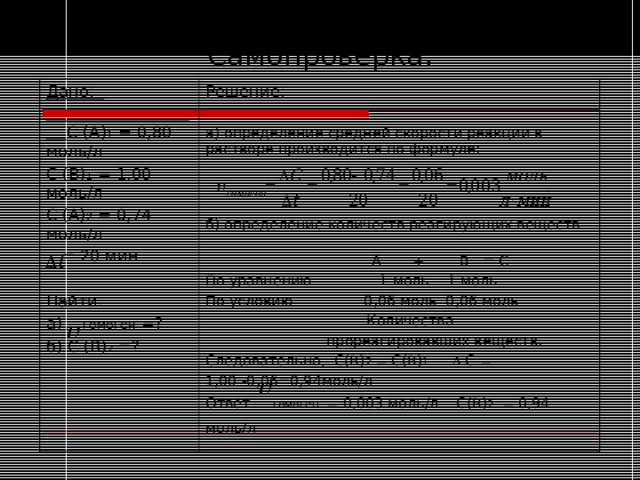
Самопроверка.
Дано:
С (А) 1 = 0,80 моль/л
С (В) 1 = 1,00 моль/л
С (А) 2 = 0,74 моль/л
= 20 мин
Найти.
а) гомоген =?
б) С (В) 2 =?
Решение:
а) определение средней скорости реакции в растворе производится по формуле:
б) определение количеств реагирующих веществ:
А + В = С
По уравнению 1 моль 1 моль
По условию 0,06 моль 0,06 моль
Количества
прореагировавших веществ.
Следовательно, С(В) 2 = С(В) 1 - С =
1,00 -0,06=0,94моль/л
Ответ: гомоген. = 0,003 моль/л С(В) 2 = 0,94 моль/л
Задача на применение знаний по «Скорости химических реакций»
- В некоторый момент времени концентрация хлора Cl 2 в сосуде, в котором протекала реакция
Н 2 + Cl 2 = 2 HCl , была равна 0,06 моль/л. Через 5 сек концентрация хлора составила 0,02 моль/л. Чему равна средняя скорость данной реакции в указанный промежуток времени.
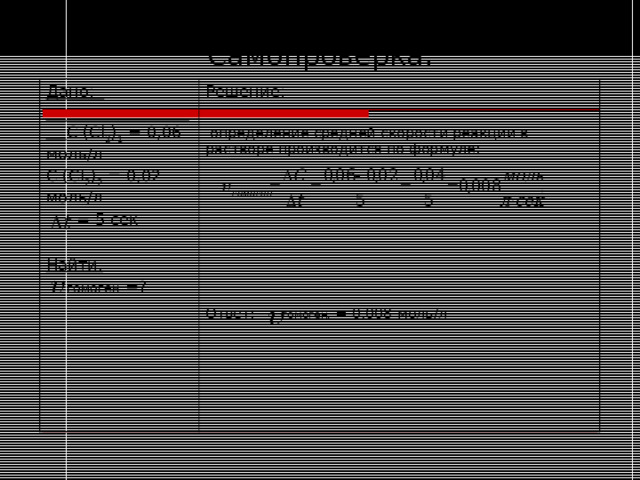
Самопроверка.
Дано:
С ( Cl 2 ) 1 = 0, 06 моль/л
С ( Cl 2 ) 2 = 0, 0 2 моль/л
= 5 сек
Найти.
гомоген =?
Решение:
определение средней скорости реакции в растворе производится по формуле:
Ответ: гомоген. = 0,008 моль/л
Факторы, влияющие на скорость химической реакции
- природа реагирующих веществ;
- температура;
- концентрация реагирующих веществ;
- действие катализаторов;
- поверхность соприкосновения реагирующих веществ (в гетерогенных реакциях).

Теория столкновений. Основная идея её такова: реакции происходят при столкновении частиц реагентов, которые обладают определённой энергией.
Выводы:
- Чем больше частиц реагентов, чем ближе они друг к другу, тем больше шансов у них столкнуться и прореагировать.
- К реакции приводят лишь эффективные соударения , т.е. такие при которых разрушаются или ослабляются «старые связи» и поэтому могут образоваться «новые». Но для этого частицы должны обладать достаточной энергией.
Минимальный избыток энергии (над средней энергией частиц в системе), необходимый для эффективного соударения частиц в системе), необходимый для эффективного соударения частиц реагентов, называется энергией активации Е а.
1. Природа реагирующих веществ.
- Под природой реагирующих веществ понимают их состав, строение, взаимное влияние атомов в неорганических и органических веществах.
- Величина энергии активации веществ – это фактор, посредством которого сказывается влияние природы реагирующих веществ на скорость реакции.
Задание на применение знаний
- Объясните разную скорость взаимодействия цинка и магния с уксусной кислотой; цинка с соляной и уксусной кислотой.
- Напишите соответствующие реакции.

2. Температура
- При увеличении температуры на каждые 10 ° С общее число столкновений увеличивается только на ~ 1,6 %, а скорость реакции увеличивается в 2-4 раза (на 100-300%).
- Число, показывающее, во сколько раз увеличивается скорость реакции при повышении температуры на 10 ° С, называют температурным коэффициентом.
- Правило Вант-Гоффа математически выражается следующей формулой:
где –скорость реакции при температуре t 2 ,
– скорость реакции при температуре t 1 ,
– температурный коэффициент.
Задача на применение знаний:
- Определите, как изменится скорость некоторой реакции:
а) при повышении температуры от 10 ° до 50 ° С;
б) при понижении температуры от 10 ° – 0 ° С.
Температурный коэффициент реакции равен 3.

Самопроверка
а) подставить данные задачи в формулу:
скорость реакции увеличится в 81 раз.
б)
Скорость реакции уменьшится в 3 раза.

3. Концентрации реагирующих веществ.
- На основе большого экспериментального материала в 1867 г. норвежские учёные К. Гульдберг, и П Вааге и независимо от них в 1865 г. русский учёный Н.И. Бекетов сформулировали основной закон химической кинетики, устанавливающий зависимость скорости реакции от концентраций реагирующих веществ:
скорость химической реакции пропорциональна произведению концентраций реагирующих веществ, взятых в степенях равных их коэффициентам в уравнении реакции.
Этот закон ещё называют
законом действующих масс.

Математическое выражение закона действующих масс.
- По закону действующих масс скорость реакции, уравнение которой А+В=С может быть вычислена по формуле:
v = k·C A · C B ,
а скорость реакции, уравнение которой А+2В= D , может быть вычислена по формуле:
v = k·C A · C B 2 .
В этих формулах: C A и C B – концентрации веществ А и В (моль/л), k – коэффициенты пропорциональности, называемые константами скоростей реакции . Эти формулы также называют кинетическими уравнениями.
Задача на применение знаний:
- Составьте кинетические уравнения для следующих реакций:
А) H 2 + I 2 =2 HI
Б) S + O 2 = SO 2
В) 2 SO 2 + O 2 =2 SO 3
Б) 2 Fe + 3 CI 2 = 2 FeCI 3
Задача на применение знаний:
- Как изменится скорость реакции, имеющей кинетическое уравнение
v = kCA 2 CB , если:
а) концентрацию вещества А увеличить в 3 раза
б) концентрацию веществ А и В увеличить в 2 раза

Самопроверка.
- Решение. Подставим соответствующие данные в кинетическое уравнение, сравним скорости реакций.
скорость реакции увеличится в 9 раз.
4. Действие катализатора
Обсуждение вопросов:
- 1.Что такое катализатор и каталитические реакции?
- 2. Приведите примеры известных вам каталитических реакций из органической и неорганической химии. Укажите названия веществ – катализаторов.
- 3. Выскажите предположение о механизме действия катализаторов (на основе теории столкновений).
- 4. Каково значение каталитических реакций?

5.Поверхность соприкосновения реагирующих веществ.
- Скорость реакции увеличивается благодаря:
-увеличению площади поверхности соприкосновения реагентов (измельчение);
-повышению реакционной способности частиц на поверхности образующихся при измельчении микрокристаллов;
-непрерывному подводу реагентов и хорошему отводу продуктов с поверхности, где идёт реакция.
- Фактор связан с гетерогенными реакциями, которые протекают на поверхности соприкосновения реагирующих веществ: газ - твердое вещество, газ - жидкость, жидкость - твердое вещество, жидкость - другая жидкость, твердое вещество - другое твердое вещество, при условии, что они не растворимы друг в друге.
- Приведите примеры гетерогенных реакций.

Домашнее задание
п. 15, упр. 11, с. 136