Тема. Внутренняя энергия.
Цели урока:
Дать понятия физической величины – внутренняя энергия и способов изменения внутренней энергии.
Проверить и развить умения переводить физические величины в СИ, ,решать задачи, используя изученные формулы
Развивать у обучающихсяся умения решать задачи.
Ход урока
I. Организационный момент
II. Опрос устный:
Вопросы
Каковы свойства молекул идеального газа?
Что называется постоянной Больцмана, и в каких единицах она измеряется?
От чего зависит средняя кинетическая энергия молекул идеального газа?
Как изменяется температура тела, если оно отдаёт энергии больше, чем получает извне?
Сколько направлений движения атома, возможно?
III. Изучение нового материала
Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема (закон Джоуля). Молекулярно-кинетическая теория приводит к следующему выражению для внутренней энергии одного моля идеального одноатомного газа (гелий, неон и др.), молекулы которого совершают только поступательное движение:
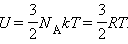
Внутренняя энергия идеального одноатомного газа равна сумме энергий хаотического движения молекул. Тогда имеем:U=NEср Так как Еср=3/2kT и N=vNa. То имеем U= 3/2 vNakT, но v=m/M, тогда получим:
U=3/2*m/M* Na kT ,
где Na – постоянная Авагадро. Na =6.02*1023моль-1.
Учитывая уравнение состояния газа получим: U=3/2*pV
Поскольку потенциальная энергия взаимодействия молекул зависит от расстояния между ними, в общем случае внутренняя энергия U тела зависит наряду с температурой T также и от объема V:
U = U(T,V).
Таким образом, внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела. Она не зависит от того, каким путем получено и изменяется данное состояние. Принято говорить, что внутренняя энергия является функцией состояния. Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу
Внутренняя энергия тела может изменяться не только в результате совершаемой работы, но и вследствие теплообмена. При тепловом контакте тел внутренняя энергия одного из них может увеличиваться, а внутренняя энергия другого – уменьшаться. В этом случае говорят о тепловом потоке от одного тела к другому. Количеством теплоты Q, полученной телом, называют изменение внутренней энергии тела в результате теплообмена.

IV. Физкультминутка.
V. Закрепление изученного. Решение задач.
Задача 1.
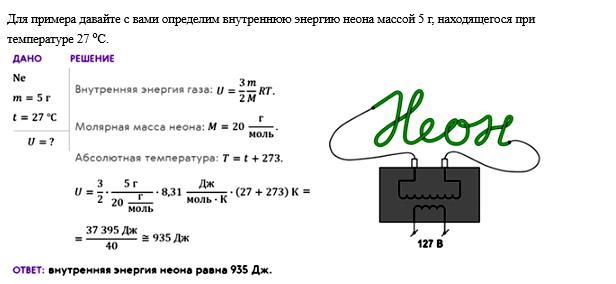

| 
| Решение  ΔU = А + Q, A = 0, ΔU = Q ΔU = А + Q, A = 0, ΔU = Q

|
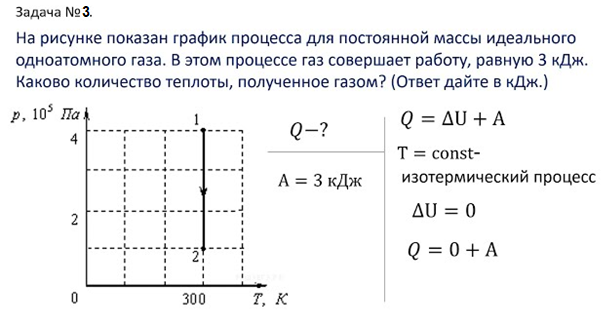
Ответ: ΔU = 3кДж
Задача 4*. Вычислим внутреннюю энергию воздуха, находящегося в классе. Давление атмосферное 1,01 · 105 Па, объём возьмём по размерам класса: 6 × 12 × 3 м3. Учитывая, что воздух состоит из кислорода и азота, число степеней свободы равно 5, как у всех двухатомных газов.
| Дано: р = 1,01 · 105 Па,
V = 6 · 12 · 3 м3,
i = 5. | Решение U = (i/2)pV;
U = (5/2) · 1.01 · 105 · 6 · 12 · 3 = 5,5 · 107 Дж.
|
| U – ? |
| Ответ: 5,5 · 107 Дж. |
|
Это почти такая же энергия, которая требуется для подъёма тяжёлого самолёта на высоту 30 м.
Если остается время по Рымкевичу решить № 650, 651, 652.
VI. Итог урока
1.От какого макроскопического параметра зависит внутренняя энергия идеального газа?
2.Как изменяется температура тела, если оно отдаёт энергии больше, чем получает извне?
3.Моль, какого газа (гелия или водорода) имеет большую внутреннюю энергию при одинаковой температуре газа?
4.Как можно определить внутреннюю энергию жидкости газа?
VII. Домашнее задание
§75, С1,2 стр.250. Посмотреть прикрепленный видеоматериал. Дополнительно: Рымкевич №621, 623.624.
VIII. Рефлексия
Какие цели мы перед собой ставили в начале урока?
Эти цели достигнуты?
Ход урока
1. Организационный этап (знакомство с классом, знакомство с планом работы на уроке).
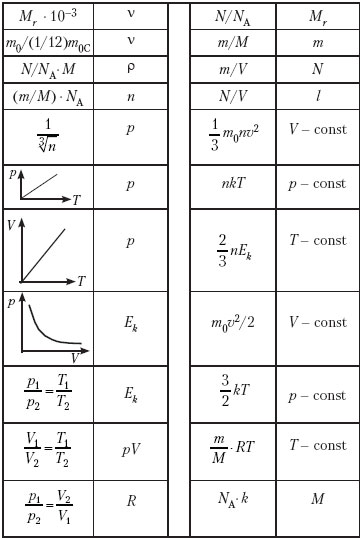
2. Повторение (актуализация знаний, повторение формул по МКТ газа, игра в домино: на каждую парту раздаётся комплект карточек домино, которые за определённое время надо разложить так, чтобы получился замкнутый круг; начать можно с любой карточки).
3. Изучение нового материала
• Урок начнём с показа картин:
– Использование мускульной силы человека и животных для совершения работы (картина из набора по истории).
– Использование простых механизмов (рычага, блоков, клина, ворота, наклонной плоскости) для совершения работы.
– Использование энергии ветра и воды.
– Использование перехода газа из одного состояния в другое или вещества из одного состояния в другое для получения телом механической энергии, т.е. перехода внутренней энергии в механическую (паровые турбины, тепловые электростанции, двигатели внутреннего сгорания).
• Термодинамика – часть физики, показывающая, что внутреннюю энергию можно использовать.
• Опыт с пластилиновым шариком (поднятый шарик обладает потенциальной энергией, при падении она переходит в кинетическую, но, упав на пол, шарик не отскакивает. Куда исчезла энергия? Что произошло с шариком?).
• Определение понятия «внутренняя энергия» – это энергия молекул, из которых состоит тело. Обозначается U, измеряется в джоулях (Дж).
• Какой энергией обладают молекулы? Почему? (Кинетической, потому что движутся. Потенциальной, потому что взаимодействуют.)
• Для чего мы ввели модель идеального газа? (Чтобы не учитывать взаимодействие молекул, т.к. идеальный газ – это газ, молекулы которого не взаимодействуют.) Какой вывод можно сделать об энергии молекул идеального газа? (Они обладают только кинетической энергией.)
• Мы знаем, что молекулы газа в пространстве движутся по трём направлениям: Х, Y, Z. Если кинетическая энергия молекулы равна Ек = (3/2)kТ, то на одно направление приходится энергия kТ/2. Число 3 называют числом степеней свободы (количество направлений движения молекул) одно-атомного газа.
• А сейчас посмотрите опорный конспект вывода формулы внутренней энергии идеального газа (у каждого на парте).

• Поработаем с этим конспектом. На основании чего переходим от одного выражения к другому?
Вычислим внутреннюю энергию воздуха, находящегося в классе. Давление атмосферное 1,01 · 105 Па, объём возьмём по размерам класса: 6 × 12 × 3 м3. Учитывая, что воздух состоит из кислорода и азота, число степеней свободы равно 5, как у всех двухатомных газов.
| Дано: р = 1,01 · 105 Па,
V = 6 · 12 · 3 м3,
i = 5. | Решение U = (i/2)pV;
U = (5/2) · 1.01 · 105 · 6 · 12 · 3 = 5,5 · 107 Дж. Ответ: 5,5 · 107 Дж. |
| U – ? |
Это почти такая же энергия, которая требуется для подъёма тяжёлого самолёта на высоту 30 м.
4. Выводы по уроку
Что мы сегодня узнали? (Что такое термодинамика, внутренняя энергия, число степеней свободы.) Какова цель урока? (Для чего нужно изучать внутреннюю энергию и как её вычислять для идеального газа.)
5. Проверка усвоения. Выполните тестовое задание. Одну карточку контроля (обе лежат на каждом столе) заполните для учителя, другую – для себя, чтобы оценить свою работу.
1. Найдите внутреннюю энергию 2 кг водорода при температуре 200 °С.
А) 6,1 кДж; Б) 6,1 МДж; В) 610 000 Дж.
2. Найдите внутреннюю энергию 5 м3 гелия при давлении 105 Па.
А) 7,5 МДж; Б) 7,5 кДж; В) 750 000 Дж.
3. Сравните внутреннюю энергию 32 г кислорода и 2 г водорода при температуре 23 °С.
А) UО UН; Б) UО UН ; В) UО = UН.
4. Сравните внутреннюю энергию 1 моля кислорода и 1 моля аргона при одной и той же температуре.
А) UО UAr; Б) UО UAr; В) UО = UAr.
5. От каких величин зависит внутренняя энергия газа?
А) только от Т; Б) только от V; В) от Т и V.
Карточка контроля
| | А | Б | В |
| 1 | | × | |
| 2 | | | × |
| 3 | | | × |
| 4 | | × | |
| 5 | | | × |
6. Рефлексия. По оставшейся карточке оцените свою работу. Сколько верных ответов – такая и оценка.
7. Домашнее задание. § 54 по учебнику Касьянова В.А. «Физика-10» до раздела «Изменения внутренней энергии». Вопросы 1–4 на с. 266.
8. Финал. Учитель. Благодарю за работу! Мне сегодня было приятно с вами работать.











 ΔU = А + Q, A = 0, ΔU = Q
ΔU = А + Q, A = 0, ΔU = Q