
Соединения серы


Н 2 S
Встречается в природе в составе нефти, природного газа, вулканического газа и в горячих источниках. . Кроме того, он образуется при разложении белков погибших животных и растений, а также при гниении пищевых отбросов.
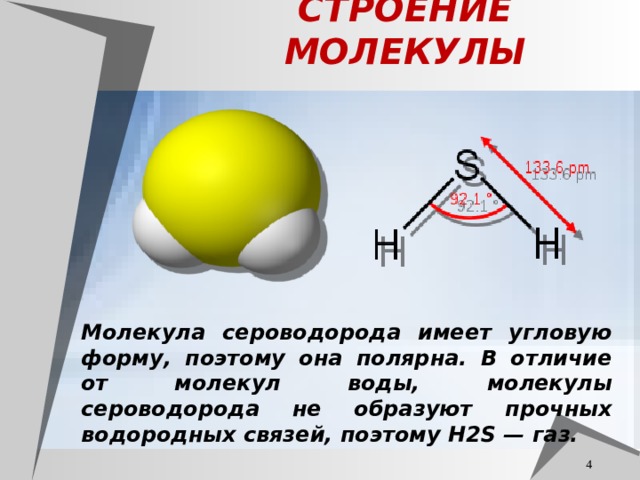
СТРОЕНИЕ МОЛЕКУЛЫ
Молекула сероводорода имеет угловую форму, поэтому она полярна. В отличие от молекул воды, молекулы сероводорода не образуют прочных водородных связей, поэтому H2S — газ.

ФИЗИЧЕСКИЕ СВОЙСТВА
- ядовитый газ тяжелее воздуха с неприятным запахом тухлых яиц, растворимый в воде. Насыщенный водный раствор H 2 S является сероводородной кислотой.

ПОЛУЧЕНИЕ
- В лаборатории обычно получают действием разбавленных кислот на сульфиды:
FeS + 2HCl = FeCl 2 + H 2 S
- Или при добавлении к сульфиду алюминия воды:
Al 2 S 3 + H2O = 2Al(OH) 3 + H 2 S
- водород + сера H 2 + S = H 2 S
- конц. серная кислота + активный металл
8 Na + 5 H 2 SO 4 ----- 4 Na 2 SO 4 + H 2 S + 4 H 2 O

ХИМИЧЕСКИЕ СВОЙСТВ А
- Сероводород — сильный восстановитель .
- сгорание
2 H 2 S + 3 O 2 =2 SO 2 + 2 H 2 O
- взаимодействие с некоторыми солями тяжелых металлов
H 2 S + CuCl 2 = CuS + 2 HCl
- взаимодействие с некоторыми неорганическими веществами по реакциям окисления-восстановления
2 H 2 S + SO 2 = 3 S + 2 H 2 О

ХИМИЧЕСКИЕ СВОЙСТВ А
- В воде сероводород мало растворим, водный раствор H2S является очень слабой кислотой:
- H 2 S → HS − + H+
- С основаниями реагирует:
H 2 S + 2NaOH = Na 2 S + 2H 2 O
(обычная соль, при избытке NaOH)
- H 2 S + NaOH = NaHS + H 2 O
(кислая соль, при отношении 1:1)
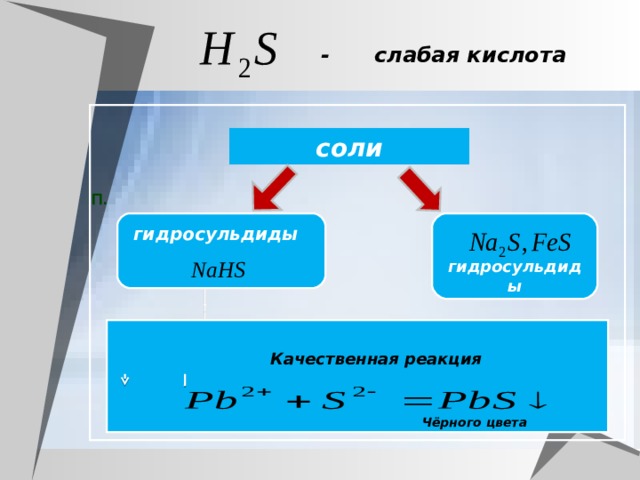
- слабая кислота
соли
П.
гидросульдиды
гидросульдиды
Качественная реакция
Чёрного цвета

ПРИМЕНЕНИЕ
- Сероводород из-за своей токсичности находит ограниченное применение.
- В аналитической химии сероводород и сероводородная вода используются как реагент для осаждения тяжёлых металлов, сульфиды которых очень слабо растворимы
- В медицине — в составе сероводородных ванн
- Сероводород применяют для получения серной кислоты, элементной серы, сульфидов
- Используют в органическом синтезе для получения тиофена и меркаптанов
- В последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моря, в качестве энергетического и химического сырья.


SO 2
СЕРНИСТЫЙ ГАЗ
Нахождение в природе
Оксид серы ( lV ) – сернистый газ, являющийся одним из главных загрязнителей атмосферного воздуха, кислотный оксид, очень хорошо растворимый в воде, образует слабую сернистую кислоту

СТРОЕНИЕ МОЛЕКУЛЫ

ПОЛУЧЕНИЕ
В промышленности: обжиг сульфидов:
4FeS 2 + 11O 2 → 2Fe 2 O 3 + 8SO 2 ↑
ZnS + O 2 = ZnO + SO 2

ФИЗИЧЕСКИЕ СВОЙСТВА
бесцветный газ с характерным резким удушливым запахом (запах загорающейся спички); хорошо растворяется в воде с образованием нестойкой сернистой кислоты; под давлением сжижается при комнатной температуре; ядовит; обесцвечивает многие красители, убивает микроорганизмы.

Химические свойства оксида серы (IV)
- Относится к кислотным оксидам . Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
SO 2 + H 2 O ↔ H 2 SO 3 .
- Со щелочами образует сульфиты:
SO 2 + 2NaOH → Na 2 SO 3 + H 2 O.
- Химическая активность SO 2 весьма велика. Наиболее ярко выражены восстановительные свойства SO 2 , степень окисления серы в таких реакциях повышается:
SO 2 + Br 2 + 2H 2 O → H 2 SO 4 + 2HBr,
2SO 2 + O 2 → 2SO 3 (требуется катализатор V 2 O 5 и температура 450°С),

Химические свойства оксида серы (IV)
- Данная реакция является качественной реакцией на сульфит-ион SO 3 2- и на SO 2 (обесцвечивание фиолетового раствора).
5SO 2 + 2KMnO 4 + 2H 2 O → 2H 2 SO 4 + 2MnSO 4 + K 2 SO 4 .
- В присутствии сильных восстановителей SO 2 способен проявлять окислительные свойства . Например, для извлечения серы их отходящих газов металлургической промышленности используют восстановление SO 2 оксидом углерода(II) :
SO 2 + 2CO → 2CO 2 + S↓.
Или для получения фосфорноватистой кислоты:
PH 3 + SO 2 → H(PH 2 O 2 ) + S↓
Проявляет как свойства окислителя, так и восстановителя:

Оксид серы ( IV) ПРИМЕНЕНИЕ
В пищевой промышленности используется как консервант (Е220) . Используются при производстве многих продуктов и полуфабрикатов, а также для дезинфекции тары. Негативно влияет на функции почек. Раздражитель дыхательных путей, может вызвать приступ астмы;
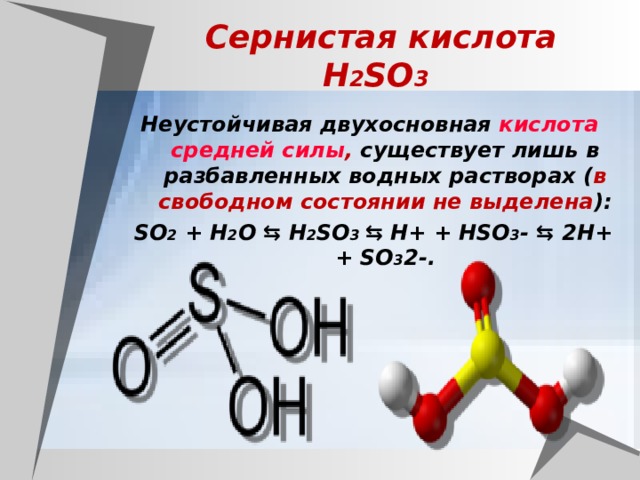
Сернистая кислота H 2 SO 3
Неустойчивая двухосновная кислота средней силы , существует лишь в разбавленных водных растворах ( в свободном состоянии не выделена ):
SO 2 + H 2 O ⇆ H 2 SO 3 ⇆ H+ + HSO 3 - ⇆ 2H+ + SO 3 2-.

Соли ее – сульфиты, растворимые из них только соли щелочных металлов.
Сульфиты - это средние соли (CaSO 3 ) ,
но есть и кислые – гидросульфиты (NaHSO 3 ) .
Сульфиты и гидросульфиты реагируют
с сильными кислотами с образованием
сернистого газа
K 2 SO 3 + 2HNO 3 ---2KNO 3 + SO 2 + H 2 O

Применение с ернистой кислоты H 2 SO 3
- Сернистая кислота и её соли применяют как восстановители, для беления шерсти , шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей ( хлора ).
- Сернистую кислоту применяют при консервировании плодов и овощей.
- Гидросульфит кальция Са(HSO3)2 (сульфитный щелок) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги ).


Оксид серы (VI) СТРОЕНИЕ МОЛЕКУЛЫ
SO 3 — высший оксид серы,
тип химической связи: ковалентная полярная

Оксид серы (VI) Физические свойств а
В обычных условиях легколетучая бесцветная жидкость с удушающим запахом. При температурах ниже 16,9 °C застывает с образованием смеси различных кристаллических модификаций твёрдого SO 3 .

ХИМИЧЕСКИЕ СВОЙСТВА
- Проявляет только свойства окислителя:
3SO 3 + H 2 S → 4SO 2 + H 2 O
- Растворяется в 100%-й серной кислоте, образуя олеум:
H 2 SO 4 (100 %) + SO 3 → H 2 S 2 O
Проявляют свойства типичного кислотного оксида:

ОКИСЛИТЕЛЬНО- ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА SO 3
характеризуется сильными окислительными свойствами, восстанавливается, обычно, до сернистого ангидрида:
5SO 3 + 2 P → P 2 O 5 + 5 SO 2
3SO 3 + H 2 S → 4 SO 2 + H 2 O
2SO 3 + 2 KI → SO 2 + I 2 + K 2 SO 4 .
При взаимодействии с хлороводородом образуется хлорсульфоновая кислота:
SO 3 + HCl → HSO 3 Cl
Также присоединяет хлор, образуя тионилхлорид:
SO 3 + Cl 2 + 2SCl 2 → 3 SOCl 2

в качестве растворителя в лабораториях;
в текстильной промышленности (отбеливание);
в качестве обесцвечивающего вещества в сахарном производстве, пищевой промышленности,
для дезинфекции помещений и уничтожения паразитов на теле животных
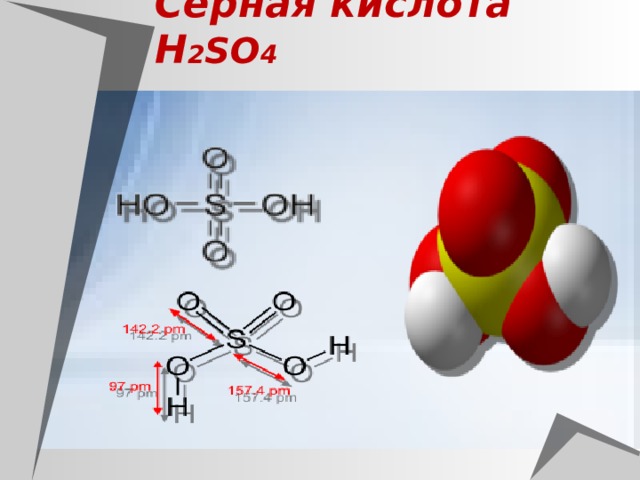
Серная кислота Н 2 SO 4

НАХОЖДЕНИЕ В ПРИРОДЕ
- Вулкан Малый Семячик
- Вулканический хребет длиной около 3 км., на гребне которого имеются три кратера. В южном (кратер Троицкого) на глубине 170м. находится необычное кислое озеро. Температура этого непрозрачного озера колеблется от +27 0 С до +42 0 С, а уровень минерализации соответствует раствору серной и соляной кислот средней концентрации. Поражают размеры озера: ширина около полукилометра, а глубина - до 140м. Существуют предположения, что кислотное озеро возникло сравнительно недавно в результате извержения вулкана, произошедшего незаметно для людей.

Физические свойства серной кислоты .
- Безводная серная кислота - это бесцветная маслянистая жидкость без запаха,
- смешивается с водой в любых отношениях,
- t пл. =10,3 0 С, t кип = 296 0 С,
=1, 84 г / см 3 .
- Обладает сильным водоотнимающим действием .
Техника безопасности при работе с серной кислотой
- Серная кислота очень едкое вещество – при попадании на кожу вызывает сильнейшие ожоги.
- ПРИ СМЕШИВАНИИ СЕРНОЙ КИСЛОТЫ С ВОДОЙ ВЫДЕЛЯЕТСЯ БОЛЬШОЕ КОЛИЧЕСТВО ТЕПЛОТЫ.
- ПРИ РАСТВОРЕНИИ СЕРНОЙ КИСЛОТЫ НУЖНО ВЛИТЬ ЕЕ ТОНКОЙ СТРУЁЙ В ВОДУ И ПЕРЕМЕШИВАТЬ.
- ЕСЛИ ВОДУ ВЛИТЬ В СЕРНУЮ КИСЛОТУ, ТО ВОДА, НЕ УСПЕВ СМЕШАТЬСЯ С КИСЛОТОЙ , МОЖЕТ ЗАКИПЕТЬ И ВЫБРОСИТЬ БРЫЗГИ НА ЛИЦО И РУКИ.

ХИМИЧЕСКИЕ СВОЙСТВА
Раствор серной кислоты взаимодействует с металлами , стоящими в ряду активности до водорода.
- Ag + H 2 SO 4 = т.к. серебро стоит в ряду активности после водорода
- 2Al + 3H 2 SO 4 = Al 2 (SO 4 ) 3 +3H 2
2Al 0 + 6H + = 2Al 3+ +3H 2 0
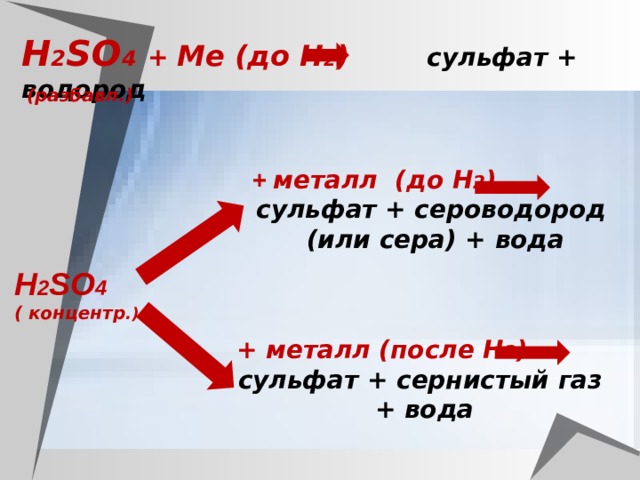
Н 2 SO 4 + Ме (до Н 2 ) сульфат + водород
(разбавл.)
+ металл (до Н 2 )
сульфат + сероводород
(или сера) + вода
Н 2 SO 4
( концентр .)
+ металл (после Н 2 )
сульфат + сернистый газ
+ вода

Раствор серной кислоты взаимодействует с основными и амфотерными оксидами.
- М nO + H 2 SO 4 = MnSO 4 + H 2 O
М nO + 2H + = Mn 2+ + H 2 O
- Mn 2 O 7 + H 2 SO 4 = т.к. Mn 2 O 7 -кислотный оксид

Серная кислота взаимодействует с основаниями и амфотерными гидроксидами .
- 2К O Н + H 2 SO 4 = К 2 SO 4 + 2 H 2 O
сульфат калия
ОН - + H + = H 2 O
- К O Н + H 2 SO 4 = КН SO 4 + Н 2 O
гидросульфат калия
O Н - + 2 H + + SO 4 2- = Н SO 4 - + H 2 O

Серная кислота взаимодействует с солями, если образуется газ или осадок.
- FeS + H 2 SO 4 =FeSO 4 +H 2 S
FeS + 2H + =Fe 2+ +H 2 S
- Mg(NO 3 ) 2 + H 2 SO 4 =
- Ba(NO 3 ) 2 + H 2 SO 4 = BaSO 4 + 2HNO 3
Ba 2+ + SO 4 2- = BaSO 4
- K 2 CO 3 + H 2 SO 4 = K 2 SO 4 + CO 2 + H 2 O
CO 3 2- + 2H + = CO 2 + H 2 O
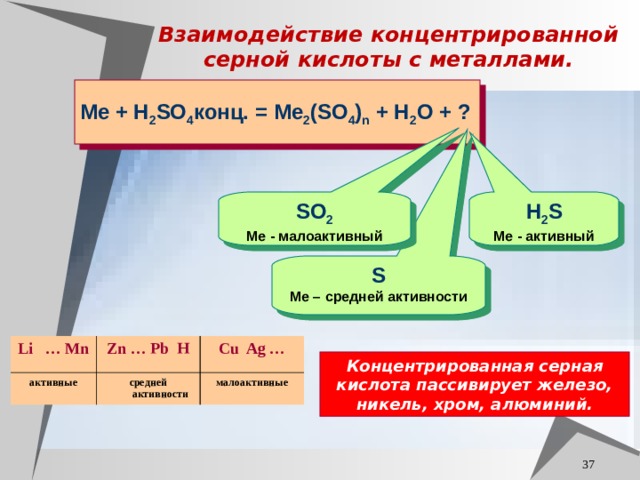
Взаимодействие концентрированной серной кислоты с металлами.
Me + H 2 SO 4 конц. = Me 2 (SO 4 ) n + H 2 O + ?
H 2 S
SO 2
Ме - активный
Ме - малоактивный
S
Ме – средней активности
Li … Mn
активные
Zn … Pb H
Cu Ag …
средней активности
малоактивные
Концентрированная серная кислота пассивирует железо, никель, хром, алюминий.

Соли серной кислоты
Серная кислота как двухосновная кислота образует два ряда солей - кислые - гидросульфаты и средние - сульфаты. В безводном состоянии выделены только гидросульфаты щелочных металлов. Средние сульфаты (безводные) - как правило, бесцветные кристаллические вещества, склонные к образованию кристаллогидратов (часто окрашеных), например:
Na2SO4*10H2O - глауберова соль (мирабилит) - бесцветная
MgSO4*7H2O - горькая (английская) соль - бесцветная
CuSO4*5H2O - медный купорос - голубой
FeSO4*7H2O - железный купорос - голубовато-зеленый
CaSO4*2H2O - гипс - белый

СВОЙСТВА СУЛЬФАТОВ
Сульфаты при нагревании разлагаются (кроме сульфатов щелочных металлов, которые термически устойчивы), например CaSO4 - при 1400oС:
2CaSO4 = 2CaO + 2SO2 + O2
Сульфаты переходных металлов разлагаются при более низких температурах, например Fe2(SO4)3 - при 700-800oС:
Fe2(SO4)3 = Fe2O3 + 3SO3

Производство серной кислоты
- Производство H 2 SO 4 в мире неуклонно растет. Так, в период с 2000 по 2005 год оно возросло со 160 до 189 млн тонн.
- В России объем производства серной кислоты c 2000 по 2005 год возрос в среднем на 1 млн тонн и составил 9,3 млн тонн.

Производство серной кислоты
Сырьём для получения серной кислоты служат сера , сульфиды металлов , сероводород , отходящие газы теплоэлектростанций, сульфаты железа, кальция и др.
Основные этапы получения серной кислоты:
- Обжиг сырья с получением SO 2
- Окисление SO 2 в SO 3
- Абсорбция SO 3
В промышленности применяют два метода окисления SO 2 в производстве серной кислоты: контактный — с использованием твердых катализаторов (контактов), и нитрозный — с оксидами азота.
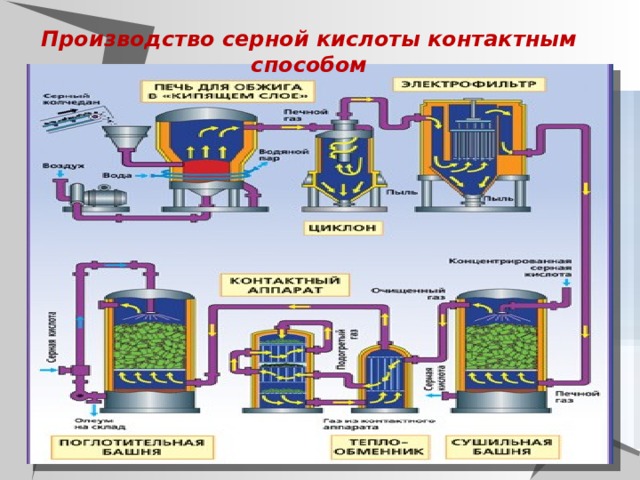
Производство серной кислоты контактным способом

Серная кислота используется для получения фосфорных и азотных удобрений: простого суперфосфата, двойного суперфосфата, преципитата и сернокислого аммония .
- при производстве 1 т . суперфосфата из фторапатита, не содержащего гигроскопической воды, расходуется 600 кг. 65-процентной серной кислоты

Применение серной кислоты в металлургии
- « Травление» – обнаружение трещин на поверхности металлов.
- В гальванических цехах серную кислоту используют для обезжиривания поверхности металла перед нанесением покрытия.
- Переработка руд редких металлов

- Серная кислота используется в качестве электролита в автомобильных аккумуляторах .
H 2 SO 4
Лекарственные препараты
Синтетические моющие средства

Домашнее задание
- § 18 упр.3,6 – письменно
- ( упр. 8,9 – творческие)
- § 19 упр.5 письменно








































































