| Организационный момент ( подготовка учащихся к активному усвоению знаний) | Приветствует учащихся.
Здравствуйте! Присаживайтесь. Закройте глаза и мысленно повторяйте за мной: «Я сегодня готов к работе, буду внимателен, сосредоточен, догадлив, сообразителен, уверен в себе». Всем желаю успеха в работе! | Приветствуют учителя, готовятся к уроку. повторяют за учителем настой на урок; настраиваются на восприятие темы и деятельность на уроке
| Личностные (смыслообразование) |
|
Этап актуализации знаний, целеполагания на уроке (Цель: актуализация соответствующих мыслительных операций и познавательных процессов; формирование у учащихся способности самостоятельно ставить учебные цели на урок)
| У меня в руках бенгальский огонь! Его цвет подсказывает нам то, что в его состав входит порошок алюминия – Al. Если порошок алюминия сильно нагреть, т.е. поджечь, что мы сейчас и сделаем, то он воспламеняется и сгорает ослепительным пламенем. (бенгальский огонь горит в руках только учителя!)
Ответьте на вопросы: -Какое явление мы наблюдаем физическое или химическое, объясните разницу?
-Как называется процесс, который мы наблюдаем?
-Назовите признаки, сопровождающие данный процесс реакции. - Какое самое главное вещество, находящиеся в составе воздуха, поддерживает этот процесс? - Какие два вещества в результате этого процесса вступили во взаимодействие? - Вещество какого состава должно получится, после того как огонь погаснет?
О веществах такого состава сегодня и пойдёт речь. Это ОКСИДЫ
Какие цели ставим перед собой?
Давайте вместе составим план для реализации поставленных целей.
С помощью, каких средств буду реализованы наши цели и план урока?
Давайте сформулируем, какими критериями будем достигать целей урока?
| Слушают и наблюдают за явлением
Отвечают на поставленные вопросы.
-Наблюдаем химическое явление, происходит изменение состава вещества, было одно, а станет другое.
-Наблюдаем процесс горения, окисление кислородом.
- Признаки, сопровождающие горение –свечение, выделение тепла.
-Вещество поддерживающие горение - кислород!
-Во взаимодействие вступили алюминий и кислород воздуха.
- Образующиеся вещество должно быть сложного состава и в нём должен быть обязательно
АЛЮМИНИЙ и КИСЛОРОД - Речь на уроке пойдёт о веществах, состоящих из двух элементов (бинарных), а раз горение – это окисление, главным в горении является КИСЛОРОД!
Значит говорить будем о бинарных соединениях, в которых обязательно присутствует КИСЛОРОД!
Предлагают формулировку темы урока
Формулируют цели урока: 1.Узнать, что такое оксиды? 2. Научиться давать названия оксидам. 3. Познакомиться классификацией соединений. 4.Выявить правила составления оксидов по степени окисления 5. Владеть правилами составления оксидов. Называют пункты плана: 1.Определение понятия ОКСИДЫ. 2.Классификация оксидов. 3. Алгоритм составления оксидов. 4.Работа с алгоритмом. 5. Названия оксидам.
Называют средства урока: учебник, рабочая тетрадь
Критерии урока: «5» - если я думаю, аргументирую, размышляю, объясняю. «4»» - если я | Коммуникативные (учет разных мнений постановка вопросов)
Познавательные (постановка и решение проблемы, логические универсальные действия)
Регулятивные: целеполагание
Личностные (самоопределение) Регулятивные (оценка результатов работы) Познавательные (общеучебные, логические универсальные действия) Коммуникативные (учет разных мнений) |
| Этап открытия нового знания. (Давать определение «оксиды», распознавать оксиды среди других веществ, составлять формулы оксидов и называть их, классифицировать).
| Вспомним понятие степени окисления.
Поработаем в парах по карточкам. Посмотрите на задание карточки и сформулируйте цель: K2O, SO2, P2O5, SO3, Cu2O, Mn2O7, FeO, Al2O3
Проверьте по представленному образцу у ученика по документ - камере; дайте оценку выполненного задания.
- Что общего обнаружили?
- Какой вывод при определении степени окислении в оксидах можем сделать?
Сформулируем определение оксидов, исходя из его состава.
Сравните полученное определение с текстом учебника и запишите его в тетрадь.
Мы уже знаем, что все элементы Периодической системы делятся на металлы и неметаллы. Значит, в качестве второго элемента в оксиде может быть один из них.
Сейчас поработаем в парах. Вернемся к карточке и распределим предложенные оксиды K2O, SO2, P2O5, SO3, Cu2O, Mn2O7, FeO, Al2O3 в таблицу: Оксиды металлов и неметаллов.
Назовите цель работы?
Представьте свои результаты и дайте оценку выполненной работы.
Посмотрите на план урока и скажите, какие пункты уже реализованы. Отметим их.
Все оксиды можно разделить на две группы: солеобразующие (основные, кислотные, амфотерные) и несолеобразующие.
Работая в группе с предложенной вам таблицей и текстом учебника составьте кластер и занесите его в тетрадь.
Проверим данную работу и сравним со своими результатами, используя документ-камеру.
От чего же зависит характер свойств оксидов?
Отметим на плане урока выполненную цель.
Вспомните правила составления формул веществ по степени окисления.
А сейчас попробуйте дать названия формулам веществ. Для этого необходимо составить алгоритм, работая в группе, используя текст учебника.
Какие цели нами уже достигнуты? Что осталось нам выполнить? | Вспоминают определение
Степень окисления (ст.ок.) — это условный заряд атомов химического элемента в сложном веществе, вычисленный на основе предположения, что оно состоит из простых ионов.
Нужно определить степень окисления элементов в указанных соединениях
Начинают работать в парах.
В составе присутствует кислород.
-Степень окисления у кислорода во всех соединениях равна - 2.
Выявляют и называют новое понятие Оксиды–сложные вещества, состоящие из двух элементов один из которых кислород со степенью окисления -2. Сравнивают и записывают в тетрадь.
Работают в парах Заполняют таблицу Оксиды неметаллов Оксиды металлов
Распределить предложенные оксиды по группам: оксиды металлов и неметаллов
Представляют результаты, сравнивают со своими и комментируют
Достигнут первый пункт плана.
Работают в группе, выполняют самостоятельную работу по составлению кластера «Классификация оксидов»: ОКСИДЫ СОЛЕОБРАЗУЮЩИЕ НЕСОЛЕОБРАЗУЮЩИЕ КИСЛОТНЫЕ 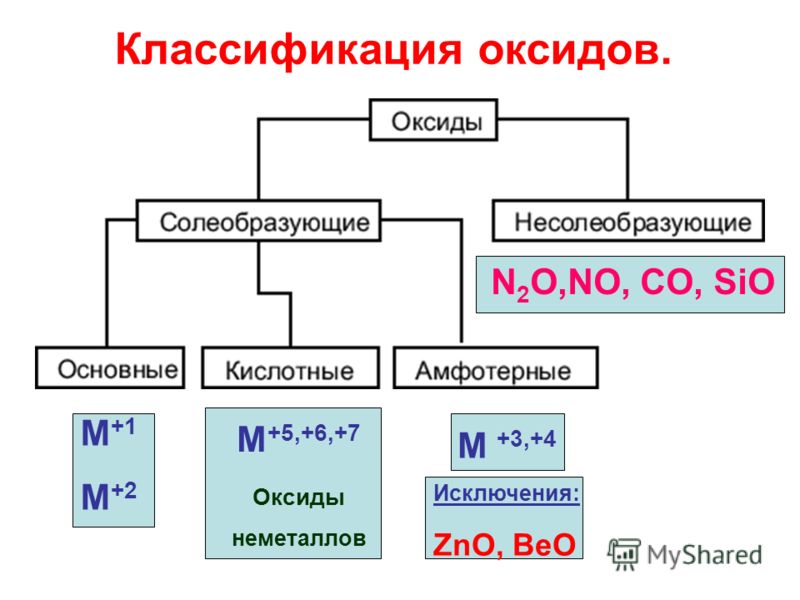
Вывод: характер свойств оксидов в первую очередь зависит от степени окисления элемента.
Учащиеся называют правила по алгоритму.
Работают группе по составлению алгоритма в течение 2 минут

Учащиеся составляют алгоритм:
Оксид + название элемента в родительном падеже (степень окисления в случае ее переменности)
От каждой группы представитель разъясняет правила, а остальные комментируют и сопоставляют со своими.
отвечают на вопросы | Регулятивные (оценка, саморегуляция, контроль и самоконтроль) Познавательные (общеучебные универсальные действия)
Регулятивные УУД: Умение организовать выполнение заданий учителя Умение работать с текстом Познавательные УУД: умение структурировать учебный материал, выделять в нем главное. Коммуникативные УУД: самостоятельное учебное взаимодействие в паре, в группе.
|
| Этап включения в систему знания и закрепление изученного материала ( Цель: Дать качественную оценку работы класса и отдельных учащихся)
| Задание № 1. Распределите оксиды по классам: кислотные основные амфотерные несолеобразующие K2O, ZnO, AI2O3, V2O5, B2O3, H2O, CaO, NO, SO2, FeO Итоги проверки: «5» - все правильно; «4» - 1-2 ошибки; «3» - 3-4 ошибки; 5 и более ошибок – плохо усвоен материал
Проверка: кислотные V2O5 B2O3 SO2 основные K2O FeO СaO амфотерные ZnO AI2O3 несолеобразующие H2O NO
Задание № 2. Выполнение задания по вариантам. 1 вариант. Составьте формулы оксидов: натрия, азота (I), серы (VI) и дайте названия этим веществам.
2 вариант. Составьте формулы оксидов: магния, углерода (II), марганца (VII)
Итоги взаимопроверки: «5» - все правильно; «4» - 1-2 ошибки; «3» - 3-4 ошибки; 5 и более ошибок – плохо усвоен материал Вернемся к плану и отметим пункт плана, который отрабатывали? | Выполнение задания № 1, самопроверка
Выполнение задания № 2 по вариантам, взаимопроверка, выставление оценки. | Регулятивные (оценка, саморегуляция, контроль и самоконтроль) Познавательные (общеучебные универсальные действия) |
























