Химическая связь. Типы химической связи
От берега до берега
Можно сделать мост.
Соединить два атома
В молекулу – вопрос…

Задачи урока:
- дать определение химической связи;
- познакомиться с различными типами химической связи;
- научиться определять тип связи в различных соединениях.
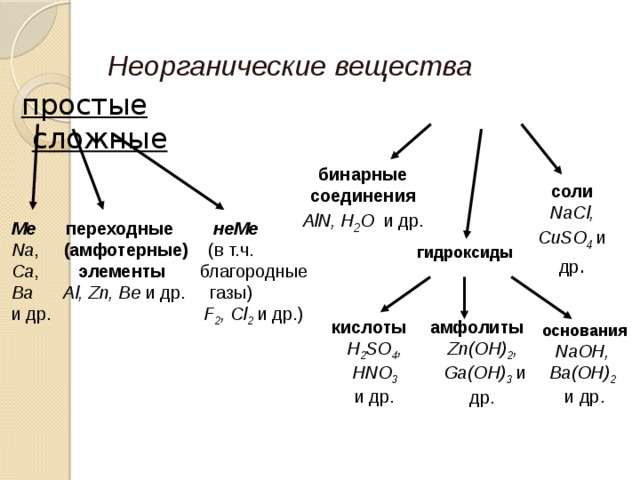
Неорганические вещества
простые сложные
бинарные соединения
AlN, H 2 O и др.
соли
NaCl, CuSO 4 и др .
Ме переходные неMe
Na , (амфотерные) (в т.ч.
Ca , элементы благородные
Ba Al, Zn, Be и др. газы)
и др. F 2 , Cl 2 и др.)
гидроксиды
кислоты
H 2 SO 4 ,
HNO 3
и др.
амфолиты
Zn(OH) 2 ,
Ga(OH) 3 и др.
основания
NaOH,
Ba(OH) 2
и др.
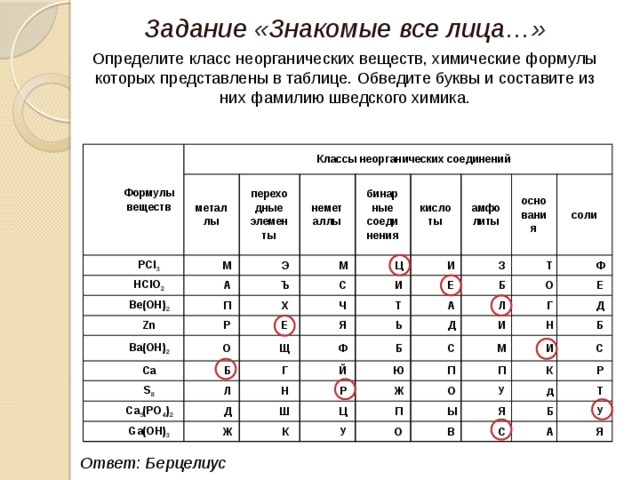
Задание «Знакомые все лица…»
Определите класс неорганических веществ, химические формулы которых представлены в таблице. Обведите буквы и составите из них фамилию шведского химика.
Ответ: Берцелиус
Формулы веществ
Классы неорганических соединений
металлы
PCl 3
М
переходные элементы
HClO 2
неметаллы
Э
Be(OH) 2
А
П
М
бинарные соединения
Zn
Ъ
Ba(OH) 2
Ц
Р
Х
кислоты
С
Ч
О
И
амфолиты
Ca
И
Е
Я
З
Щ
Е
S 8
Т
основания
Б
Ф
Л
Т
А
Ca 3 (PO 4 ) 2
Г
Ь
Б
соли
Ф
Ga(OH) 3
Д
Й
О
Н
Л
Б
Д
Ж
С
Г
Р
Е
Ю
Ш
И
Ц
К
Ж
Н
Д
М
П
У
О
И
П
Б
П
Ы
О
У
К
С
В
д
Р
Я
С
Т
Б
А
У
Я

Химическая связь – это взаимодействие атомных частиц, сопровождающееся перестройкой электронных оболочек (орбиталей), как правило, ВЭУ.
Химическая связь – это связь между химическими частицами (атомными частицами, молекулами, ионами), объединяющая их в более сложные структуры (молекулы, ионы, ассоциаты).

Энергия химической связи – количество теплоты, поглощаемое при разрыве ковалентной связи или выделяемое при ее образовании (единица – кДж/моль).
Длина химической связи – расстояние между ядрами связываемых атомных частиц одного химического элемента или разных элементов (единицы – нанометр (нм), пикометр (пм)).
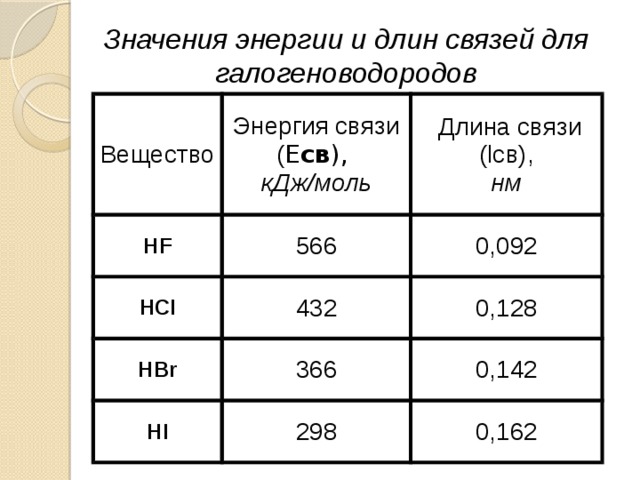
Значения энергии и длин связей для галогеноводородов
Вещество
HF
Энергия связи ( E св ), кДж/моль
566
HCl
Длина связи (lсв),
нм
0,092
432
HBr
0,128
366
HI
0,142
298
0,162
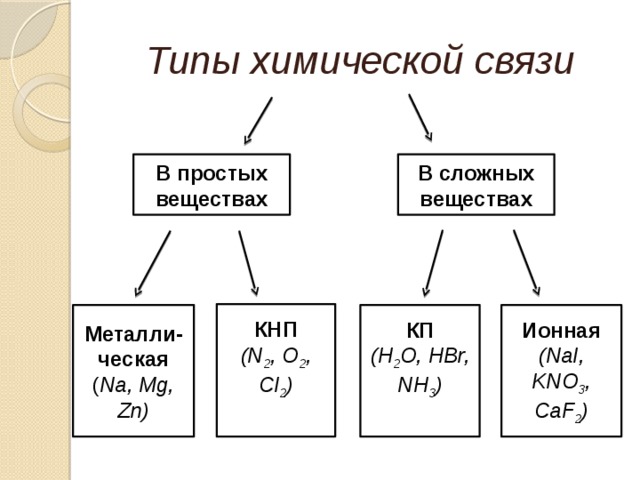
Типы химической связи
В простых веществах
В сложных веществах
КНП
(N 2 , O 2 , Cl 2 )
КП
Металли-
Ионная
ческая
(H 2 O, HBr, NH 3 )
(NaI, KNO 3 , СaF 2 )
( Na, Mg, Zn)
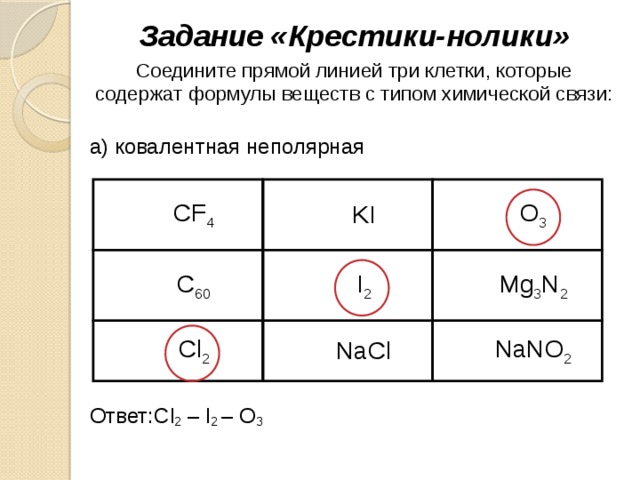
Задание «Крестики-нолики»
Соедините прямой линией три клетки, которые содержат формулы веществ с типом химической связи:
а) ковалентная неполярная
Ответ:Cl 2 – I 2 – O 3
CF 4
KI
C 60
O 3
I 2
Cl 2
NaCl
Mg 3 N 2
NaNO 2
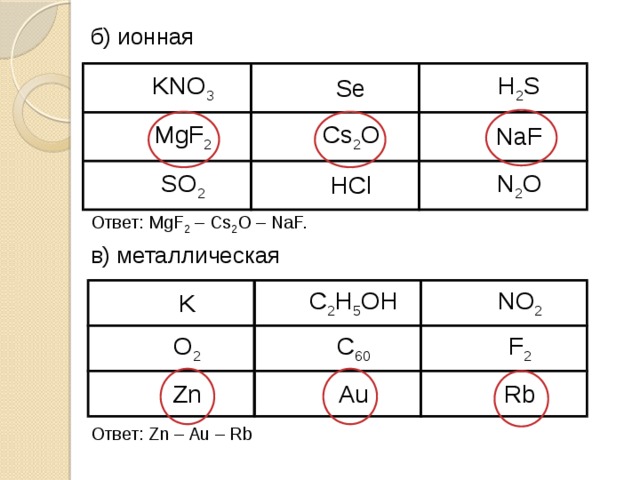
б) ионная
Ответ: MgF 2 – Cs 2 O – NaF.
в) металлическая
Ответ: Zn – Au – Rb
KNO 3
Se
MgF 2
SO 2
Cs 2 O
H 2 S
NaF
HCl
N 2 O
K
O 2
C 2 H 5 OH
NO 2
C 60
Zn
F 2
Au
Rb
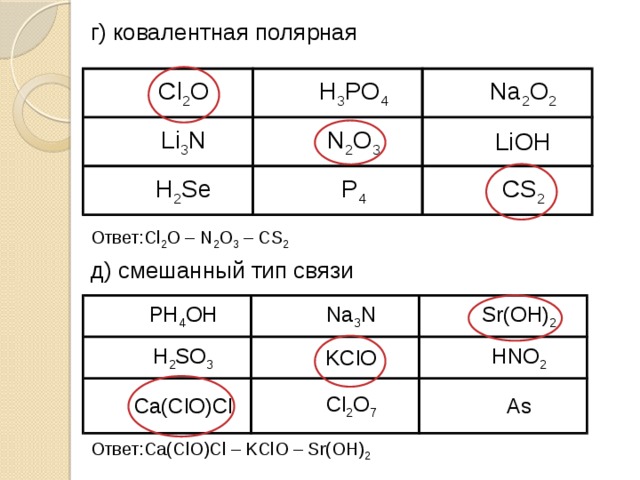
г) ковалентная полярная
Ответ:Cl 2 O – N 2 O 3 – CS 2
д) смешанный тип связи
Ответ:Ca(ClO)Cl – KClO – Sr(OH) 2
Cl 2 O
H 3 PO 4
Li 3 N
H 2 Se
Na 2 O 2
N 2 O 3
LiOH
P 4
CS 2
PH 4 OH
H 2 SO 3
Na 3 N
KClO
Sr(OH) 2
Ca(ClO)Cl
HNO 2
Cl 2 O 7
As
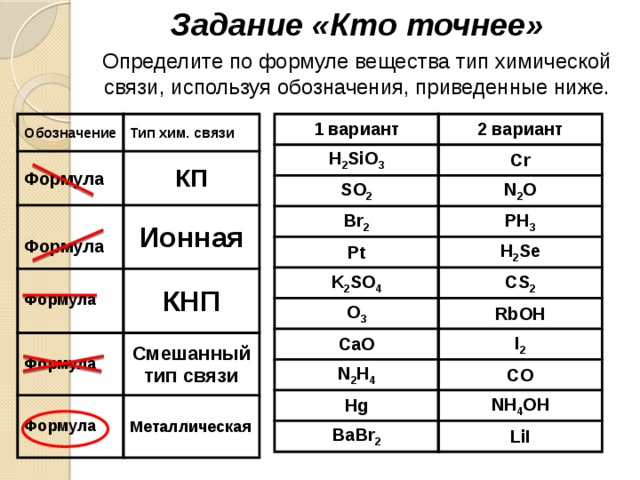
Задание «Кто точнее»
Определите по формуле вещества тип химической связи, используя обозначения, приведенные ниже.
1 вариант
Обозначение
H 2 SiO 3
2 вариант
Тип хим. связи
Формула
КП
Cr
SO 2
Br 2
Ионная
N 2 O
Формула
PH 3
Формула
КНП
Pt
K 2 SO 4
H 2 Se
Формула
Смешанный тип связи
Формула
Металлическая
CS 2
O 3
CaO
RbOH
I 2
N 2 H 4
CO
Hg
NH 4 OH
BaBr 2
LiI
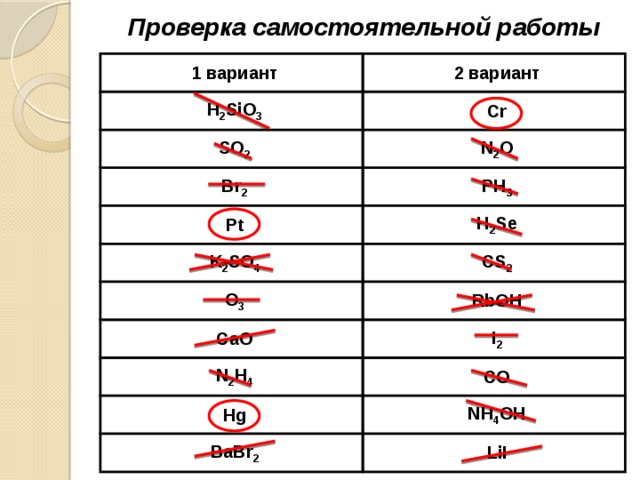
Проверка самостоятельной работы
1 вариант
2 вариант
H 2 SiO 3
Cr
SO 2
N 2 O
Br 2
PH 3
Pt
H 2 Se
K 2 SO 4
O 3
CS 2
RbOH
CaO
I 2
N 2 H 4
CO
Hg
NH 4 OH
BaBr 2
LiI
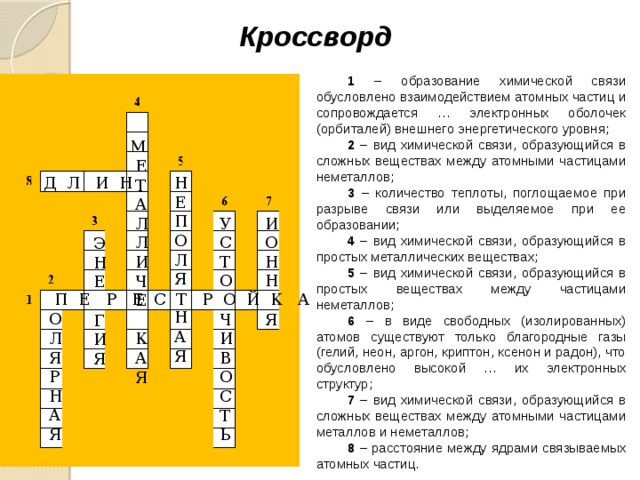
Кроссворд
1 – образование химической связи обусловлено взаимодействием атомных частиц и сопровождается … электронных оболочек (орбиталей) внешнего энергетического уровня;
2 – вид химической связи, образующийся в сложных веществах между атомными частицами неметаллов;
3 – количество теплоты, поглощаемое при разрыве связи или выделяемое при ее образовании;
4 – вид химической связи, образующийся в простых металлических веществах;
5 – вид химической связи, образующийся в простых веществах между частицами неметаллов;
6 – в виде свободных (изолированных) атомов существуют только благородные газы (гелий, неон, аргон, криптон, ксенон и радон), что обусловлено высокой … их электронных структур;
7 – вид химической связи, образующийся в сложных веществах между атомными частицами металлов и неметаллов;
8 – расстояние между ядрами связываемых атомных частиц.
М
Е
Т
А
Л
Л
И
Ч
Е
К
А
Я
Н
Д Л И Н
Е
П
О
Л
Я
Н
А
Я
И
У
О
С
Н
Т
Н
О
Я
Ч
И
В
О
С
Т
Ь
Э
Н
Е
Г
И
Я
П Е Р Е С Т Р О Й К А
О
Л
Я
Р
Н
А
Я






































