МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«ШАТКОВСКАЯ СРЕДНЯЯ ШКОЛА»
Муниципальный конкурс методических разработок уроков физики,
внеклассных мероприятий ««Отец» советской атомной бомбы»,
посвященный 120-летию со дня рождения И.В.Курчатова
УРОК-ИГРА ДЛЯ 9 КЛАССА
«Атом от А до Я»
Учитель физики: Сальникова
Анна Александровна
Стаж работы: 11 лет
Р.п. Шатки, 2023 г.
Урок-игра по физике для 9-х классов «Атом от А до Я»
Тип урока: обобщающий урок.
Цель урока: обобщить и систематизировать знания учащихся 9-х классов в области атомной физики.
Задачи урока:
1. Образовательные:
– повторить с учащимися основные понятия, формулы и законы в области атомной физики;
– проконтролировать степень усвоения знаний, умений и навыков по данной теме.
2. Развивающие:
– развивать интерес учащихся к физике, используя игровую деятельность;
– развивать у учащихся умения анализировать и систематизировать изученный материал.
3. Воспитательные:
– формировать умения и навыки коллективной работы;
– формировать у учащихся навыки взаимопомощи и взаимоконтроля.
Планируемые результаты:
1. Личностные:
– сформированность познавательных интересов;
– сформированность навыка рефлексии, признание своего права на ошибку и такого же права у другого человека.
2. Метапредметные:
– формирование умений анализировать и перерабатывать полученную информацию в соответствии с поставленными задачами, выделять основное содержание.
3. Предметные:
– знания о природе атома и атомного ядра.
Универсальные учебные действия:
1. Регулятивные:
– ориентироваться в различных подходах принятия решений (индивидуальное, принятие решения в группе, принятие решений группой);
— самостоятельно составлять алгоритм решения физической задачи или плана исследования с учётом имеющихся ресурсов и собственных возможностей, аргументировать предлагаемые варианты решений;
— делать выбор и брать ответственность за решение.
2. Познавательные:
– выявлять причинно-следственные связи при изучении физических явлений и процессов; делать выводы с использованием дедуктивных и индуктивных умозаключений, выдвигать гипотезы о взаимосвязях физических величин;
– анализировать, систематизировать и интерпретировать информацию различных видов и форм представления.
3. Коммуникативные:
– сопоставлять свои суждения с суждениями других участников диалога, обнаруживать различие и сходство позиций;
– понимать и использовать преимущества командной работы при решении конкретной физической проблемы;
– принимать цели совместной деятельности, организовывать действия по её достижению: распределять роли, обсуждать процессы и результаты совместной работы; обобщать мнения нескольких людей;
Форма работы: групповая.
Оборудование: компьютер, экран, презентация, карточки с заданиями, сигнальные карточки, призовые жетоны – «атомы», периодическая таблица Д.И.Менделеева.
Ход урока.
1. ОРГАНИЗАЦИОННЫЙ МОМЕНТ.
На данном этапе происходит мобилизация детей на занятие: приветствие; проверка готовности учащихся к уроку.
2. ЭТАП МОТИВАЦИИ.
– Здравствуйте, дорогие ребята! Сегодня мы проведём наш урок в форме игры, которая называется «Атом от А до Я». Она поможет вам вспомнить и обобщить все знания, которые вы получили, изучая атом и его строение. (Слайд №1)
Быть может, эти электроны –
Миры, где пять материков,
Искусства, знанья, войны, троны
И память сорока веков!
Еще, быть может, каждый атом –
Вселенная, где сто планет;
Там все, что есть, в объеме сжатом,
Но также то, чего здесь нет.
3. ИГРА «АТОМ ОТ А ДО Я»
Краткое описание игры: класс заранее делится на три команды, каждая команда выбирает себе капитана. Команды стремятся получить как можно больше "атомов" (призовых жетонов) в отдельных конкурсах, объявляемых учителем. В конце игры команды подсчитывают жетоны. Команда, набравшая больше всех жетонов, «награждается пятёрками», также награждаются самые активные игроки в других командах.
Задание 1. Дай название команде. (Слайд №2)
Для определения названия команды капитан выбирает конверт, в нём находятся определение, которое необходимо заменить одним словом-понятием, названием объекта из данной темы, это и будет названием команды. (Приложение 1)
1. Положительная частица, входящая в состав атомного ядра, – … .
2. Мельчайшая частица простого вещества – … .
3. Элементы, имеющие одинаковое зарядовое число и разные массовые числа – … .
Задание 2. Разминка. (Слайд №3)
Учитель задаёт вопросы по теме. Команда, которая первая поднимет сигнальную карточку, даёт ответ. За каждый правильный ответ команда получает жетон.
1. Кто открыл явление радиоактивности? (Беккерель)
2. Как заряжено ядро атома? (положительно)
3. Явление испускания атомами невидимых проникающих излучений. (радиоактивность)
4. Какой заряд имеет атом? (нейтральный)
5. Часть атома, в которой сосредоточена практически вся его масса. (ядро)
6. Создатель планетарной модели атома. (Резерфорд)
7. Нейтральная частица, входящая в состав атомного ядра. (нейтрон)
8. Единое название протонов и нейтронов, входящих в состав ядра. (нуклоны)
9. Реакции слияния легких ядер при очень высокой температуре называется … (термоядерная)
Задание 3. Паспорт атома вещества. (Слайд №4)
Каждой команде предлагается заполнить таблицу, используя периодическую таблицу Д.И.Менделеева. За каждую правильную строку даётся один жетон. Команде, которая быстрее всех и правильно заполнит таблицу, добавляется ещё 1 жетон. (Приложение 2)
| Химический элемент | Атомная масса | Порядковый № | Кол-во протонов | Кол-во нейтронов | Кол-во электронов |
| Сu - медь | 64 | 29 | 29 | 35 | 29 |
| As - мышьяк | 75 | 33 | 33 | 42 | 33 |
| O - кислород | 16 | 8 | 8 | 8 | 8 |
| U - уран | 238 | 92 | 92 | 146 | 92 |
Задание 4. Идентификация. (Слайд №5)
Каждой команде даётся задание назвать (идентифицировать) изотопы. За каждый правильный ответ даётся жетон. Команде, которая быстрее всех и правильно назовёт изотопы, добавляется ещё 1 жетон. (Приложение 3)
1 команда: 18 9 Х; 20282 Х; 105 47Х. (F-фтор, Pb- свинец, Ag-свинец).
2 команда: 17 8 Х; 235 92 Х; 190 76 Х. (О-кислород, U-уран, Os-осмий)
3 команда: 37 17 Х; 124 50 Х; 202 80 Х. (Cl-хлор, Sn-олово, Hg-ртуть)
Задание 5. Закон радиоактивного распада. (Слайд №6)
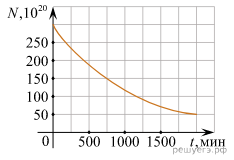
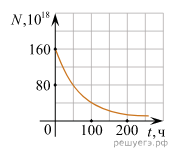
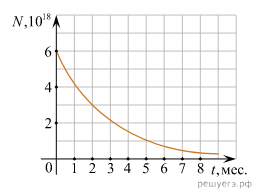
Для каждой команды даётся график изменения числа ядер находящегося в пробирке радиоактивного изотопа с течением времени. По этому графику нужно ответить на три вопроса. За каждый правильный ответ команда получает жетон. Команде, которая быстрее всех и правильно даст ответы на вопросы, добавляется ещё 1 жетон. (Приложение 4)
| 
| 
| 
|
| На рисунке представлен график изменения числа ядер находящегося в пробирке радиоактивного изотопа с течением времени. 1. Каков период полураспада этого изотопа? 2. Через какое время распадется 75% ядер? 3. Сколько ядер останется через время, равное трем периодам полураспада этого изотопа? |
Задание 6. Допиши реакцию. (Слайд №7)
Каждая команда получает неполную запись ядерных реакций, их задача - определить неизвестное и записать его. За каждую, верно записанную, реакцию команда получает один жетон. (Приложение 5)
| 188О + 11p → 10n + ? | 3517Cl + 10n → 11p + | 94Be + 11H → 105B + ? |
| 115B + ? → 10n + 147N | 136C + 11p →? | 147N + ? → 146C + 11p |
| 147N + 42He → 178О + ? | 105B + ? → 10n +137N | 147N + 42He → ? + 11H |
| ? + 10n → 94Be +42He | 2412Mg + 42He → 2714Si+ | 2713Al + 42He → 3015P + ? |
| 2713Al + 42He → 3015Р + ? | ? + 10n → 5625Mn +11p | ? + 42He → 3014Si + 11p |
4. ПОДВЕДЕНИЕ ИТОГОВ ИГРЫ. (Слайд №8)
Подсчёт жетонов, заработанных командами. Награждение победителей. Выставление оценок.
5. ДОМАШНЕЕ ЗАДАНИЕ. (Слайд №9)
Подготовиться к контрольной работе.
6. РЕФЛЕКСИЯ. (Слайд №10)
Ответьте, пожалуйста, на следующие вопросы.
– Доволен(а) ли ты тем, как прошёл урок?
– Было ли тебе интересно?
– Сумел(а) ли ты закрепить свои знания?
– Ты был(а) активен(а)?
ПРИЛОЖЕНИЕ 1
КОНВЕРТ №1
Положительная частица, входящая в состав атомного ядра, – … .
КОНВЕРТ №2
Мельчайшая частица простого вещества – … .
КОНВЕРТ №3
Элементы, имеющие одинаковое зарядовое число и разные массовые числа – … .
ПРИЛОЖЕНИЕ 2
Задание 3. Паспорт атома вещества
| Химический элемент | Атомная масса | Порядковый № | Кол-во протонов | Кол-во нейтронов | Кол-во электронов |
| Сu - медь | 64 | 29 | 29 | 35 | 29 |
| As - мышьяк | 75 | 33 | 33 | 42 | 33 |
| O - кислород | 16 | 8 | 8 | 8 | 8 |
| U - уран | 238 | 92 | 92 | 146 | 92 |
ПРИЛОЖЕНИЕ 3
Задание 4. Идентификация.
Назови (идентифицируй) изотопы
18 9 Х –
20282 Х –
105 47Х –
Задание 4. Идентификация.
Назови (идентифицируй) изотопы
17 8 Х –
235 92 Х –
190 76 Х –
Задание 4. Идентификация.
Назови (идентифицируй) изотопы
37 17 Х –
124 50 Х –
202 80 Х –
ПРИЛОЖЕНИЕ 4
Задание 5. Закон радиоактивного распада.
| 
| На рисунке представлен график изменения числа ядер находящегося в пробирке радиоактивного изотопа с течением времени. 1. Каков период полураспада этого изотопа? 2. Через какое время распадется 75% ядер? 3. Сколько ядер останется через время, равное трем периодам полураспада этого изотопа? |
Задание 5. Закон радиоактивного распада.
| 
| На рисунке представлен график изменения числа ядер находящегося в пробирке радиоактивного изотопа с течением времени. 1. Каков период полураспада этого изотопа? 2. Через какое время распадется 75% ядер? 3. Сколько ядер останется через время, равное трем периодам полураспада этого изотопа? |
Задание 5. Закон радиоактивного распада.
| 
| На рисунке представлен график изменения числа ядер находящегося в пробирке радиоактивного изотопа с течением времени. 1. Каков период полураспада этого изотопа? 2. Через какое время распадется 75% ядер? 3. Сколько ядер останется через время, равное трем периодам полураспада этого изотопа? |
ПРИЛОЖЕНИЕ 5
Задание 6. Допиши реакцию.
| 188О + 11p → 10n + ? |
| 115B + ? → 10n + 147N |
| 147N + 42He → 178О + ? |
| ? + 10n → 94Be +42He |
| 2713Al + 42He → 3015Р + ? |
Задание 6. Допиши реакцию.
| 3517Cl + 10n → 11p + |
| 136C + 11p →? |
| 105B + ? → 10n +137N |
| 2412Mg + 42He → 2714Si+ |
| ? + 10n → 5625Mn +11p |
Задание 6. Допиши реакцию.
| 94Be + 11H → 105B + ? |
| 147N + ? → 146C + 11p |
| 147N + 42He → ? + 11H |
| 2713Al + 42He → 3015P + ? |
| ? + 42He → 3014Si + 11p |