Основное уравнение МКТ. Температура и средняя кинетическая энергия движения молекул.
Древние считали газ неуловимой формой тела, представляющего собой нечто среднее между веществом и духом. Новые взгляды на газ потрясли мир в XVIIв. Первому из исследованных газов – воздуху – были приданы свойства вещества
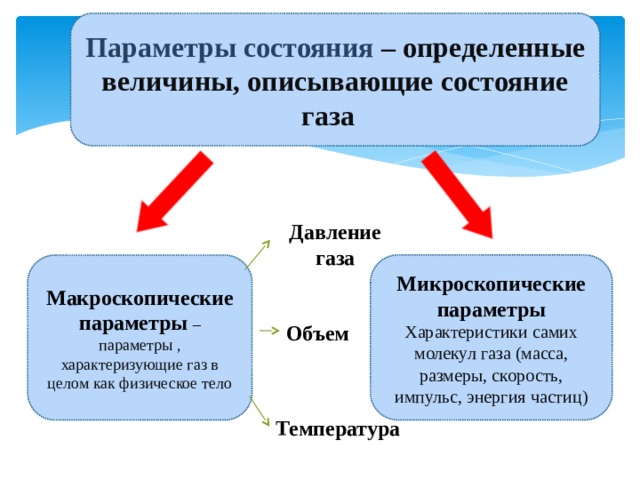
Параметры состояния – определенные величины, описывающие состояние газа
Давление газа
Микроскопические параметры
Характеристики самих молекул газа (масса, размеры, скорость, импульс, энергия частиц)
Макроскопические параметры – параметры , характеризующие газ в целом как физическое тело
Объем
Температура

Макроскопические – параметры, которые можно измерить с помощью приборов.
Микроскопические – параметры, которые измеряются косвенным путем.

Идеальный газ – это физическая модель газа, молекулы которого представляют собой материальные точки, не взаимодействуют друг с другом и их соударения являются абсолютно упругими.
- Идеальный газ – физическая модель реального газа
- Физическая модель – это некоторое описание реального явления, в котором участвует минимум параметров, необходимых для правильного описания явления и правильного решения поставленных задач.
- Модели идеального газа соответствует реальный газ находящийся под низким давлением и при высокой температуре
- Воздух и инертные газы при нормальных условиях можно приближенно считать идеальным газом

Реальный газ
Идеальный газ
(модель)
1 . Совокупность большого числа молекул, размерами которых можно пренебречь (принимают молекулы за материальные точки).
1. Молекулы реального газа не являются точечными образованиями, диаметры молекул лишь в десятки раз меньше расстояний между молекулами (имеют собственный объем) .
2. Молекулы находятся на больших расстояниях друг от друга и движутся хаотически ( все направления движения молекул равноправны ) .
2. Молекулы не взаимодействуют по законам упругих столкновений .
3. Молекулы взаимодействуют по законам упругих столкновений , силами притяжения между молекулами пренебрегают.
4. Скорости молекул разнообразны, но при определенной температуре средняя скорость молекул остается постоянной.
5. Все соударения молекул являются абсолютно упругими

Свойства идеального газа
1. Суммарный объем молекул по сравнению с объемом, занимаемым газом, пренебрежимо мал.
2. Молекулы представляют собой упругие шарики
3. Внутренняя энергия газа определяется лишь кинетической энергией.

Макропараметры идеального газа
- Давление
- Температура
- Объем
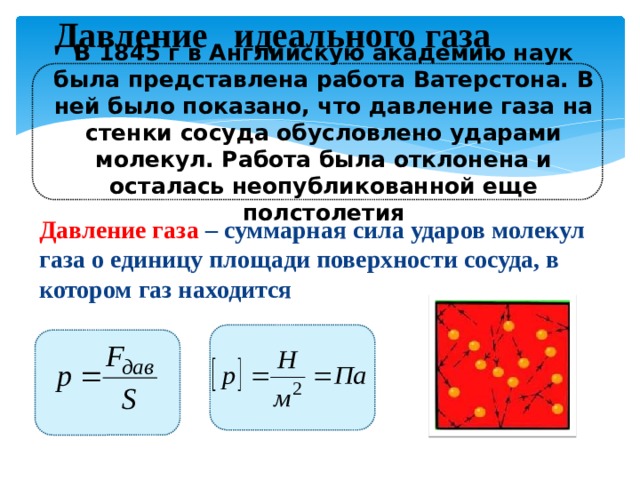
Давление идеального газа
В 1845 г в Английскую академию наук была представлена работа Ватерстона. В ней было показано, что давление газа на стенки сосуда обусловлено ударами молекул. Работа была отклонена и осталась неопубликованной еще полстолетия
Давление газа – суммарная сила ударов молекул газа о единицу площади поверхности сосуда, в котором газ находится
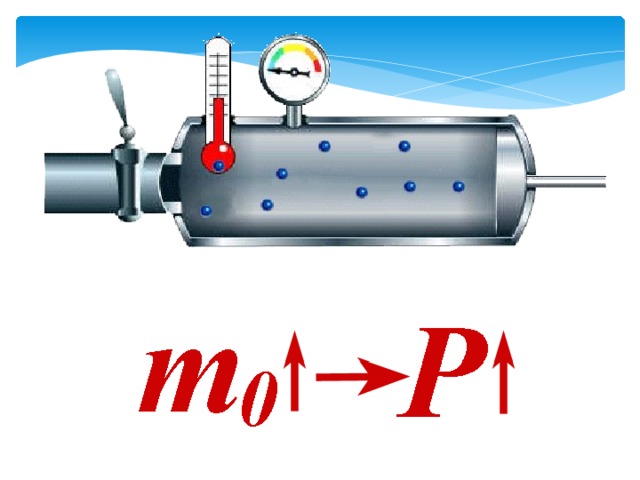
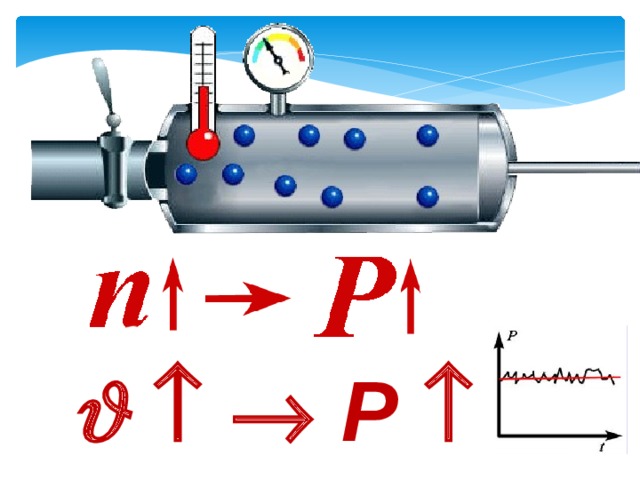
Р
![Основное уравнение МКТ идеального газа. Средний квадрат скорости движения молекул [м/с] Масса молекулы [кг] 2 Концентрация молекул [ ] Давление газа [Па]](https://fsd.multiurok.ru/html/2021/01/20/s_60083daa54f7c/img11.jpg)
Основное уравнение МКТ идеального газа.
Средний квадрат скорости движения молекул [м/с]
Масса
молекулы [кг]
2
Концентрация
молекул [ ]
Давление газа [Па]

- Это уравнение, выведенное впервые немецким физиком Р. Клаузиусом, называется основным уравнением молекулярно-кинетической теории идеального газа.
- Оно устанавливает связь между микроскопическими параметрами и макроскопическими (измеряемыми) величинами.
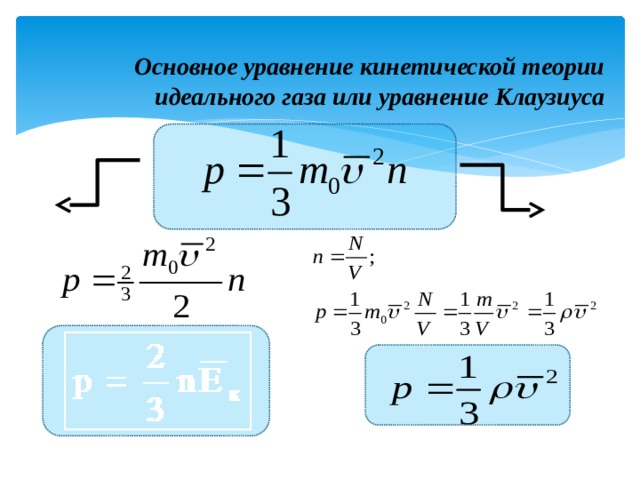
Основное уравнение кинетической теории идеального газа или уравнение Клаузиуса

Закон Дальтона
Давление смеси газов равно сумме их парциальных давлений
Парциальное давление газа – давление,
которое бы оказывал газ на стенки сосуда,
находясь в нем один
Если в сосуде содержится несколько газов, то каждый газ занимает объем, равный объему сосуда, и все газы имеют одинаковую температуру

Температура. Энергия теплового движения молекул

- Температура и тепловое равновесие
- Абсолютная температура. Температура – мера средней кинетической энергии молекул

Термодинамическое равновесие.
Термодинамическое равновесие – состояние при котором все макроскопические параметры системы остаются неизменными сколь угодно долго.
Температура – мера средней кинетической энергии системы, находящейся в состоянии термодинамического равновесия.
Экспериментально было установлено, что при одинаковой температуре средние кинетические энергии поступательного движения молекул любых газов одинаковы .
12

Измерение температуры.
Для измерения температуры используют термометры. В основе их работы лежит способность веществ (ртуть, спирт и др.) увеличивать свой объем при нагревании. Существуют различные температурные шкалы (Цельсия, Кельвина, Фаренгейта).
12

Связь абсолютной шкалы со шкалой Цельсия
Уильям Томсон,
лорд Кельвин
- британский физик и механик .
1824 - 1907
Андерс Цельсий — шведский астроном, геолог и метеоролог .
1701 - 1744
В шкале Цельсия за 0 0 С принята температура тающего льда, а за 100 0 С – температура кипения воды при нормальном давлении.
Единица температуры по абсолютной шкале называется Кельвином и выбрана равной одному градусу по шкале Цельсия 1К=1 0 С. За абсолютный нуль принимается температура, при которой тепловое (хаотическое)движение молекул полностью прекращается

Запомни!
В формулах абсолютная температура обозначается буквой « Т »,
а температура по шкале Цельсия буквой « t ».
Т = t + 273

Молекулярно - кинетический смыл температуры.
Установлено, что при тепловом равновесии средние кинетические энергии поступательного движения молекул всех газов одинаковы, т.е.
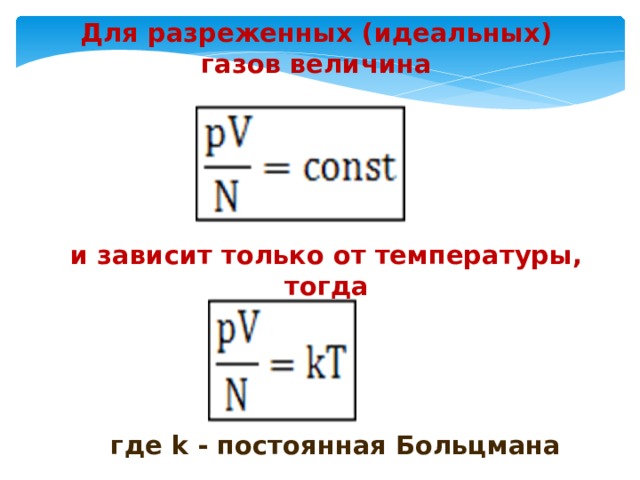
Для разреженных (идеальных) газов величина
и зависит только от температуры, тогда
где k - постоянная Больцмана

Следовательно ,
Средняя кинетическая энергия поступательного движения молекул

- Постоянная Больцмана связывает температуру в энергетических единицах с температурой Т в кельвинах
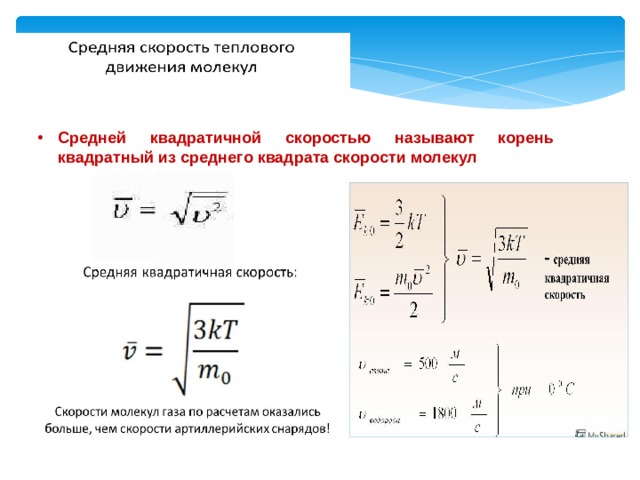
- Средней квадратичной скоростью называют корень квадратный из среднего квадрата скорости молекул
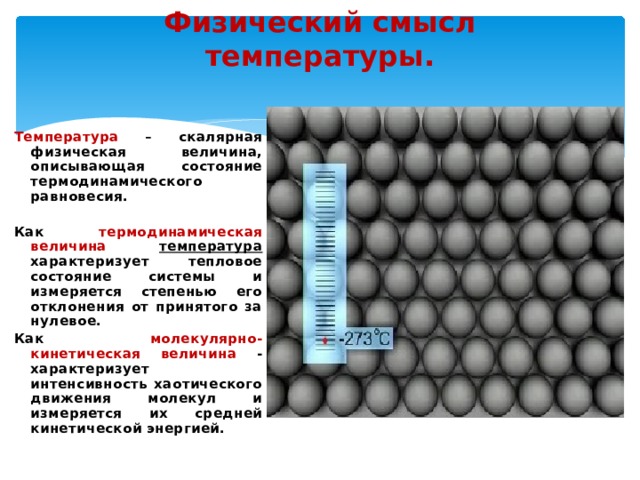
Физический смысл температуры.
Температура – скалярная физическая величина, описывающая состояние термодинамического равновесия.
Как термодинамическая величина температура характеризует тепловое состояние системы и измеряется степенью его отклонения от принятого за нулевое.
Как молекулярно-кинетическая величина - характеризует интенсивность хаотического движения молекул и измеряется их средней кинетической энергией.
24

1
2
Т =
E
3
k
Температура - это физическая величина, являющаяся мерой средней кинетической энергии поступательного движения молекул.

Домашнее задание
- §57, 59 , стр. 202
- стр. 192 , задачи А1-А4

















![Основное уравнение МКТ идеального газа. Средний квадрат скорости движения молекул [м/с] Масса молекулы [кг] 2 Концентрация молекул [ ] Давление газа [Па]](https://fsd.multiurok.ru/html/2021/01/20/s_60083daa54f7c/img11.jpg)